
Растворы полимеров
Под растворением понимается взаимное диспергирование вдруг в друге молекул полимера и растворителя. Взаимодействия полимеров с растворителями имеет огромное значение и в процессах синтеза, переработки и эксплуатации полимеров [1, 3, 6…9, 12…14]. В зависимости от степени диспергирования полимера в растворителе могут образовываться истинные растворы и коллоидные системы.
Основными признаками истинных растворов являются самопроизвольное образование и гомофазность. Коллоидные системы образуются принудительно и являются гетерофазными.
Растворение,
или самопроизвольное диспергирование,
как любой самопроизвольный процесс при
постоянных давлении и температуре,
может происходить, если сопровождается
уменьшением свободной энергии
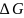 системы. В истинных растворах при
заданных температурах и давлениях
концентрация раствора, его свойства и
структура будут одними и теми же
независимо от способа его получения.
системы. В истинных растворах при
заданных температурах и давлениях
концентрация раствора, его свойства и
структура будут одними и теми же
независимо от способа его получения.
Свойства и структура коллоидных систем зависят от способа их приготовления. В коллоидных системах всегда имеют место процессы агрегирования, в результате чего системы распадаются на две фазы.
Истинные растворы полимеров имеют специфические отличия от растворов низкомолекулярных соединений, а именно: образование истинных растворов полимеров протекает через стадию набухания; растворы полимеров, даже очень разбавленные, отличаются высокой вязкостью. Свойства растворов полимеров имеют существенные отклонения от свойств, описываемых классическими законами термодинамики.
Механизм растворения полимеров.
Механизм процесса растворения полимеров сводится к следующим явлениям:
— проникновению или диффузин молекул растворителя в полимер через области с наиболее рыхлой упаковкой макромолекул по механизму капиллярного всасывания (рис.1):

Рисунок 1.
— одновременному возникновению взаимодействия между молекулами растворителя и молекулами полимера, которое называется сольватацией. Явления сольватации и образования сольватированных комплексов происходят за счет возникновения между молекулами растворителя и функциональными группами полимера водородных или донорно-акцепторных связей, π-комплексов, физического взаимодействия и др. (рис.2):

Рисунок 2.
В результате сольватации ослабляется молекулярное взаимодействие в полимере, молекулы растворителя как бы обволакивают функциональные группы и раздвигают макромолекулы полимера. Полимер увеличивается в объеме, возрастает его масса за счет проникающего в фазу полимера растворителя. Говорят, что полимер набухает. Следовательно, набухание — поглощение (сорбция) растворителя полимером, сопровождающееся изменением структуры и увеличением его массы и объема;
— отделению полностью от сольватированных макромолекул от остальной массы набухшего полимера и диффузии этих макромолекул в объеме растворителя, т.е. собственно растворению, образованию гомогенной системы.
Обязательным условием растворения является уменьшение свободной энергии системы при смешении компонентов. Поскольку свободная энергия системы по закону термодинамики связана с энтальпией H и энтропией S, то самопроизвольное растворение полимера возможно, если:
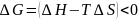 .
.
С изменением свободной энергии системы вплотную связано второе условие самопроизвольного растворения полимеров — наличие термодинамического сродства между компонентами. Растворение идет лишь в том случае, если между компонентами имеется термодинамическое сродство. Термодинамическое сродство компонентов друг к другу количественно оценивают по снижению величин химического потенциала растворителя и полимера после их взаимодействия с образованием раствора. Химический потенциал компонентов системы связан с величиной свободной энергии. Под химическим потенциалом компонента μi многокомпонентной системы данного состава понимают приращение свободной энергии системы dGi при добавлении к ней бесконечно малого количества i-го компонента при постоянных P, T и числе молей всех остальных компонентов.
 ;
;
Химический потенциал индивидуальных компонентов обозначается μ0. Таким образом, для самопроизвольного растворения полимера в растворителе необходимо, чтобы химический потенциал компонента в растворе (μi полимера или μi растворителя) был меньше химического потенциала данного компонента в чистом виде μ0, т.е.
 .
.
Чем
больше абсолютное значение отрицательной
величины
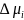 ,
тем больше сродство между компонентами,
тем легче идет растворение.
,
тем больше сродство между компонентами,
тем легче идет растворение.
С точки зрения термодинамического сродства растворители подразделяют условно на «хорошие» и «плохие» соответственно с большим отрицательным значением и малым отрицательным значением .
В процессе растворения на стадии набухания различают межструктурное и внутриструктурное, неограниченное и ограниченное набухание. Если молекулы растворителя могут проникать только в участки между надмолекулярными структурами, то имеет место межструктурное набухание. Если растворитель проникает между отдельными макромолекулами, то происходит внутриструктурное набухание полимеров.
Неограниченное набухание — это набухание, самопроизвольно переходящее в растворение и характерное для линейных аморфных полимеров с невысокой степенью полимеризации. Сольватированные макромолекулы таких полимеров легко переходят в раствор (рис.3, кривые 1…2).
Ограниченное набухание — процесс взаимодействия полимера с растворителем, не сопровождающийся растворением. Ограниченное набухание характерно для сетчатых полимеров, полимеров с высокой молекулярной массой и в случае невысокого термодинамического сродства полимера и растворителя (рис.3, кривые 3…5). Процесс набухания характеризуется полимеров кинетическими кривыми набухания, а интенсивность набухания полимеров количественно оценивается степенью набухания Q (рис.3). Участки о-а кривых набухания отражают постепенно замедляющееся увеличение степени набухания. Для растворимых полимеров на участках а-в кривых 1 и 2 скорость набухания становится сопоставимой со скоростью растворения, а на участке в-с идет интенсивное растворение полимеров, которое сопровождается уменьшением массы образцов. Кинетика ограниченного набухания сетчатых полимеров описывается кривыми 3, 4 и 5.

Рисунок 3.
Степень набухания полимеров Q выражается через увеличение их массы Qm или объема QV:
 ;
;
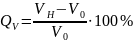 ,
где
,
где
 и
и
 — соответственно масса и объем исходного
полимера;
— соответственно масса и объем исходного
полимера;
 и
и
 — масса и объем набухшего полимера.
— масса и объем набухшего полимера.
Скорость набухания оценивают по увеличению массы или объема полимера во времени:
 ;
;
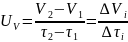 ,
где m1,
V1
—
соответственно масса и объем полимера
в момент времени
,
где m1,
V1
—
соответственно масса и объем полимера
в момент времени
 ;
;
 ,
,
 —
масса и объем полимера в момент времени
—
масса и объем полимера в момент времени
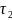 .
.
По
величине максимальной степени набухания
 можно
судить о термодинамическом сродстве
полимеров и растворителей. Для
полимергомологов, испытанных в одинаковых
условиях, по кривым набухания можно
дать качественную оценку молекулярной
массе, судить о наличии пространственной
сшитой структуры и т.д.
можно
судить о термодинамическом сродстве
полимеров и растворителей. Для
полимергомологов, испытанных в одинаковых
условиях, по кривым набухания можно
дать качественную оценку молекулярной
массе, судить о наличии пространственной
сшитой структуры и т.д.
