
- •Предельные углеводороды. Алканы
- •Алкены. Олефины
- •Диеновые углеводороды (диены)
- •Алкины. Ацетиленовые углеводороды
- •Ароматические углеводороды. Арены
- •Предельные одноатомные и многоатомные спирты
- •Плавлением сульфокислот со щелочами (чаще всего используется NaOh)
- •Качественная реакция на фенол:
- •Альдегиды и кетоны
- •2Ch3 – coh ch3 – ch(oh) – ch2 – coh (альдоль)
- •Литература:
- •Оглавление:
Плавлением сульфокислот со щелочами (чаще всего используется NaOh)

в промышленности


гидролизом хлорбензола


из бурых углей и каменноугольной смолы.
Химические свойства. Характерны свойства ароматических углеводородов и спиртов. При этом возрастает кислотность ОН-группы и повышается реакционная способность бензольного кольца.
Кислотность фенола

С6Н5ОН
+ NaOH
![]() C6H5ONa
+ H2O
C6H5ONa
+ H2O
Кдисс. = 1,7·10-10, т.е. фенол , как кислота, слабее H2S и Н2СО3, но сильнее R-OH.
C6H5 – ONa + H2O + CO2 C6H5OH + NaHCO3
Образование простых эфиров

Образование сложных эфиров. Фенолы не образуют сложные эфиры непосредственно с органическими кислотами, нужно использовать хлорангидриды органических кислот (CH3 – C(Cl) = O – хлорангидрид уксусной кислоты)
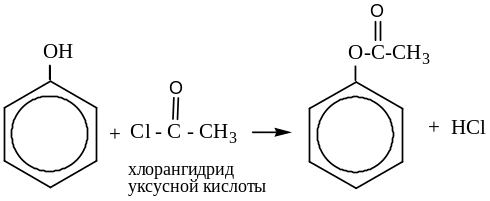
Реакции замещения ароматического кольца
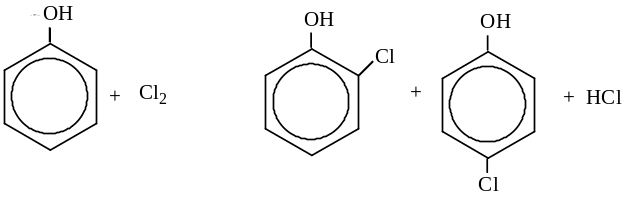

Качественная реакция на фенол:




5) Каталитическое гидрирование протекает в газовой фазе при 1800С, катализатор Ni. В жидкой фазе реакция протекает при повышенном давлении.

Побочно образуется циклический кетон:

Окисление
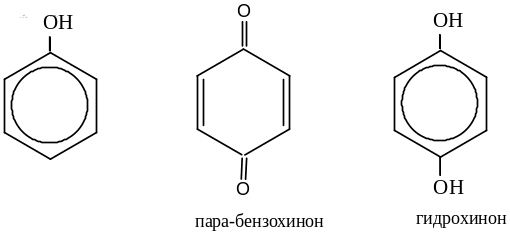
Условия окисления: хромовая смесь K2Cr2O7 + H2SO4.
7) Качественная реакция на фенолы
3С6Н5ОН + FeCl3 (C6H5O)3Fe↓ + 3HCl
красно-фиолетовый
Крезолы – голубые, другие фенолы – зеленые.
Задачи
Для грунтовки досок в иконописных мастерских использовали казеиновый клей. При анализе этого клея было выяснено, что одно из составляющих его органических веществ. в котором массовые доли углерода, кислорода и водорода, соответственно равны 76,59%, 17,02% и 6,38%, было известно на Руси за 250 лет до того, как было официально получено и зарегистрировано английским ученым. Укажите формулу этого вещества. Тип № 4.
Решение: Пусть масса вещества составляла 100 г. Тогда массы элементов углерода, кислорода и водорода составят: mC = 76,59 г, mO = 17,02 г, mH = 6,38 г.
Разделим массы элементов на их атомные массы и получим при этом число моль каждого элемента в 100 г данного вещества:
-
m(г)
C
O
H
76,59
17,02
6,38
n
6,38
1,06
6,38
Разделим эти цифры на наименьшее число (1,06): 6,0; 1; 6.0
Таким образом, неизвестное вещество – С6Н6О, т.е. фенол.
Ответ: формула вещества С6Н5ОН, фенол.
Выведите формулу вещества, относящегося к спиртам, и предложите его изомеры, содержащим ароматический радикал, придающего краске для волос светоустойчивость, если при полном гидрировании 0,2 моль этого вещества поглощается 1,2 г водорода, 55 г этого вещества, с молярной массой 110 г/моль взаимодействует с 23 г натрия. Тип № 4.
Решение. Рассчитаем число моль водорода: n(H2) = 1,2 : 2 = 0,6 моль.
Число моль неизвестного вещества при взаимодействии с натрием составит n(X) = 55 : 110 = 0,5 моль.
Число моль натрия: n(Na) = 23 : 23 = 1 моль. Из соотношения n(X) : n(Na) очевидно, что на 1 моль неизвестного вещества приходится 2 моль натрия. Поэтому можно предположить, что неизвестное вещество представляет собой одноядерный (с учетом соотношения молей реагентов при гидрировании) двухатомный фенол, т.е. дигидроксибензол – С6Н6О2.
Молярная масса дигидроксибензола М(С6Н6О2) = 110 г/моль. Изомеры: 1,2; 1,3; 1,4 – дигидроксибензолы.
Ответ: один из трех дигидроксибензолов или их смесь.
32. Вычислите выход реакции гидролиза салола (С6Н5ОСОС6Н4ОН), если в 100 г зубной пасты «Жемчуг» содержится его от 5,3 до 6,8%, а число молекул фенола, образующегося при чистке зубов в процессе гидролиза от 1,2 · 1022 до 1,395 ∙ 1023 молекул. Другим продуктом гидролиза является ароматическая спиртокислота. Тип № 8.
Решение. Уравнение гидролиза салола имеет вид:
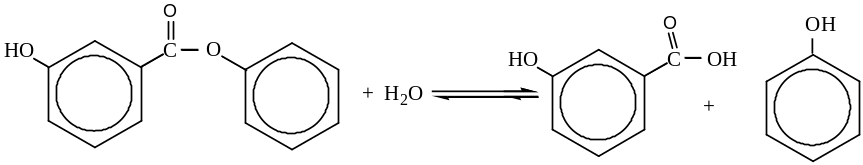
Примем, что в 100 г зубной пасты содержится 5,3% салола, а число молекул фенола, образующегося при чистке зубов в процессе гидролиза 1,2 ∙ 1022 молекул. Тогда масса салола составит 5,3 г.
Молярная масса салола М(С13Н10О3) = 214 г/моль. Число моль салола n(салола) = 5,3 : 214 = 0,025 моль.
Число моль фенола n(C6H5OH) = 1,2 · 1022 : 6,02 ∙ 1023 = 0,02 моль (6,02 ∙ 1023 – число Авогадро).
Выход
гидролиза салола
![]() .
.
Ответ: выход гидролиза салола 80%.
Для опровержения заявления представителей предприятия «Оргсинтез» о невозможности нахождения в сбросах их сточных вод фенола, ученики 14 школы г.Дзержинска Нижегородской области провели эксперимент: собрав сточную воду в банку, емкостью 3 л, они добавили 1М раствор хлорида трехвалентного железа и выделился фиолетовый осадок, массой 2,0
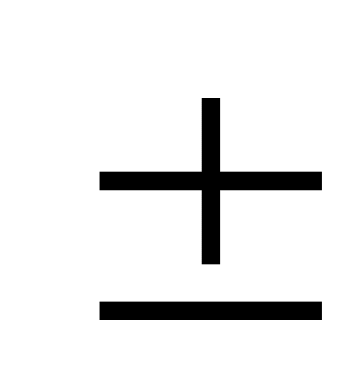 2,5 г. Какова была масса фенола в сточной
воде и превзошла ли она ПДК = 0,001 моль/л.
Тип № 8.
2,5 г. Какова была масса фенола в сточной
воде и превзошла ли она ПДК = 0,001 моль/л.
Тип № 8.
Решение. Хлорид трехвалентного железа был наверняка в большом избытке. Протекала следующая реакция:
3С6Н5ОН + FeCl3 (C6H5O)3Fe↓ + 3HCl
Пусть масса осадка составила 2,5 г. Молярная масса фенолята железа (III) М = (72 + 15 + 16)∙3 + 56 = 335 г/моль. Число моль вещества осадка составит n(осадка) = 2,5 : 335 = 0,0075 моль, следовательно по уравнению реакции число моль фенола будет в три раза больше, т.е. n(C6H6O) = 0,0075 · 3 = 0,0225 моль.
Найдем массу фенола m(C6H6O) = 0,0225 ∙ 94 = 0,21 г.
Эта масса содержится в 3 л воды. В одном литре m(C6H6O) = 0,21 : 3 = 0,07 г/л = 70 мг/л, что в 70000 раз превышает ПДК.
Ответ: m(C6H6O) = 70 мг/л, превышает ПДК.
Какой продукт образуется в результате последовательного превращения ацетилена по реакциям тримеризации, замещения с хлором, обмена с водой, замещения с бромом? Тип № 4.
Решение. Реакция тримеризации ацетилена
![]()
Реакция замещения бензола с хлором
![]()
Реакция взаимодействия хлорбензола с раствором щелочи
![]()
Реакция взаимодействия фенолята натрия с соляной кислотой
Реакция бромирования фенола
Ответ: 2,4,6 – трибромфенол.
