
- •Введение
- •1. Реакция горения
- •1.1. Уравнение материального баланса процесса горения
- •1.2. Горючесть и коэффициент горючести веществ
- •2.Материальный и тепловой баланс процесса горения
- •2.1. Избыток воздуха
- •2.2. Расчёт объёма воздуха для горения индивидуальных химических соединений, находящихся в твёрдом и жидком агрегатном состоянии
- •2.5. Расчёт объёма и состава компонентов продуктов горения индивидуальных химических соединений, находящихся в газообразном агрегатном состоянии
- •2.6. Расчёт объёма воздуха для горения веществ сложного состава, находящихся в твёрдом и жидком агрегатном состоянии
- •2.7. Расчёт объёма воздуха, необходимого для сгорания смеси газов
- •2.8. Расчёт объёма и процентного состава компонентов продуктов горения веществ сложного состава, находящихся в твёрдом (жидком) агрегатном состоянии
- •2.9. Расчёт объёма и процентного состава компонентов продуктов горения смеси газов
- •2.10. Расчёт теплоты сгорания
- •2.11. Расчёт температуры горения
- •3.2. Расчет минимальной флегматизирующей концентрации и минимального взрывоопасного содержания кислорода
- •3.3. Расчет температуры вспышки паров жидкостей
- •3.4. Расчет температурных пределов распространения пламени
- •4. Самовоспламенение и самовозгорание
- •4.1. Расчет температуры самовоспламенения паров веществ по средней длине углеродной цепи
- •4.2. Расчет йодного числа жиров, масел и других веществ
- •5. Основные параметры взрыва
- •5.1. Расчёт температуры и давления взрыва
- •Расчетно-аналитические зависимости для решения задач по курсу «Теория горения и взрыва»
- •153040, Г.Иваново, пр.Строителей, 33
4. Самовоспламенение и самовозгорание
4.1. Расчет температуры самовоспламенения паров веществ по средней длине углеродной цепи
Стандартной температурой самовоспламенения паров жидкости в воздухе называется определенная стандартным методом самая низкая температура, до которой должна быть нагрета наиболее легковоспламеняемая смесь (смесь близкая к стехиометрической) данного газа или пара с воздухом, чтобы она воспламенилась без внесения в нее постороннего источника зажигания.
Температура самовоспламенения (ТСВ) определяется по таблицам, исходя из средней длины углеродной цепи в молекуле данного класса соединений. Расчетная формула условной средней длины углеродной цепи в молекуле имеет вид:
 (4.1.1)
(4.1.1)
Здесь ci - длина i - ой углеродной цепи в молекуле;
mi - число углеродных цепей, длина которых составляет ci;
![]() - общее число углеродных цепей в молекуле.
Оно находится по формуле:
- общее число углеродных цепей в молекуле.
Оно находится по формуле:
= 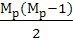 (4.1.2)
(4.1.2)
В формуле (4.1.2) Мр - число концевых групп в молекуле.
Концевыми группами являются:
- в молекуле парафинового углеводорода метильные группы – СН3;
- в молекуле спирта – метильные и гидроксильные ОН;
- в молекуле ароматического углеводорода – метильные группы и ароматическое кольцо. Ароматическое кольцо считают только концевой групп
пой, если в нем замещен только один атом водорода. Если в ароматическом кольце замещены два и более атомов водорода, то его считают и концевой и промежуточной группой.
Расчет длины углеродных цепей для каждого класса соединений имеет свои особенности. При подсчете числа атомов углерода в каждой цепи применяются следующие правила:
а) для парафинов расчетное число атомов углерода в цепи равно фактическому числу атомов углерода;
б) для спирта расчетное число атомов углерода в цепи, включающей ОН-группу равно фактическому числу атомов углерода, увеличенному на единицу;
в) для ароматического углеводорода расчетное число атомов углерода в цепи, включающей ароматическое кольцо, равно фактическому числу атомов углерода в цепи, уменьшенному на единицу. Атомы углерода ароматического кольца при подсчете длины углеродной цепи не учитываются.
В зависимости от полученного значения Lср по таблице для данного класса соединений определяют температуру самовоспламенения.
4.2. Расчет йодного числа жиров, масел и других веществ
Йодное число – это масса йода, поглощенная 100 граммами жира или масла. Йодное число характеризует количество глицеридов непредельных кислот, содержащихся в масле или жире. Оно является критерием склонности жиров и масел к самовозгоранию. Масла, имеющие йодное число более 50, считаются склонными к самовозгоранию.
Пример. Определить йодное число льняного масла, содержащего 5 % (по массе) глицеридов пальмитиновой и стеариновой кислот, 18 % глицерида олеиновой кислоты, 30 % глицерида линолевой кислоты и 47 % глицерида линоленовой кислоты.
Решение.
Глицериды пальмитиновой и стеариновой кислот являются предельными, поэтому при низких температурах они не присоединяют йод.
Определяем количество йода, присоединяющегося к глицериду олеиновой кислоты.
Уравнение реакции: (С17Н33СОО)3С3Н5+ 3 I2 = (С17Н33I2СОО)3С3Н5
Молекулярная масса глицерида олеиновой кислоты 884 г/моль, йода 254 г/моль.
К 884 г глицерида олеиновой кислоты присоединяется 254 3 г йода.
К 18 г глицерида олеиновой кислоты (столько содержится в 100 г масла) присоединяется Х1 г йода.
Х1 = 254 3 18/884 = 15,5 г
Определяем количество йода, присоединяющегося к глицериду линолевой кислоты.
Уравнение реакции: (С17Н31СОО)3С3Н5+ 6 I2 = (С17Н33I4СОО)3С3Н5
Молекулярная масса глицерида линолевой кислоты 878 г/моль.
К 878 г глицерида олеиновой кислоты присоединяется 254 6 г йода.
К 30 г глицерида линолевой присоединяется Х2 г йода
Х2 = 254 6 30/878 = 52,1 г
Определяем количество йода, присоединяющегося к глицериду линоленовой кислоты.
Уравнение реакции: (С17Н29СОО)3С3Н5+ 9 I2 = (С17Н33I6СОО)3С3Н5
Молекулярная масса глицерида линоленовой кислоты 872 г/моль.
К 872 г глицерида олеиновой кислоты присоединяется 254 9 г йода.
К 47 г глицерида линоленовой присоединяется Х3 г йода
Х2 = 254 9 47/872 = 123,2 г
Йодное число льняного масла равно:
И.ч. = Х1 + Х2 + Х3 = 15,5 + 52,1 + 123,2 = 190,8 г
