
- •Российской академии медицинских наук
- •7 Июня 2001 г.
- •Раздел 1. Нейротравматология. Использование аутокости для реконструктивных операций на краниоорбитальной области.
- •Некоторые аспекты черепно-мозговой травмы при дорожно-транспортных происшествиях.
- •Раздел 2. Пороки развития. Гидроцефалия. Лобная плагиоцефалия (клиника, диагностика, тактика хирургического лечения).
- •Изолированный 4-й желудочек. Клиническое наблюдение и обзор литературы.
- •Раздел 3. Нейроонкология. Первичные интракраниальные меланомы.
- •Провакационные (тестирующие) фармакологические тесты, применяемые при эмболизации опухолей.
- •Материалы и методы.
- •Прогностическое значение иммуногистохимического выявления онкопротеинов р53, р21,р27 и KiS1 в олигодендроглиомах больших полушарий головного мозга. Ю.Л. Яковлев, а.Г. Коршунов.
- •Раздел 4. Хирургия основания черепа. Доступ к основанию черепа через лобную пазуху (клинико-анатомическое исследование).
- •Дефекты основания черепа после удаления краниофациальных опухолей (классификация, пластическое закрытие).
- •III группа. Комбинированные дефекты (6 больных).
- •Структура летальности у больных, оперированных по поводу аденам гипофиза в зависимости от хирургического доступа.
- •Хирургическое лечение опухолей краниовертебрального перехода.
- •Эндоскопическая эндоназальная диагностика краниофациальных новообразований.
- •Краниоорбитальные менингиомы. Нейроофтальмологическая симптоматика раннего послеоперационного периода.
- •Введение.
- •Материалы и методы.
- •Применение экстрадурального доступа к аденомам гипофиза, врастающим в кавернозный синус.
- •Невриномы яремного отверстия.
- •Тактика хирургического лечения петрокливальных менингиом с супра- и субтенториальным распространением.
- •Статистический анализ.
- •Хирургия интракраниальных менингиом, распространяющихся в подвисочную ямку.
- •Раздел 5.
- •Хирургия позвоночника, спинного мозга и периферической нервной системы.
- •Возможности реконструктивных операций
- •У больных в позднем периоде спинномозговой травмы.
- •Процессы апоптоза при экспериментальном повреждении спинного мозга
- •Минимально инвазивные эндоскопические доступы к поясничному отделу позвоночника.
- •Хирургическое лечение патологии плечевого сплетения с учетом данных клиники и магнитно-резонансной томографии.
- •Микродискэктомия при повреждениях шейного отдела позвоночника.
- •Микрохирургическая и расширенная декомпрессия при стенозе поясничного отдела позвоночного канала. Патогенетический выбор оперативного лечения.
- •Первый опыт вертебропластики при гемангиомах тел позвонков.
- •Малоинвазианая хирургия в лечении болевых синдромов при спондилоартрозах шейного отдела прозвоночника
- •Материалы и методы
- •Результаты и их обсуждение
- •Раздел 6. Нейрофизиология. Транскраниальной магнитной стимуляции для верификации доминантного по речи полушария
- •Оценка состояния моторной системы у больных в коме
- •Проблемы мониторинга мозгового кровообращения у больных с тяжёлой черепно-мозговой травмой.
- •Содержание. Предисловие …………………………………………………...3
- •Раздел 1. Нейротравматология.
- •Раздел 2. Пороки развития. Гидроцефалия.
- •Раздел 3. Нейроонкология.
- •Раздел 4. Хирургия основания черепа.
- •Раздел 5. Хирургия позвоночника, спинного мозга и периферической нервной системы.
- •Раздел 6. Нейрофизиология.
Оценка состояния моторной системы у больных в коме
Гимранов Р.Ф., Мальцева Е.А
При тяжелом повреждении головного мозга с постоянным отсутствием сознания, но без признаков смерти мозга, больные пребывают в состоянии, называемом комой. Для этого состояния характерна неразбудимость больного, открывание глаз невозможно даже на сильные раздражения.
Была проведена регистрация и анализ вызванных моторных ответов (ВМО) с мышц правой и левой кисти при транскраниальной магнитной стимуляции (ТМС) правого и левого полушария у 32 больных с нейрохирургической патологией находящихся в коме. ВМО при ТМС правого и левого полушария удалось получить у 11 (34,4%) больных находящихся в коме. У 14 (43,8%) удалось получить ВМО при ТМС левого полушария, у 17 (53,1%) удалось получить ВМО при ТМС правого полушария и у 12 (37,5%) больных ВМО не удалось получить при ТМС как правого, так и левого полушария. Среднестатистический уровень индукции магнитного поля вызывающий ВМО при ТМС правого полушария у больных в коме составил 98,6%, левого полушария 96,8% от максимальной индукции магнитного стимулятора (2,2 Тл). У больных в коме (у кого были получены ответы) отмечалось резкое снижение среднестатистических значений амплитуды ВМО при ТМС как правого, так и левого полушария. При анализе временных характеристик ВМО отмечалось увеличение как латентности, так и центрального времени проведения. Периферическое проведение импульса (спинной мозг, плечевое сплетение, периферические нервы) у данных больных не страдало. Удлинение времени проведения импульса отражало именно дисфункцию пирамидного тракта, причиной которого могли послужить как травматические, так и ишемические поражения. Таким образом, у больных с нейрохирургической патологией, находящихся в коме, отмечались выраженные изменения как в моторной коре, так и пирамидном тракте.
Проблемы мониторинга мозгового кровообращения у больных с тяжёлой черепно-мозговой травмой.
Козлова Е.А, Ошоров А.В., Шовикова О.А., Анзимиров В.Л., Сафин А. М.
Нарушения мозгового кровообращения являются одним из наиболее тяжёлых осложнений острого периода черепно-мозговой травмы (1). Непосредственно за первичными проявлениями травмы мозга, обусловленными разрывом аксонов и блокадой нейрональных связей, быстро проявляются и нарастают явления так называемой вторичной травмы мозга вследствие сопутствующего снижения АД с развитием гипоксии и отёка мозга, с ростом внутричерепного давления (ВЧД), прогрессирующим в течение первых суток после травмы. Спустя 3 - 4 суток после черепно-мозговой травмы, сопровождавшейся субарахноидальным кровоизлиянием, следует ожидать развития нового грозного осложнения - распространённого ангиоспазма церебральных артерий в результате токсического воздействия на сосудистую стенку продуктов распада крови. Своевременная диагностика и быстрая коррекция разнообразных гемодинамических факторов, осложняющих течение травматической болезни мозга и, в конечном итоге, определяющих её прогноз, весьма актуальны. Поэтому правильная организация использования неинвазивных ультразвуковых методов оценки мозгового кровообращения у больных с тяжёлой черепно-мозговой травмой является важнейшей практической задачей.
Наилучшим объектом для мониторинга церебральных артерий является исследование линейных скоростей кровотока (ЛСК) в средних мозговых артериях (СМА), васкуляризирующих всю конвекситальную поверхность коры обоих полушарий мозга. Полученные данные необходимо сопоставлять с характеристиками кровотока по внутренним сонным артериям (ВСА) и по возможности дополнять исследованиями ЛСК в передних (ПМА) и задних (ЗМА) мозговых артериях и в вертебро-базилярной системе. Поскольку при постоянстве диаметра сосуда и угла инсонации регистрируемые изменения ЛСК пропорциональны изменениям объёмного кровотока, получаемая информация имеет исключительную ценность для клиники.
Специфика обследования больных в условиях отделения интенсивной терапии требует выделения в первую очередь нескольких наиболее важных и определяющих диагностических критериев, способствующих наиболее быстрой оценке состояния пациентов. Основным показателем кровообращения является ЛСК. Снижение максимальных ЛСК в обеих СМА ниже 28 см/с свидетельствует об угрозе ишемии мозга и требует немедленной коррекции. Не менее опасным является и рост ЛСК свыше 140 см/с, указывающий на развитие вазоспазма, являющегося одной из существенных причин развития клинических осложнений, в особенности, если отношение ЛСК в СМА и ВСА (индекс Линденгаарда) превышает 3,0. Вторым по значимости показателем является пульсационный индекс Гослинга (PI), определяющий уровень циркуляторного сопротивления в исследуемом сосуде. Поскольку во многих работах была убедительно доказана зависимость этого показателя от уровня ВЧД, увеличение индекса может своевременно сигнализировать о развитии внутричерепной гипертензии, опасной для мозгового кровообращения при снижении перфузионного давления мозга (ПД) ниже 60 мм рт. ст. (ПД представляет собой разницу между средним артериальным и внутричерепным давлениями). Прогрессирующее снижение ПД приводит к изменению формы пульсаций допплерограммы с формированием резистивного паттерна кровотока, переходящего в т.н. реверберирующий тип кривой, систолическая и диастолическая части которой приобретают противоположную направленность и свидетельствуют о неэффективности кровотока.
Адекватная оценка функциональных возможностей мозгового кровообращения невозможна без проведения соответствующих функциональных проб, исследующих резервные возможности сосудов головного мозга. Для этой цели широко используются исследования реактивности сосудов к изменениям СО2, фармакологические тесты, а в последние годы применяется компрессионный тест, позволяющий оценить состояние как дилататорного, так и констрикторного резервов ауторегуляции мозгового кровообращения.
Задачей настоящей работы является изучение роли ультразвуковых характеристик мозгового кровообращения как в остром периоде тяжёлой черепно-мозговой травмы, так и в отдалённом периоде после перенесенной травмы мозга. В остром периоде черепно-мозговой травмы особенности церебральной гемодинамики были нами изучены у 11 больных в возрасте от 5 до 70 лет. Все поступившие больные находились в коматозном состоянии. У 6 из них уровень комы по шкале Глазго соответствовал 4-5 баллам, а у остальных 5 - оценивался 6 - 8 баллами. По данным КТ мозга тяжесть состояния 5 больных была обусловлена диффузным поражением мозга; у 6 – наличием острых эпи-, суб- и внутримозговых гематом, по поводу которых проводились оперативные вмешательства. Неврологический статус 5-ти пострадавших характеризовался доминированием грубых стволовых симптомов, а у остальных 6-ти наличием очаговой полушарной симптоматики. У всех больных имели место нарушения витальных функций, в связи с чем у них проводилась искусственная вентиляция лёгких (ИВЛ) в режиме нормовентиляции (рСО2 = 32 – 34 мм рт. ст.) и коррекция гемодинамических расстройств, как путём использования крупномолекулярных декстранов, так и применением вазопрессоров и симпатомиметических средств. Летальные исходы наступили у 2-х больных в течение первой недели после полученной травмы, остальные после стабилизации витальных функций были переведены в общее отделение при уровне комы 9-14 баллов по шкале Глазго.
Начиная с первых суток после поступления больных в отделение реанимации, проводили повторные динамические ультразвуковые исследования мозгового кровотока методом дуплексной транскраниальной допплерографии с помощью системы «Sonos 5500». Обследования больных в условиях общего отделения проводили на приборе «Pioneer 2020 EME-Nicolett».
Анализ полученных результатов показал, что в течение первых двух недель после травмы межполушарные асимметрии ЛСК и PI , как правило, отсутствовали, а коэффициенты овершута (КО) свидетельствовали о глубоком угнетении сосудистых ауторегуляторных реакций (см. рис. 1).
А Б


Рис.1. А. Компрессионная проба, проведенная в остром периоде черепно-мозговой травмы, выявляет значительное снижение сосудистой реактивности (КО = 1,06). Б. Показано увеличение ЛСК по прямому синусу до 70 см/с, обусловленное нарастанием гипертензионных явлений.
Спустя
2 недели, одновременно с появлением
межполушарной асимметрии этих показателей
отмечалось появление очаговых полушарных
симптомов и в неврологическом статусе.
Графики динамики ЛСК, индекса пульсации
(PI)
и коэффициентов овершута (КО) представлены
на рис 2.



У 7 больных было отмечено обусловленное вазоспазмом повышение ЛСК в зонах васкуляризации обеих СМА (рис. 3), у двоих из них вазоспазм распространялся и на бассейн одной из ПМА. Величины индексов Линденгаарда у обследованных больных колебались в пределах 2.9 – 3.8.

Рис. 3. Картина вазоспазма в средней мозговой артерии на 6 сутки после тяжёлой черепно-мозговой травмы.
Двое больных с наиболее ранним и интенсивным развитием вазоспазма скончались. Динамика ЛСК у больного с купированным вазоспазмом и при летальном исходе представлена на графике (рис 4).
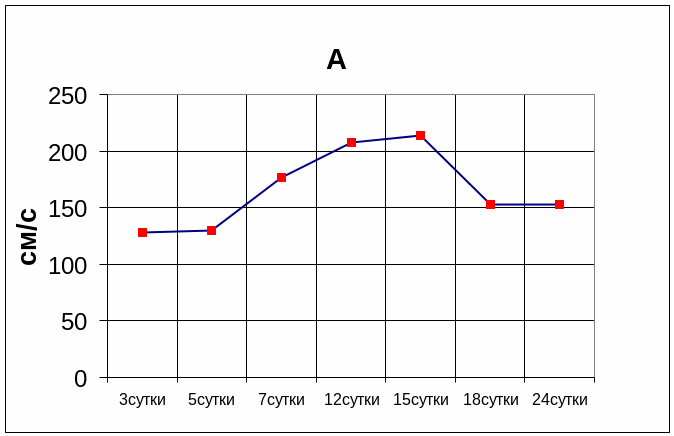
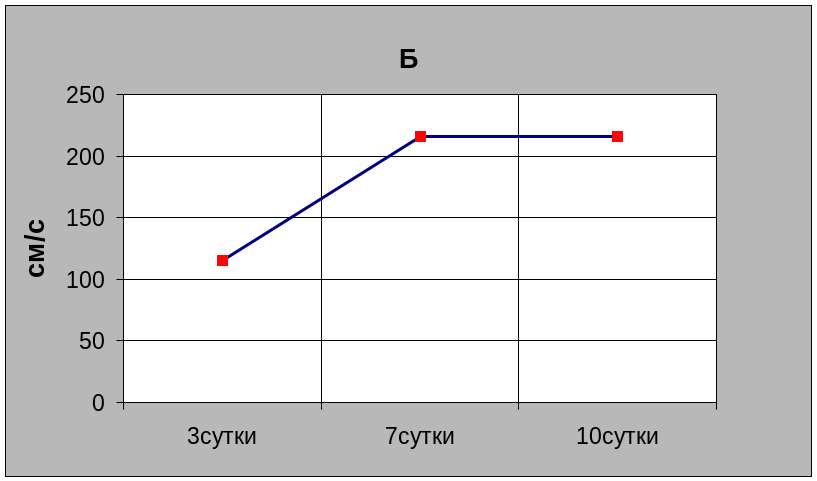
Рис. 4. Изменение значений линейной скорости кровотока в различные сроки после черепно-мозговой травмы у больных с купированным вазоспазмом (А) и при летальном исходе (Б).
У остальных больных показатели ЛСК в церебральных артериях были нормальными. Снижения ЛСК не было обнаружено ни в одном из произведенных 50 исследований, что, по-видимому, обусловлено выраженностью сопутствующей гиперемии мозга.
Снижение пульсационного индекса в раннем периоде черепно-мозговой травмы было отмечено у 4-х пациентов, а у остальных 7 индекс PI был повышен. По мере наблюдения за больными в течение месяца отмечалась отчётливая тенденция к росту этого показателя, отражающего постепенное нарастание внутричерепной гипертензии.
В отдалённом периоде после черепно-мозговой травмы нами наблюдалось 22 пациента. После перевода больных в общее отделение у части больных отмечался постепенный регресс неврологических симптомов и прояснение сознания, что сопровождалось улучшением сосудистой реактивности, нормализацией ЛСК и PI. У остальных больных на фоне стойкого угнетения сознания, порою усиливающегося, отмечалось прогрессирующее нарастание PI при одновременном диффузном снижении ЛСК с формированием резистивного паттерна кровотока. Одновременно регистрировались признаки нарушения венозного оттока (аномальный дополнительный отток по глазным и позвоночным венам, увеличение ЛСК по венам Троларда или Розенталя свыше 20 см/с, а по прямому синусу и вене Галена – свыше 30 см. Обследование, как правило, выявляло явления посттравматической гидроцефалии (рис. 5 А).
А В
 Рис.
5. А. Результаты исследования больного
с явлениями посттравматической
гидроцефалии. Компрессионная проба
свидетельствует о снижении сосудистой
реактивности (КО = 1,18). Имеются
высокорезистивные паттерны кровотока
по обеим СМА. ЛСК по прямому синусу и
вене Галена увеличены. В. У больного с
существенным регрессом общемозговых
и очаговых симптомов сосудистая
реактивность нормализовалась (КО =1,51);
регистрируется нормальный кровоток по
обеим СМА при нормализации венозного
оттока.
Рис.
5. А. Результаты исследования больного
с явлениями посттравматической
гидроцефалии. Компрессионная проба
свидетельствует о снижении сосудистой
реактивности (КО = 1,18). Имеются
высокорезистивные паттерны кровотока
по обеим СМА. ЛСК по прямому синусу и
вене Галена увеличены. В. У больного с
существенным регрессом общемозговых
и очаговых симптомов сосудистая
реактивность нормализовалась (КО =1,51);
регистрируется нормальный кровоток по
обеим СМА при нормализации венозного
оттока.
После проведения шунтирующей операции и регресса гипертензионных явлений (рис. 5. Б.) обычно наблюдалось прояснение сознания и улучшение неврологического статуса. Проведение допплеровского обследования подтверждало улучшение основных показателей мозгового кровообращения. Обычно имело место двустороннее снижение ЛСК, более выраженное на стороне преимущественно травмированного полушария наряду с умеренным увеличением показателя PI. Хорошим прогностическим признаком, сочетающимся с восстановлением утраченных функций, является восстановление нормальной сосудистой реактивности.
Таким образом, опыт работы с больными, перенесшими тяжёлую черепно-мозговую травму, показывает пользу, информативность и прогностическую ценность использованных показателей, как при остром периоде травматической болезни мозга, так и на стадиях последующей восстановительной терапии.
