
- •3 Теплообмен. Уравнение теплового баланса. Учет направлений процессов фазовых переходов при решении задач на утб. Примеры не алгоритмизированных задач.
- •5 Превращение механической энергии во внутреннюю. Явление диссипации механической энергии. Учет потерь мэ, кпд процесса.
- •7 Опыт Резерфорда. Строение атома по Резерфорду. Объяснение электризации тел на основе модели атома Резерфорда.
- •8 Сила Кулона, закон Кулона, границы применимости, напряженность электростатического поля, принцип суперпозиции.
- •9 Электростатическое поле. Силовые линии. Структура поля монополя, диполя. Применение принципа суперпозиции. Проводники и диэлектрики.
- •10 Электрический ток, сила тока, направление электрического тока, напряжение, условие существования тока в проводнике, электрическая цепь, условие существования тока в цепи.
- •11 Эл.Сопротивление проводников, Удельное сопротивление, последовательное и параллельное соединение, законы.
- •1 2 Закон Ома для участка цепи. Графическая интерпретация. Электроизмерительные приборы. Изменение пределов измерения амперметра и вольтметра с помощью шунта и добавочного сопротивления.
- •13 Работа эл. Тока, мощность эл. Тока. Закон Джоуля-Ленца.
- •Магнитное поле. Магнитное поле проводника с током, кольца с током, катушки с током. Магнитное поле Земли. Постоянные магниты.
- •Действие магнитного поля на помещенный в него проводник с током. Сила Ампера. Действие магнитного поля на движущийся в нем электрический заряд. Сила Лоренца.
1 Внутренняя энергия. Способы изменения ВЭ. Теплопередача, ее виды (примеры). Количество теплоты, физический смысл. Температура. Нагревание и охлаждение вещества с т.з. изменения ВЭ. Удельная теплоемкость вещества, физический смысл. Расчет Q в процессах с изменением температуры. Графическая интерпретация.
 При
изучении физики рассматриваются
механические, тепловые, световые,
электрические и др. явления. Известно
также, что существует два вида механической
энергии. Кинетической обладает движущееся
тело, потенциальная определяется
взаимным расположением тел или их
частей. Оба вида энергии могут переходить
один в другой. Опыт
- свинцовый шар сначала поднять над
свинцовой плитой, а потом уронить.
Происходит превращение потенциальной
энергии шара в кинетическую. После того,
как шар остановится после удара,
кинетическая и потенциальная энергии
будут равны нулю. Но это не значит, что
механическая энергия исчезла бесследно.
Она перешла в другую форму. После удара
шар и плита нагрелись и деформировались.
Следовательно, изменилась кинетическая
и потенциальная энергия частиц, из
которых состоят эти тела. Механическая
энергия перешла в энергию молекул.
При
изучении физики рассматриваются
механические, тепловые, световые,
электрические и др. явления. Известно
также, что существует два вида механической
энергии. Кинетической обладает движущееся
тело, потенциальная определяется
взаимным расположением тел или их
частей. Оба вида энергии могут переходить
один в другой. Опыт
- свинцовый шар сначала поднять над
свинцовой плитой, а потом уронить.
Происходит превращение потенциальной
энергии шара в кинетическую. После того,
как шар остановится после удара,
кинетическая и потенциальная энергии
будут равны нулю. Но это не значит, что
механическая энергия исчезла бесследно.
Она перешла в другую форму. После удара
шар и плита нагрелись и деформировались.
Следовательно, изменилась кинетическая
и потенциальная энергия частиц, из
которых состоят эти тела. Механическая
энергия перешла в энергию молекул.
Внутренняя
энергия (ВЭ)
– кинетическая энергия беспорядочного
движения молекул и потенциальная энергия
их расположения и взаимодействия
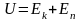
И зменение
ВЭ и передача от одного тела к другому
происходит в процессе взаимодействия
тел. 2 способа - либо ВЭ одного тела
изменяется за счет изменения энергии
упорядоченного движения другого тела
(работа, электризация, облучение,
перемагничивание), либо изменение ВЭ
при соударении движущихся молекул
соприкасающихся тел.
зменение
ВЭ и передача от одного тела к другому
происходит в процессе взаимодействия
тел. 2 способа - либо ВЭ одного тела
изменяется за счет изменения энергии
упорядоченного движения другого тела
(работа, электризация, облучение,
перемагничивание), либо изменение ВЭ
при соударении движущихся молекул
соприкасающихся тел.
 Способы
изменения ВЭ
- совершение работы или теплопередача.
Если
работа совершается над телом, его ВЭ
увеличивается (тело нагревается). Если
работа совершается самим телом, его В.Э
уменьшается (тело охлаждается).
Способы
изменения ВЭ
- совершение работы или теплопередача.
Если
работа совершается над телом, его ВЭ
увеличивается (тело нагревается). Если
работа совершается самим телом, его В.Э
уменьшается (тело охлаждается).
Опыт 1 работа над телом - эфир залили в латунную трубку, закрыли пробкой, натираем веревкой трубку. Эфир нагреется, закипит и вытолкнет пробку. Нагревание происходит при деформации.
Опыт 2 работа тела - закачиваем воздух в баллон с пробкой. После выталкивания пробки образуется туман, воздух в сосуде охлаждается.
Теплопередача – процесс изменения ВЭ тела обусловленный тепловым движением молекул без совершения работы внешней средой. Опыт – в стакан с кипятком опустим металлич.спицу. Молекулы воды передают часть кинетической энергии молекулам спицы. Вода охлаждается, спица нагревается. Виды теплопередачи -
 Теплопроводность
–
передача ВЭ от более нагретой части
тела к менее нагретой или от тела к
телу в результате теплового движения
и взаимодействия молекул. Не происходит
переноса вещества. Опыт
–
проволока на штативе, к ней воском
прикреплены гвозди. Нагреваем один
конец, гвозди отваливаются постепенно,
от огня. Скорость колебаний молекул
металла увеличивается при нагреве. Они
передают ее соседним частицам и т.д.
Следовательно - лучше в твердых телах,
хуже в жидкостях, почти нет в газах.
Самая низкая теплопроводность у вакуума.
Теплопроводность
–
передача ВЭ от более нагретой части
тела к менее нагретой или от тела к
телу в результате теплового движения
и взаимодействия молекул. Не происходит
переноса вещества. Опыт
–
проволока на штативе, к ней воском
прикреплены гвозди. Нагреваем один
конец, гвозди отваливаются постепенно,
от огня. Скорость колебаний молекул
металла увеличивается при нагреве. Они
передают ее соседним частицам и т.д.
Следовательно - лучше в твердых телах,
хуже в жидкостях, почти нет в газах.
Самая низкая теплопроводность у вакуума.

 Конвекция
–
передача ВЭ путем перемещения и
перемешивания слоев жидкого и газообразного
вещества. Естественная–
нагрев, принудительная
– нагрев с помешиванием. Опыт
– вертушка над лампочкой или свечкой.
Воздух нагревается, расширяется,
становится менее плотным, сила Архимеда
(со стороны холодного воздуха снизу
вверх) больше, чем сила тяжести, воздух
«всплывает» и вращает вертушку.
Конвекция
–
передача ВЭ путем перемещения и
перемешивания слоев жидкого и газообразного
вещества. Естественная–
нагрев, принудительная
– нагрев с помешиванием. Опыт
– вертушка над лампочкой или свечкой.
Воздух нагревается, расширяется,
становится менее плотным, сила Архимеда
(со стороны холодного воздуха снизу
вверх) больше, чем сила тяжести, воздух
«всплывает» и вращает вертушку.
 Излучение
–
передача внутренней энергии на расстоянии
с помощью электромагнитных волн. Может
происходить и в вакууме. Опыт
–
жидкостный манометр, резиновая трубка,
теплоприемник, поднесли нагретый кусок
металла, оставив воздушную прослойку.
Воздух в теплоприемнике расширился,
уровень жидкости опустился, без
соприкосновения тел. После удаления
нагретого металла жидкость вернулась
на прежний уровень.
Излучение
–
передача внутренней энергии на расстоянии
с помощью электромагнитных волн. Может
происходить и в вакууме. Опыт
–
жидкостный манометр, резиновая трубка,
теплоприемник, поднесли нагретый кусок
металла, оставив воздушную прослойку.
Воздух в теплоприемнике расширился,
уровень жидкости опустился, без
соприкосновения тел. После удаления
нагретого металла жидкость вернулась
на прежний уровень.
При теплопередаче изменяется ВЭ тела. Мерой ее изменения служит количество теплоты.
Количество
теплоты
- энергия, которую теряет или получает
тело при теплопередаче. Оно идет на
изменение ВЭ тела и на совершение телом
работы над внешней средой
 .
.
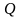 ,
сообщенное телу – положительно, отданное
телом – отрицательно.
А
положительна, если тело совершает работу
над внешней средой, отрицательна – если
над телом совершается работа. Измеряется
в Дж. или ккал,
4,2 Дж=1 ккал Дж=
,
сообщенное телу – положительно, отданное
телом – отрицательно.
А
положительна, если тело совершает работу
над внешней средой, отрицательна – если
над телом совершается работа. Измеряется
в Дж. или ккал,
4,2 Дж=1 ккал Дж=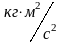 .
Физ.смысл
– чем больше масса тела, тем большее
кол-во теплоты надо затратить, чтобы
изменить его температуру на одно и то
же число градусов.
.
Физ.смысл
– чем больше масса тела, тем большее
кол-во теплоты надо затратить, чтобы
изменить его температуру на одно и то
же число градусов.
Опыт – нагрев двух сосудов с разной массой воды до одинаковой темп., или веществ одинаковой массы, но разной плотности. зависит от свойств вещества, разности температур и массы.
Как и , работа является мерой изменения внутренней энергии в процессе превращения механической энергии в теплоту.
Температура – скалярная физическая величина, характеризующая состояние термодинамического равновесия макроскопической системы (или степень нагретости тела)
Удельная
теплоемкость с
–
скалярная величина, равная количеству
теплоты, которое требуется для изменения
температуры тела массой 1 кг на 1 градус.
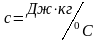 показывает,
на какую величину изменяется внутренняя
энергия 1кг вещества при нагревании или
охлаждении его на 1 градус.
показывает,
на какую величину изменяется внутренняя
энергия 1кг вещества при нагревании или
охлаждении его на 1 градус.
Общая
теплоемкость
– скалярная величина, равная количеству
теплоты, которое требуется для изменения
температуры тела на 1 градус, не зависит
от массы
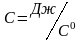
Если
суммарная кинетическая энергия молекул
изменяется, а потенциальная неизменна,
то изменение внутренней энергии или
расчет количества теплоты происходит
по формуле
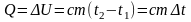 либо
либо

2 Три состояния вещества. Агрегатные превращения с т.з. строения вещества. Кристаллические и аморфные вещества. Фазовые переходы кристаллических веществ с т.з. изменения ВЭ. Удельные характеристики фазовых переходов, их физический смысл. Расчет Q в процессах фазовых переходов. Графическая интерпретация.
В зависимости от условий одно и то же вещество может находиться в различных состояниях. Эти состояния называют агрегатными. Сами молекулы вещества в различных состояниях не отличаются. Следовательно, агрегатные состояния объясняются их расположением, взаимодействием и характером движения. Газы – расстояние между молекулами велико, притяжение мало. Кинетической энергии молекул достаточно, чтобы преодолеть молекулярное притяжение, газы разлетаются (не держат ни формы, ни объема). Твердые тела и жидкости – плотность больше, молекулы ближе. Кинетической энергии недостаточно для преодоления межмолекулярного притяжения. Жидкости держат объем, твердые – и форму и объем.
Отдавая или забирая энергию, тела переводят из одного агрегатного состояния в другое. Фаза – физически однородная часть вещества, отделенная от остальных частей границей раздела. Фазовый переход – плавление, отвердевание, испарение – переход от одного агрегатного состояния в другое при строго заданной температуре.

Кристаллические вещества – это твёрдые вещества, имеющие естественную внешнюю форму правильных симметричных многогранников, в которых атомы расположены закономерно, образуя трёхмерно-периодическую пространственную укладку — кристаллическую решётку. Сохраняют форму и объем. Плавятся при определенной температуре. Многим присуще свойство анизотропии, то есть зависимость их свойств от направления.
Аморфные вещества (стекло, воск, парафин, вар) – не имеют определенной точки плавления. Размягчаются постепенно. Графики а) – плавление кристаллич. веществ, б) – плавление аморфных

Переход кристаллических веществ из твердой фазы в жидкую - плавление. Обратный процесс – кристаллизация. Точка (температура) плавления – температура, при которой тело плавится или отвердевает при постоянном давлении.
Почти все вещества при плавлении увеличивают объем и наоборот. Температура их плавления повышается при повышении давления (давление препятствует увеличению объема). Исключение – вода, чугун – у них все наоборот.
Для
плавления телу необходимо передать
некоторое количество теплоты. За счет
этого у вещества массой т
потенциальная
или кинетическая?
энергия атомов возрастает на величину
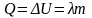
Удельная
теплота плавления
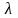 –
количество теплоты, необходимое, чтобы
кристаллическое тело 1 кг при
температуре плавления и постоянном
давлении
полностью перешло в жидкое состояние.
–
количество теплоты, необходимое, чтобы
кристаллическое тело 1 кг при
температуре плавления и постоянном
давлении
полностью перешло в жидкое состояние.
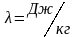
При
кристаллизации потенциальная
или
кинетическая?
энергия атомов уменьшается на ту же
величину и кол-во теплоты отводится к
окружающим телам
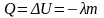 .
Кинетическая энергия атомов при этом
почти не меняется.
.
Кинетическая энергия атомов при этом
почти не меняется.
Переохлаждение – охлаждение жидкости ниже точки кристаллизации.
Из наблюдений известно, что количество жидкости, находящейся в открытом сосуде, уменьшается. Она не исчезает бесследно, а превращается в пар.
Явление превращения жидкости в пар, или переход из жидкой фазы в газообразную – парообразование. Наоборот – конденсация. Парообразование идет двумя путями – испарением и кипением.
Физика процесса - молекулы непрерывно движутся. Достаточно быстрая молекула, оказавшись на поверхности жидкости, может преодолеть притяжение соседних и вылететь из жидкости. Вылетевшие молекулы образуют над поверхностью жидкости пар. У оставшихся – изменяются скорости после соударений. Скорость испарения зависит от ряда причин.
Опыт – смачиваем бумагу эфиром и жидкостью. Эфир испарится быстрее. Следовательно, чем меньше силы притяжения между молекулами, тем быстрее испарение.
Опыт – одинаковый объем воды налили в блюдце и в кувшин с узким горлом. В блюдце вода испарится быстрее. Следовательно, скорость испарения зависит от площади поверхности.
Поскольку в жидкости всегда есть движущиеся молекулы, то испарение происходит при любой температуре. Но быстрее оно происходит при высокой температуре. Итак,
Испарение – парообразование с поверхности при любой температуре. Зависит от S поверхности, температуры, рода жидкости и внешнего давления. При испарении внутренняя энергия жидкости уменьшается, так как наиболее быстрые молекулы вылетают, а скорость оставшихся ниже. Температура оставшейся жидкости уменьшается.
 Одновременно
с испарением происходит обратный процесс
– беспорядочно двигаясь над поверхностью
жидкости, некоторые молекулы возвращаются
в нее. Если испарение идет в закрытом
сосуде, то сначала вылетевших молекул
будет больше, чем вернувшихся. Плотность
пара будет увеличиваться. С увеличением
плотности папа будет увеличиваться и
число молекул, вернувшихся обратно в
жидкость. Наступает динамическое
равновесие
– число молекул, вылетающих из жидкости,
равно числу возвращающихся в нее. Пар,
находящийся в динамическом равновесии
со своей жидкостью, называется насыщенным
(и наоборот).
При динамическом равновесии в закрытом
сосуде масса жидкости не уменьшается,
а в открытом – уменьшается, так как
часть молекул пара рассеивается в
воздухе и не возвращается обратно.
Одновременно
с испарением происходит обратный процесс
– беспорядочно двигаясь над поверхностью
жидкости, некоторые молекулы возвращаются
в нее. Если испарение идет в закрытом
сосуде, то сначала вылетевших молекул
будет больше, чем вернувшихся. Плотность
пара будет увеличиваться. С увеличением
плотности папа будет увеличиваться и
число молекул, вернувшихся обратно в
жидкость. Наступает динамическое
равновесие
– число молекул, вылетающих из жидкости,
равно числу возвращающихся в нее. Пар,
находящийся в динамическом равновесии
со своей жидкостью, называется насыщенным
(и наоборот).
При динамическом равновесии в закрытом
сосуде масса жидкости не уменьшается,
а в открытом – уменьшается, так как
часть молекул пара рассеивается в
воздухе и не возвращается обратно.
Так как одновременно с испарением часть молекул возвращается обратно, то это явление называют конденсацией (превращение пара в жидкость). Конденсация пара сопровождается выделением энергии.
Опыт – из нагретой колбы пар соприкасается с холодным стеклом и конденсируется. При этом выделяется энергия. Точные опыты показывают, что при конденсации пара выделяется столько же энергии, сколько пошло на его образование.

 Кипение
–
парообразование по всему объему и с
поверхности при определенной температуре.
В жидкости при нагреве образуются
пузырьки растворенного воздуха с парами
жидкости внутри. Под действием
выталкивающей силы пузырьки поднимаются
и частично конденсируются в верхних
холодных слоях. При прогреве всей
жидкости пузырьки достигают поверхности,
давление в них становится атмосферными
пар из пузырьков выходит наружу.
Каждое
вещество кипит при определенной
температуре.
Кипение
–
парообразование по всему объему и с
поверхности при определенной температуре.
В жидкости при нагреве образуются
пузырьки растворенного воздуха с парами
жидкости внутри. Под действием
выталкивающей силы пузырьки поднимаются
и частично конденсируются в верхних
холодных слоях. При прогреве всей
жидкости пузырьки достигают поверхности,
давление в них становится атмосферными
пар из пузырьков выходит наружу.
Каждое
вещество кипит при определенной
температуре.
Температура
(точка) кипения
– температура, при которой жидкость
кипит при постоянном давлении (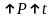 и наоборот).
и наоборот).
При
парообразовании за счет подводимой
теплоты потенциальная энергия молекул
вещества массой т
возрастает
на

Удельная
теплота парообразования
L
–количество теплоты, необходимое для
превращения единицы массы жидкости в
пар при температуре кипения.
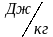
L уменьшается с повышением температуры испаряющейся жидкости.
При
конденсации потенциальная энергия
молекул уменьшается на величину
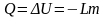 и соответственное количество теплоты
отводится окружающим телам.
и соответственное количество теплоты
отводится окружающим телам.
3 Теплообмен. Уравнение теплового баланса. Учет направлений процессов фазовых переходов при решении задач на утб. Примеры не алгоритмизированных задач.
Теплообмен - самопроизвольный необратимый процесс переноса теплоты от более нагретых тел (или участков тел) к менее нагретым (в общем случае перенос теплоты может вызываться также неоднородностью полей др.физических величин, напр., разностью концентраций - т. н. диффузионный термоэффект). Различают теплообмен теплопроводностью, конвективный и радиационный (излучением).
Теплопроводность – передача ВЭ от более нагретой части тела к менее нагретой или от тела к телу в результате теплового движения и взаимодействия молекул. Не происходит переноса вещества. Опыт – проволока на штативе, к ней воском прикреплены гвозди. Нагреваем один конец, гвозди отваливаются постепенно, от огня. Скорость колебаний молекул металла увеличивается при нагреве. Они передают ее соседним частицам и т.д. Следовательно - лучше в твердых телах, хуже в жидкостях, почти нет в газах. Самая низкая теплопроводность у вакуума.
Конвекция – передача ВЭ путем перемещения и перемешивания слоев жидкого и газообразного вещества. Естественная– нагрев, принудительная – нагрев с помешиванием. Опыт – вертушка над лампочкой или свечкой. Воздух нагревается, расширяется, становится менее плотным, сила Архимеда (со стороны холодного воздуха снизу вверх) больше, чем сила тяжести, воздух «всплывает» и вращает вертушку.
Излучение – передача внутренней энергии на расстоянии с помощью электромагнитных волн. Может происходить и в вакууме. Опыт – жидкостный манометр, резиновая трубка, теплоприемник, поднесли нагретый кусок металла, оставив воздушную прослойку. Воздух в теплоприемнике расширился, уровень жидкости опустился, без соприкосновения тел. После удаления нагретого металла жидкость вернулась на прежний уровень.
При теплопередаче изменяется ВЭ тела. Мерой ее изменения служит количество теплоты.
Количество теплоты - энергия, которую теряет или получает тело при теплопередаче. Оно идет на изменение ВЭ тела и на совершение телом работы над внешней средой . , сообщенное телу – положительно, отданное телом – отрицательно. А положительна, если тело совершает работу над внешней средой, отрицательна – если над телом совершается работа. Измеряется в Дж. или ккал,
Уравнение теплового баланса – в замкнутой системе, внутренняя энергия не изменяется, над системой работа не совершается. Внутри системы в процессе теплообмена одни тела нагреваются, другие охлаждаются, но суммарное количество теплоты, полученное системой, равно нулю. Q1+Q2+Q3+….=0
Отдавая или забирая энергию, тела переводят из одного агрегатного состояния в другое. Фаза – физически однородная часть вещества, отделенная от остальных частей границей раздела
Фазовый переход — переход вещества из одной термодинамической фазы в другую при изменении внешних условий. Любая смена агрегатного состояния вещества есть фазовый переход.
Наиболее часто рассматриваются фазовые переходы при изменении температуры, но при постоянном давлении. Именно поэтому часто употребляют термины «точка» (а не линия) фазового перехода, температура плавления и т. д.
Наиболее распространённые примеры фазовых переходов первого рода:
плавление и кристаллизация
испарение и конденсация
Наиболее распространённые примеры фазовых переходов второго рода:
прохождение системы через критическую точку
переход парамагнетик-ферромагнетик или парамагнетик-антиферромагнетик (параметр порядка — намагниченность)
переход металлов и сплавов в состояние сверхпроводимости
переход аморфных материалов в стеклообразное состояние
Под скачкообразным изменением свойств вещества имеется в виду скачок при изменении температуры и давления. В реальности же, воздействуя на систему, мы изменяем не эти величины, а её полную внутреннюю энергию.
Учет фазовых переходов - отдает или забирает энергию тело при переходе из одной фазы в другую.
Кристаллизация – отдает тепло, скорость молекул уменьшается, внутренняя энергия уменьшается.
Плавление – забирает тепло, скорость молекул увеличивается, как и расстояние между ними, внутренняя энергия увеличивается.
Аналогично с испарением – самые подвижные молекулы вылетают из жидкости, средняя скорость оставшихся ниже, внутренняя энергия уменьшается.
При конденсации – внутренняя энергия пара уменьшается.
Пример задачи с разными вариантами решения
В
калориметр налито 2 кг воды, имеющей
температуру 5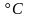 ,
и положен кусок льда массой 5 кг, имеющий
температуру -40
.
Определить температуру
,
и положен кусок льда массой 5 кг, имеющий
температуру -40
.
Определить температуру
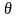 и объем содержимого калориметра после
установления теплового равновесия.
Теплоемкостью калориметра и теплообменом
с внешней средой пренебречь.
и объем содержимого калориметра после
установления теплового равновесия.
Теплоемкостью калориметра и теплообменом
с внешней средой пренебречь.
Дано:
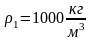 ,
,
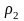 = 920
= 920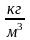 ,
C1
= 4,2
,
C1
= 4,2
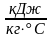 ,
C2
= 2,1
,
= 330
,
C2
= 2,1
,
= 330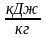 ,
,
m1
= 2 кг,
 ,
m2
= 5 кг,
,
m2
= 5 кг,
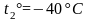 .
.
Найти:
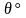 ,
V.
,
V.
Анализ:
Можно представить себе следующие случаи:
Весь лед растает, и температура смеси будет больше нуля.
Вся вода замерзнет, и температура смеси будет меньше нуля.
Температура смеси будет равна нулю, и часть льда растает.
Температура смеси будет равна нулю, и часть воды замерзнет.
Для того, чтобы понять, какой случай реализуется в данной задаче, необходимо сделать предварительные вычисления.
При
охлаждении до
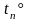 = 0
вода отдает количество теплоты
= 0
вода отдает количество теплоты
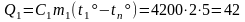 кДж.
кДж.
При нагревании льда до температуры плавления лед поглощает количество теплоты
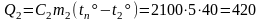 кДж.
кДж.
Если весь лед растает, он поглощает количество теплоты
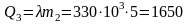 кДж.
кДж.
Если вся вода замерзнет, она отдаст количество теплоты
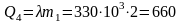 кДж.
кДж.
Так как Q2 > Q1, то лед не может таять, и могут осуществиться случаи 2 или 4. Для осуществления случая 2 необходимо, чтобы Q1 + Q4 < Q2
Q1 + Q4 = 702 кДж, Q2 = 420 кДж.
Соответственно
реализуется случай 4: температура смеси
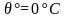 и часть воды замерзнет. Обозначим массу
замерзшей воды m3,
и составим уравнение теплового баланса:
и часть воды замерзнет. Обозначим массу
замерзшей воды m3,
и составим уравнение теплового баланса:

 -
количество теплоты, которое отдает
вода, остывая до 0
-
количество теплоты, которое отдает
вода, остывая до 0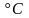 .
.
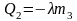 -
количество теплоты, которое отдает
замерзающая вода.
-
количество теплоты, которое отдает
замерзающая вода.
 -
количество теплоты, полученное льдом
при нагревании до 0
.
-
количество теплоты, полученное льдом
при нагревании до 0
.
Отсюда
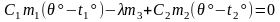
Из этого выражения находим массу замерзшей воды
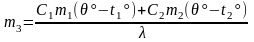
После
установления теплового равновесия,
масса воды
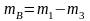 ,
и масса льда будет
,
и масса льда будет
 .
Объем полученной смеси
.
Объем полученной смеси
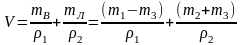
4 Энергия топлива. Удельная теплота сгорания топлива, физический смысл. Превращение ВЭ в механическую. Тепловые двигатели. Паровой двигатель, ДВС, паровая турбина - устройство и принцип действия. КПД тепловых двигателей.
В процессе химического соединения ряда веществ перестраивается структура молекул, в результате резко увеличивается их кинетическая энергия. Такие процессы называют процессами горения, а вещества – топливо и окислитель.
Например, вода Н2О – для разделения на атомы надо совершить работу и затратить энергию. При горении происходит соединение атомов в молекулы и энергия выделяется. Так атомы углерода, содержащиеся в топливе, при горении соединяются с двумя атомами кислорода и выделяется энергия.
При
полном сгорании топлива массой т
внутренняя энергия теплового движения
молекул возрастает на величину
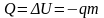
Удельная
теплота сгорания топлива
 –
скалярная физическая величина, равная
количеству теплоты, которое выделяется
при полном сгорании 1 кг топлива при
данном окислителе.
–
скалярная физическая величина, равная
количеству теплоты, которое выделяется
при полном сгорании 1 кг топлива при
данном окислителе.
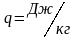
Явления перехода энергии в механических процессах рассматривались ранее.
Энергия движения переходит в потенциальную взаимодействия и обратно. При этом полная механическая энергия остается неизменной, если действуют только силы упругости и тяготения и отсутствуют силы трения.
При падении свинцового шара на доску с деформацией и нагреванием мы видели переход механической энергии во внутреннюю. След., механическая и внутренняя энергии могут переходить от одного тела к другому. При теплопередаче – более нагретое тело отдает, а холодное – получает энергию, внутренняя энергия топлива превращается в энергию движения. При переходе энергии от одного тела к другому или при превращении энергии из одного вида в другой энергия сохраняется.
Закон сохранения и превращения энергии – во всех явлениях в природе энергия не возникает и не исчезает. Она превращается из одного вида в другой с сохранением значения. Энергия солнечных лучей переходит во ВЭ почвы и микроорганизмов, нагретые воздушные массы двигаются и появляется ветер и т.д.
Тепловые двигатели – машины, превращающие внутреннюю энергию топлива в механическую энергию (или работу).Общая структура – нагреватель, рабочее тело, холодильник (атмосфера) Опыт – в пробирке с пробкой вскипятили воду – пробка вылетела. При замене пробирки на цилиндр, а пробки – на поршень получим простейший двигатель Джеймса Уатта.
Паровой двигатель — тепловой двигатель внешнего сгорания, преобразующий энергию нагретого пара в механическую работу возвратно-поступательного движения поршня, а затем во вращательное движение вала.
После
этого расширенный пар может выпускаться
в атмосферу или поступать в конденсатор
. Полный цикл двигателя занимает один
полный оборот и состоит из четырёх фаз
- впуска, расширения (рабочая фаза),
выпуска и сжатия
В
машинах одиночного действия поршень
перемещался в одну сторону силой
расширяющегося пара, обратно - под
действием гравитации, или за счёт момента
и нерции
вращающегося маховика. В паровых
машинах двойного действия свежий пар
поочередно подается в обе стороны
рабочего цилиндра, в то время как
отработанный пар с другой стороны
цилиндра выходит в атмосферу или в
конденсатор.
нерции
вращающегося маховика. В паровых
машинах двойного действия свежий пар
поочередно подается в обе стороны
рабочего цилиндра, в то время как
отработанный пар с другой стороны
цилиндра выходит в атмосферу или в
конденсатор.
1 — Поршень, 3 — Ползун 4 — Шатун
5 — Коленчатый вал
6 — Эксцентрик для привода клапана
7 —маховик
8 — Золотник
—маховик
8 — Золотник
Двигатель внутреннего сгорания - топливо сгорает внутри, в цилиндре. Состоит – цилиндр, поршень 3, шатун 4, вал 5, клапан 1 для горючего, клапан 2 для выпуска газов, свеча 6. Рабочий цикл за 4 хода – четырехтактный, впуск, сжатие, рабочий ход, выпуск. один ход поршня- полоборота вала.
1 такт поршень вниз, объем над ним увеличивается, в цилиндре разрежение, клапан 1 открывается, в цилиндр входит горючая смесь, клапан 1 закрывается.
2 такт вал поворачивается, поршень вверх, сжимает смесь. Смесь загорается от искры и образует газы, когда поршень в крайнем верхнем положении.
3 такт (рабочий ход) – газы давят на поршень, толкают его вниз. При этом двигатель совершает работу. Движение передается шатуну и далее коленчатому валу с маховиком. После толчка маховик по инерции перемещает поршень вверх. Сжатые газы открывают клапан 2 и выходят наружу.
4 такт – выпуск продуктов сгорания через клапан 2, газы вышли, поршень опускается, клапан 2 закрывается, клапан 1 открывается.


 Паровая
турбина
– тип двигателя, в котором пар или
нагретый газ вращает вал двигателя без
помощи поршня, шатуна и коленчатого
вала. Состоит
–
на вал 5 насажен диск 4, по ободу которого
закреплены лопатки 2. Около лопаток
расположены сопла1, в которые поступает
пар 3 из котла. Струи пара оказывают
давление на лопатки и вращают диск
турбины. В современных – несколько
дисков с лопатками на общем вале.
Паровая
турбина
– тип двигателя, в котором пар или
нагретый газ вращает вал двигателя без
помощи поршня, шатуна и коленчатого
вала. Состоит
–
на вал 5 насажен диск 4, по ободу которого
закреплены лопатки 2. Около лопаток
расположены сопла1, в которые поступает
пар 3 из котла. Струи пара оказывают
давление на лопатки и вращают диск
турбины. В современных – несколько
дисков с лопатками на общем вале.
Любой тепловой двигатель превращает в механическую только часть энергии топлива. Рабочее тело при нагреве передает часть энергии атмосфере вместе с паром или выхлопными газами. Для характеристики экономичности двигателей ввели КПД.
КПД
тепловых двигателей
– отношение полезной работы двигателя
к энергии, полученной от нагревателя.

