
1. Амінокислоти
Різні пептиди і білки складаються із залишків α-амінокислот. Загальне число амінокислот, що зустрічаються в природі, досягає 300, проте деякі з них виявлені лише в певному співтоваристві або навіть в одному організмі.
Серед них виділяється група з 20 найбільш важливих α-амінокислот, що постійно зустрічаються у всіх білках (таблиця. 1.1). Одна з них не містить первинної аміногрупи і є, таким чином, α-імінокислотою. Ця амінокислота - пролін. Саме ці 20 амінокислот беруть участь у біосинтезі білка і мають свій шифр.
Амінокислоти - це похідні карбонових кислот, в яких один або декілька атомів водню заміщені на аміногрупу.
Походять амінокислоти лише від деяких органічних кислот: оцтової, пропіонової, масляної, валеріанової, капронової та двох дикарбонових – янтарної і глутарової.
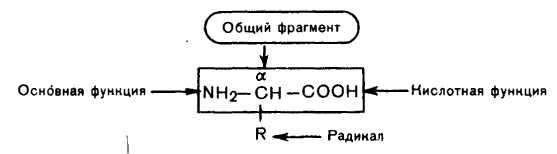
α-Амінокислоти — гетерофункціональні сполуки. Вони обов'язково містять карбоксильну групу і аміногрупу, що знаходяться у одного і того ж атома вуглецю в -положенні.
Більшість амінокислот, що входять до складу білка мають одну аміногрупу, лише лізин та аргінін – по дві. Друга аміногрупа в таких амінокислотах стоїть у кінці молекули.
У твердому стані і водних розчинах при нейтральних значеннях рН α-амінокислоти існують переважно у вигляді внутрішніх солей (диполярних іонів, див. 1.3).
Назви α-амінокислот будуються за замісною номенклатурою, але зазвичай використовуються їх тривіальні назви.

Тривіальні назви α-амінокислот часто пов'язані з джерелами їх виділення:
серин входить до складу фіброїну шовку (від латів. serieus — шовковистий);
тирозин вперше виділений з сиру (від греч. tyros — сир);
глутамін — із злакової клейковини (від латів. gluten — клей);
цистин — з каменів сечового міхура (від греч. kystys — міхур);
аспарагінова кислота — з паростків спаржі (від латів. asparagus — спаржа).
Основним джерелом α-амінокислот для живого організму є харчові білки. Багато α-амінокислот синтезуються в організмі, деякі ж необхідні для синтезу білків α-амінокислоти не синтезуються в організмі і повинні поступати ззовні. Такі амінокислоти називають незамінними: валін, лейцин, ізолейцин, лізин, треонін, метіонін, фенілаланін, триптофан (див. табл. 1.1).
При деяких, найчастіше вроджених, захворюваннях перелік незамінних кислот розширюється. Наприклад, при фенілкетонурії людський організм не синтезує ще одну α-амінокислоту — тирозин, який в організмі здорових людей утворюється при гідроксилюванні фенілаланіну. Для деяких організмів (щури, миші) необхідно 9 незамінних амінокислот (до названих додається гістидин).
Напівнезамінні амінокислоти – синтезуються в недостатній кількості, тому повинні частково поступати в організм з їжею. Для організму людини такими амінокислотами є аргінін, тирозин, гістидин.
Замінні амінокислоти синтезуються в організмі з цілого ряду органічних сполук.
1.1. Класифікація α-амінокислот.
α-Амінокислоти класифікують декількома способами залежно від ознаки, покладеної в основу їх поділу на групи.
Однією з класифікаційних ознак є хімічна природа радикала R. За цією ознакою α-амінокислоти діляться на аліфатичні, ароматичні і гетероциклічні (табл. 1.1).
Таблиця 1.1. Найважливіші α-амінокислоти


1 Для запису амінокислотних залишків в макромолекулах пептидів і білків використовують трьохбуквені (іноді однобуквені) скорочення їх тривіальних назв.
2 Незамінні α-амінокислоти.
І. Аліфатичні α-амінокислоти
Аліфатичні (або ациклічні) α-амінокислоти складають найбільш численну групу. Всередині цієї групи їх підрозділяють із залученням додаткових класифікаційних ознак. Наприклад, залежно від числа карбоксильних груп і аміногруп в молекулі виділяють:
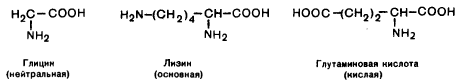
нейтральні (моноаміномонокарбонові) амінокислоти (одна NH2- і одна СООН-групи)
лужні (диамінодикарбонові) амінокислоти (дві NH2- і одна СООН-групи)
кислі (моноамінодикарбонові)амінокислоти (одна NH2- і дві СООН-групи).

У аліфатичному радикалі можуть міститися «додаткові» функціональні групи, наприклад:
гідроксильна (серін, треонін),
карбоксильна (аспарагінова і глутамінова кислоти),
тіольна (цистеїн),
амідна (аспарагін, глутамін) групи.
1.1. Моноаміномонокарбонові (нейтральні) амінокислоти містять органічні радикали, не здатні ні приймати, ні віддавати протон.
1). Гліцин (Gly) – проста і єдина оптично неактивна амінокислота цієї групи.
NH2
– CН2
– СООН гліцин
(ГЛІ)
Очевидно, ця амінокислота не проявляє особливо цікавих хімічних властивостей, а її біологічне значення зводиться до ролі структурного елементу в тих випадках, коли важливо розташувати структуру в невеликому об'ємі (компактно). Структурні білки (колаген, шовк, шерсть) містять значні кількості гліцину.
2). Аланін (Ala) було вперше виділено у 1881 р. із фіброїну шовку.

3). Валін (Val) вперше виділений з білків підшлункової залози у 1879 р.

4). Лейцин (Leu) міститься у пророслому зерні у помітній кількості; є джерелом утворення сивушних масел при спиртовому бродінні.
Лейцин погано розчиняється в холодній воді, легко з неї кристалізується у вигляді характерних перламутрових пластинок та листочків.

5). Ізолейцин (Ilе) відкрито у 1904 р. і виділено з меляси. Є джерелом утворення сивушних масел при бродінні.

До нейтральних гідроксилмістких оксиамінокислот відносять:
6). Серин (Ser) також було виділено із фіброїну шовку у 1856 р.

Оксиметильна група (рКа ≈ 15) не дисоціює за звичайних фізіологічних умов. Проте серин відіграє важливу роль у ряді біохімічних реакцій завдяки здатності своєї первинної гідроксильної групи виступати за певних умов в ролі нуклеофілу.
7). Треонін (Thr)

Наскільки відомо, вторинна (спиртова) гідроксильна група треоніну не бере участь ні в одній біохімічній реакції.
До нейтральних сірковмісних амінокислот відносять:
8). Цистеїн (Cys).

Заміна атома кисню у серині на атом сірки обумовлює дисоціацію протона, в результаті утворюється амінокислота цистеїн.
Відіграє важливу роль в обміні речовин як джерело сірки та як відновлюючий агент.
Крім того, сульфгідрильна група цистеїну легко окислюється з утворенням дисульфіду - цистіну.
9). Метіонін (Met) Метіонін відіграє в організмі важливу роль як джерело (донор) метильних груп. Широко використовується у тваринництві для підвищення продуктивності.

1.2. Диаміномонокарбонові (лужні) амінокислоти можна відрізнити, наприклад, за їх здатністю утворювати осади з певними кислотами. До цієї групи входять:
10). Лізин (Lys)
Можна припустити, що чотири метиленові групи додають рухливість аміногрупі в білковій молекулі.

11). Аргінін (Arg)
Гуанідинова група цієї амінокислоти додає їй сильно лужні властивості. Дійсно, гуанідин - один з найсильніших відомих органічних основ, він порівнянний за силою з гідроксидом натрію.

Сильнолужні властивості гуанідинової групи пояснюються тим, що приєднання протонів (протонування) до іміногрупи (>C=NH) призводить до утворення більш стабільного катіону, ніж протонування первинної аміногрупи.
Отже, за фізіологічних умов (рН 7,35) ця група завжди іонізована. Дуже ймовірно, що її присутність в амінокислотах обумовлена здатністю специфічно взаємодіяти з фосфатними групами.

1.3. Моноамінодикарбонові (кислі) амінокислоти можна визначити, наприклад, за здатностю утворювати в спирті нерозчинні кальцієві або барієві солі.
Бічні групи таких амінокислот несуть карбоксильну групу, що обумовлює кислі властивості. До таких амінокислот відносять дві:
12). Аспарагінова кислота (Asp)

13). Глутамінова кислота (Glu)

При утворенні первинних амідов аспарагінової і глутамінової кислот утворюються дві нейтральні амінокислоти:
14). Аспарагин (Asn)

15). Глутамін (Gin)

Перетворення карбоксильної групи на амідну дозволяє цим амінокислотам брати участь в утворенні водневого зв'язку, що важливе для виконання біологічних функцій.
ІІ. Циклічні (ароматичні і гетероциклічні) α-амінокислоти
Ароматичні і гетероциклічні α-амінокислоти побудовані таким чином, що бензольні і гетероциклічні кільця в них відокремлені від загального α-амінокислотного фрагменту метиленовою групою –СН2–.

Розділяюча метиленова ланка відіграє важливу роль при формуванні просторової структури білкової макромолекули, до складу якої входять ароматичні або гетероциклічні α-амінокислоти. За рахунок метиленової групи розширюється можливість обертання плоских циклічних систем і таким чином зменшуються ускладнення в їх просторовому розміщенні.
Ароматичні і гетероциклічні α-амінокислоти можна розглядати як β-заміщені похідні аланину.
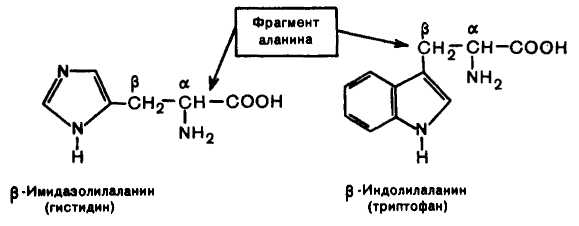

Циклічні амінокислоти поділяються на:
