
- •Общие замечания к проведению практикума
- •III. Техника безопасности
- •Лабораторная работа №1
- •Краткое теоретическое введение
- •Порядок выполнения работы
- •I.По ниже приведенным методикам нужно получить следующие лиофобные золи:
- •1.Получение золя серы в воде методом замены растворителя
- •2. Получение золя методом восстановления.(пока не делаем)
- •3. Получение золей реакцией двойного обмена
- •4. Получение золя берлинской лазури пептизацией пасты
- •5) Получение золя жедезисто-синеродистой меди реакцией обмена
- •II. По ниже приведенным методикам нужно получить следующие лиофильные золи:
- •III. Определение конуса Тиндаля.
- •Обработка результатов измерений
- •Опыт 3. Зависимость устойчивости эмульсии от концентрации эмульгатора.
- •Экспериментальная часть
- •Опыт 1. Зависимость времени жизни пены от концентрации пенообразователя
- •Набухание эластичных гелей
- •Контракция набухания эластичных гелей
- •Теплота набухания эластичных гелей
- •Влияние рН среды на набухание гелей
- •Влияние электролитов на набухание гелей
- •Порядок выполнения работы
- •Лабораторная работа № 6.
- •Порядок выполнения работы
- •Краткое теоретическое введение Адсорбция пав из растворов на твердом адсорбенте.
- •Реактивы, посуда и оборудование
- •Порядок выполнения работы
- •Часть 1
- •Часть 2
- •Обработка результатов измерений и содержание отчета
- •Часть 1
- •Определение концентрации растворов уксусной кислоты до и после адсорбции
- •Экспериментальные результаты адсорбции уксусной кислоты на угле
- •Значения адсорбции, рассчитанные различными методами
- •Часть 2.
- •Контрольные вопросы
Экспериментальная часть
Цель работы: 1. Получить пену методом взбалтывания.
2. Изучить влияние различных факторов на стабильность пен.
Оборудование и реактивы: мерный цилиндр на 250 мл с притертой пробкой, секундомер, дистиллированная вода, пенообразователь (мыла, синтетические моющие вещества, горчица, порошок мыльного корня, солодового ростка и т. д.), стабилизатор (золи Fe(OH)3, Аl(ОН)3, K2SO4, КJ, К3РO4).
Опыт 1. Зависимость времени жизни пены от концентрации пенообразователя
В чистый измерительный цилиндр наливают 100 мл дистиллированной воды и вносят навеску пенообразователя в количестве 1 г. Для сравнительной характеристики пенообразователей следует использовать их по группам: хозяйственные мыла, туалетные, жидкие и твердые CMC, растворы ПАВ.
После этого цилиндр крепко закрывают пробкой и содержимое цилиндра взбалтывают (энергично) одну минуту, при этом цилиндр держат в вертикальном положении. Затем цилиндр ставят на стол, пробку открывают и измеряют время, за которое разрушается половина столба пены. Это и есть время жизни пены (t, с).
Разбавляют исходный раствор в два раза дистиллированной водой и вновь определяют время жизни пены, объем жидкости оставляют всегда 100 мл. Производят 7–8 разбавлений, данные опыта записывают в виде таблицы и строят график, откладывая на оси ординат время жизни пены t, а по оси абсцисс – концентрацию пенообразователя (г/л).
Опыт 2. Зависимость времени жизни пены от температуры пенообразующей жидкости
Для опыта используют слив одного из разбавлений жидкости из предыдущего эксперимента и изучают время жизни пены этой жидкости при температуре 20, 30, 40, 50, 60, 70 °С.
По данным эксперимента строят график, откладывая на оси ординат время жизни пены, а по оси абсцисс – температуру.
Опыт 3. Зависимость времени жизни пен от природы стабилизатора
К 100 мл пенной жидкости прибавляют 0,1 г порошка:
1) сульфатов магния, алюминия, железа;
2) сульфатов кобальта, никеля. Изучают время жизни пены и формулируют выводы.
Опыт 4. Зависимость времени жизни пены от природы пеногасителя
К 100 мл пенной жидкости добавляют по 0,1 мл различных органических веществ: этилового спирта, диэтилового эфира, изоамилового спирта, силиконового масла и т. д.
Определяют время жизни пен и формулируют выводы.
Контрольные вопросы
1. Как получить пену? Строение пен.
2. Перечислить факторы устойчивости пен.
3. Как изменяется устойчивость пленки пены от концентрации пенообразователя?
4. Перечислите основные положения теории устойчивости пен.
5. Расскажите о применении пен в быту и технике.
6. Поясните роль стабилизатора пены.
7. Как зависит время жизни пены от природы пеногасителя?
8. Какую роль играет пена при стирке и флотации?
Лабораторная работа № 4
Исследование кинетики ограниченного набухания полимеров
Цель работы: Исследовать кинетику набухания желатина в воде и определить константу скорости набухания.
Краткое теоретическое введение
Гель представляет собой систему, состоящую из двух фаз: одна образует пространственную сетку, которая придает гелю свойства твердого тела; другая – жидкую фазу, заполняющую все промежутки пространственной сетки. Эта заполняющая жидкость чаще всего является раствором вещества, составляющего сетку геля.
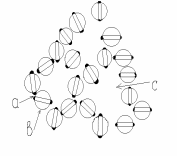
Рис. 10. Сетчатая структура студня
a – лиофобные участки;
b – сольватная оболочка;
c – дисперсионная среда
В зависимости от характера пространственной сетки гели разделяются на эластичные (набухающие) и неэластичные, хрупкие (ненабухающие) гели. Неэластичные гели (уголь, силикагель, пемза, цемент) способны впитывать в себя любую жидкость и не набухать, не изменяться в объеме. Впитываемая жидкость заполняет свободные капилляры (поры), суммарный объем которых может составлять от 30 до 60 % общего объема геля. Рабинович указывает, что для определения радиусов пор в неэластичных гелях может быть применено уравнение Томсона:
R = 4,79 · 10–8 · lg ρ1/ρ0,
где ρ1 – давление водяного пара над капилляром радиуса;
ρ0 – давление водяного пара над плоской поверхностью воды.
Однако надо учесть, что пористые вещества и, в частности, гели обладают порами различной величины от 10–2 до 10–7 см. Сложная поверхность геля обладает большой адсорбционной способностью, что объясняется значительной величиной ее удельной поверхности (Sуд, см2), для характеристики которой приводятся некоторые данные в табл. 13.
Таблица 5
Вещество |
Sуд, см2 |
Животный уголь Активированный уголь Желатин Силикагель |
2 · 107
1 · 107
1 · 107
0,5 · 107 |
