- •Курс Лекций «Современные проблемы органической химии»
- •Защита гидроксильной группы
- •Сложные эфиры
- •Силиловые эфиры
- •Триметилсилиловые эфиры tms
- •Триэтилсилиловые эфиры tes
- •Третбутилдиметилсилиловые эфиры tbs
- •Третбутилдифенилсилиловые эфиры tbdps
- •Триизопропилсилиловые эфиры tips I-Pr3Si
- •Защитные группы для азота
- •Защиты карбосильных групп.
- •Метиловые эфиры.
- •Трет-бутиловые эфиры.
- •Аллиловые эфиры
- •Силиловые эфиры
Курс Лекций «Современные проблемы органической химии»
Часто требуется в процессе синтеза защита и активация функциональных групп.
В процессе органического синтеза с использованием полифункциональных соединений очень часто возникает проблема защиты одной из них с целью сохранить в процессе превращений. Затем после проведения ряда последовательных превращений уже в конечном продукте снять эту защиту – регенерировать функциональную группу и использовать ее в дальнейших превращениях.
Эти защитные группы должны удовлетворять следующим условиям:
Быть дешевыми и легко доступными
Должны легко и эффективно вводиться
Должны легко характеризоваться и избегать таких сложностей как создание новых стереогенных центров.
Должны быть стабильными в реакционных условиях и при обработке
Должны быть устойчивы в условиях разделения, очистки и хроматографирования
Должны легко удаляться селективно и полностью при весьма специфических условиях.
Побочные продукты снятия защитных групп должны легко отделяться от субстрата
Чаще всего в процессе синтеза приходится защищать гидроксильную, диольную, карбоксильную и аминную группы – т.е. наиболее важные группировки природных веществ и их синтетических аналогов. Эти группировки или их производные наиболее часто встречаются в лекарственных соединениях.
При этом каждая из защитных групп должна отщепляться такими реагентами и в таких условиях, в которых не затрагивались бы другие защитные группы.
Давайте вначале рассмотрим способы удаления и отщепления защитных групп.
Самый простой способ это основной сольволиз.
Ацильная защита широко используется для защиты SH, OH и аминогрупп. Ацильная защита легко снимается в условиях щелочного гидролиза. Эфиры тиолов очень чувствительны к нуклеофильной атаке, поэтому для защиты используются ацетаты, бензоаты и пивалаты. Ацетаты и бензоаты особенно ценимы, т.к. легко отделяются K2CO3 или NH3 в MeOH. Стерические препятствия ацильного радикала важны как и электронные эффекты в α положении к карбонилу. Пивалаты из-за стерических препятствий значительно медленнее могут быть удалены селективно. Трифторацетаты очень легко гидролизуются при pH 7.
Влияние электронных эффектов заместителей демонстрирует следующий ряд:
|
ацетат |
хлорацетат |
дихлорацетат |
трихлорацетат |
Vотн |
1 |
700 |
16 000 |
100 000 |
Конечно, когда имеем дело с защищенными сложноэфирными группами полифункциональными соединениями здесь могут возникать проблемы внутримолекулярной переэтерификации, связанной с миграцией ацильных групп на соседние спиртовые. Эта проблема более существенна для бензоатов, чем для ацетатов.
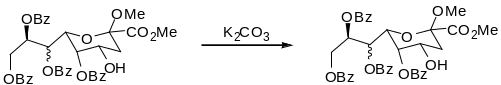
Амиды. Трифторацетамиды очень лабильны и легко удаляются с K2CO3 в MeOH – аналогично метиловым эфирам.
Если мы перейдем к фталимидам, то их расщепление гидразином в MeOH или EtOH - не строго реакция сольволиза. На первой стадии имеет место атака гидразина на карбонильную группу имида (более чувствительна к атаке нуклеофильной, чем в амиде).

Защитные группы, удаляющиеся с помощью кислот.
Такое расщепление имеет место в случае третичных бензиловых и алкиловых эфиров.

Реакция требует промотирования H+ или кислот Льюиса. Здесь широкий разброс условий: например HBr в AcOH снимает защиту с бензиловых эфиров, а третиловые (Ph3C-) эфиры уже расщепляются разбавленной уксусной кислотой.
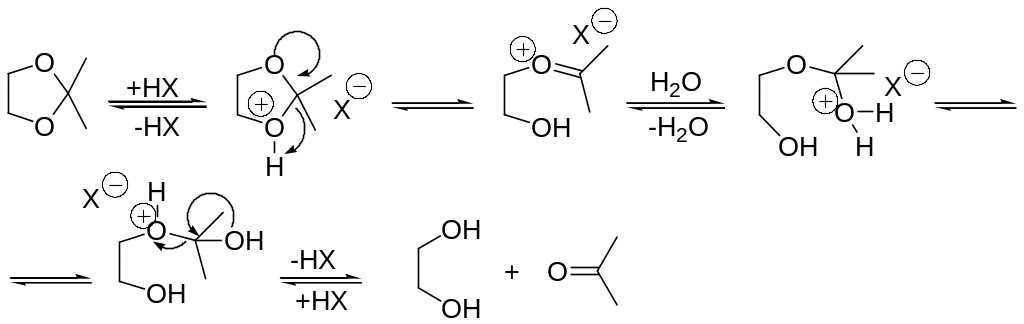
Вторая защитная группа, которая легко снимается в условиях кислого гидролиза – это ацетальная защита. В качестве кислот используют H+ или кислоты Льюиса.
M eOCH2OMe
(MOM)
- легко расщепляются в кислых условиях
в PhOCH2OMe
(BOM) процессе
гидролиза.
eOCH2OMe
(MOM)
- легко расщепляются в кислых условиях
в PhOCH2OMe
(BOM) процессе
гидролиза.
CH3-CH(OMe)2
Расщепление тяжелыми металлами.
Расщепление О,О ацеталей, O,S и S,S- ацеталей в условиях гидролиза можно катализировать солями Ag (I) и Hg (II).

Расщепление связей Si-C и Si-O под действием фтораниона.
Силильная защита - одна из наиболее перспективных защитных групп, которая разрабатывается в последние 20 лет. R3Si группа силиловых эфиров легко удаляется в условиях кислого и щелочного гидролиза.
Однако триалкилсилильная группа может быть снята действием Bu4NF в ТГФ или HF в ацетонитриле, KF в ДМСО. Это обусловлено возможностью взаимодействия F- с вакантными орбиталями атома Si с образованием пентакоординационного атома кремния.
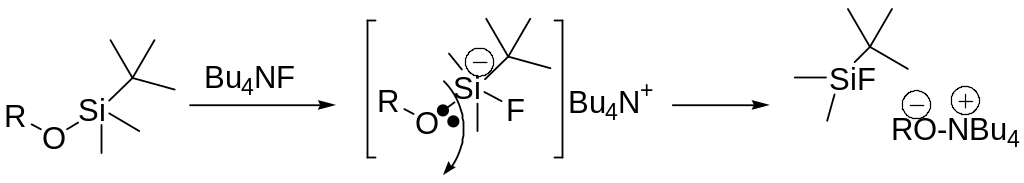
В качестве защитной группы может выступать триметилсилилэтильная группа, которая легко снимается действием F-.
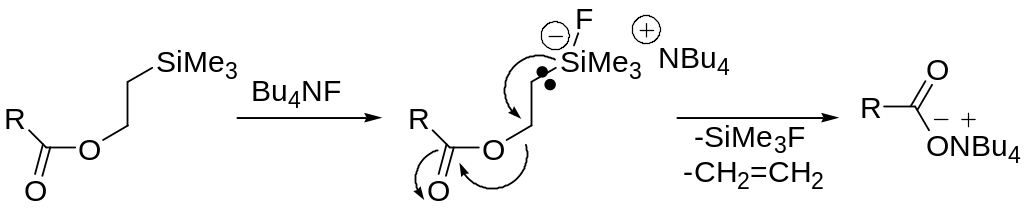
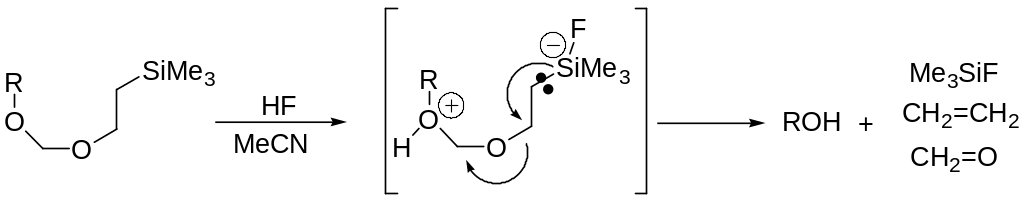
В основе всех этих процессов лежит реакция β-элиминирования.
Снятие защитных групп с помощью цинка.
Этот тип снятия защитной группы можно продемонстрировать следующим примером трихлорэтилового эфира.
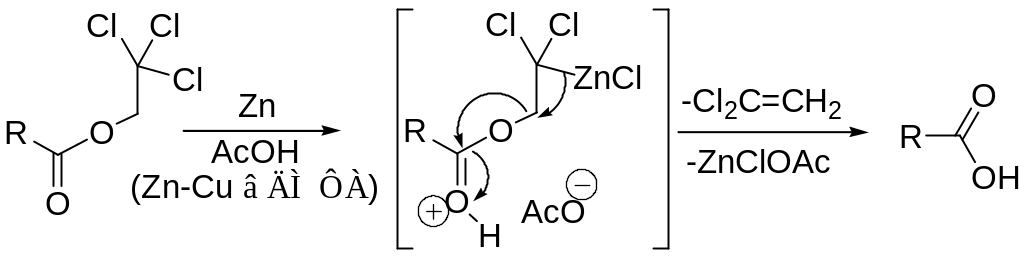
Снятие защиты с использованием реакции β-элиминирования.
Пример снятия защиты 9-флуоренилметоксикарбонильной (Fmoc). Механизм E1CB. Пиперидин или морфолин в ДМФА.
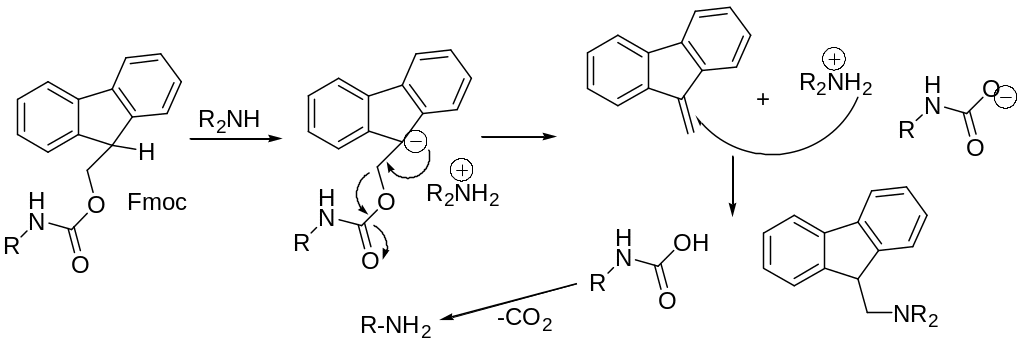
Fmoc защита используется в пепетидном и гликопептидном синтезе.
Снятие защиты реакцией гидрогенолиза.
Этот метод годен для снятия бензильной защиты в простых и сложных эфирах, карбоматах и аминах. Связь O-CH2Ph и N-CH2Ph легко расщепляется в условиях гидрогенолиза в присутствии Pd и др. переходных металлов. Иногда используют Ni Ренея. Бензильная защита используется в основном в синтезе пептидов.
Удаление защитной группы окислением.
Этот метод используется в синтезе п-метокси- и 3,4-диметоксибензиловых эфиров. В качестве окислителя используют 2,3-дихлор-5,6-дициано-1,4-бензохинон (DDQ). Идет перенос e- к DDQ.

Снятие защиты с помощью металлов в растворах.
Na или Li в жидком аммиаке расщепляет бензиловые простые и сложные эфиры в присутствии источника протонов с отщепленной алкоксидной или карбоксилатной уходящих групп.

Нуклеофильное расщепление связи C-O.

Это классическое нуклеофильное замещение. Нуклеофилы хлорид, иодид, цианид, тиофенолят в биполярном апротонном растворителе при повышенной температуре.
Ограничивается метиловыми и этиловыми эфирами. Большую роль играет стабилизация карбоксилат аниона, чем она выше, тем реакция идет легче.
Аналогично реагируют и фениловые эфиры.
Аллильные защитные группы.
Аллильные группы требуют для своего снятия мягких и специфических условий не затрагивающих других функциональных и защитных групп. Аллильная группа не используется для защиты спиртов, карбоновых кислот (аллиловые эфиры) и аминов (аллилкарбаматы).
Аллиловые простые эфиры стабильны в сильно щелочной среде, но расщепляются tBuOK в ДМСО, включая двухступенчатый процесс, вовлекающий изомеризацию двойной связи. При этом образуется эфиры енолов, которые гидролизуются мягкими кислотами.
Для целей снятия защиты можно использовать комплексы Rh (I). Возможный химизм процесса показан далее.

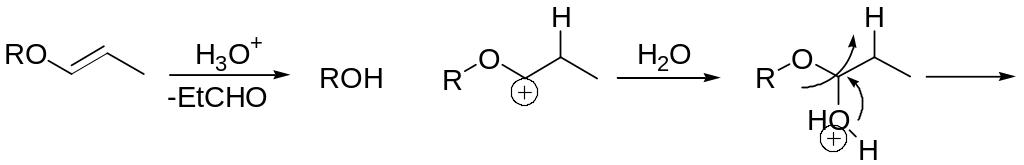
![]()
Снятие защиты при действии УФ.
о-Ниторбензиловые эфиры (спирт), о-ниторбензиловые карбаматы (амин), о-ниторбензилкарбонаты (спирт), о-ниторбензиловые сложные эфиры (карбоновые кислоты), о-ниторбензилиденацетали (1,2- и 1,3-диолы).
Схема протекания процесса.
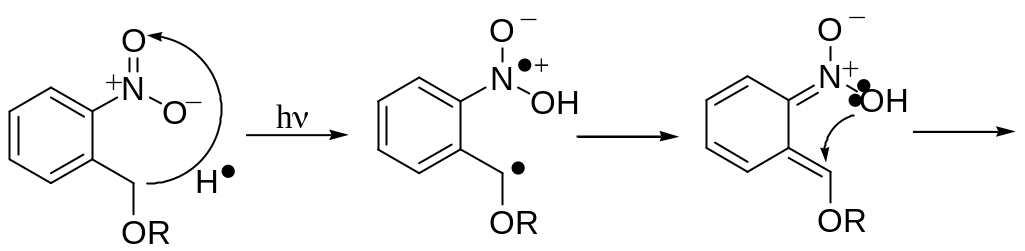

Снятие защитных групп.
Это случай когда защитная группа устойчива в широком интервале реакционных условий и в процессе реакции трансформируется в новую группу, которая лабильна и легко отщепляется в мягких условиях.
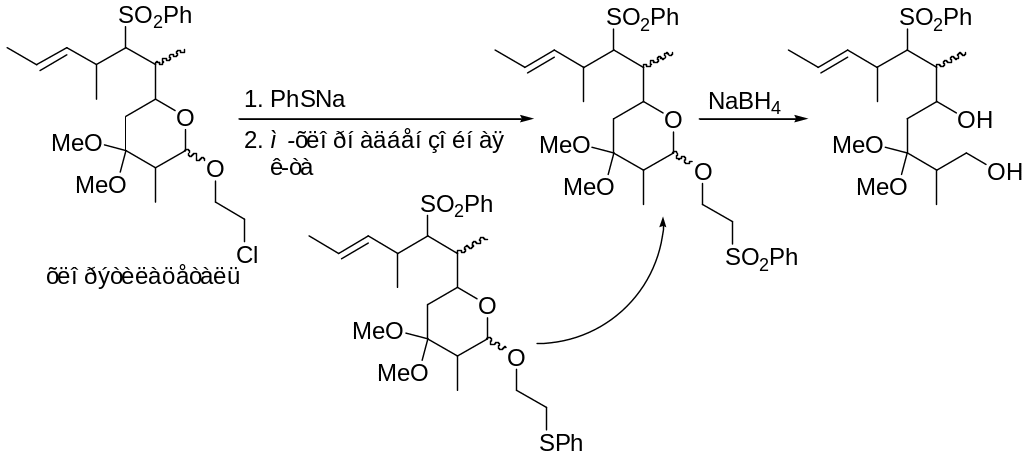
Временные защитные группы.

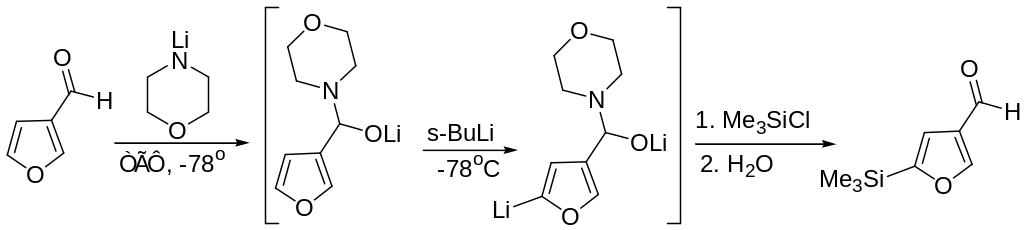
Когда требуется защитить на 1-2 стадии. Для того, чтобы провести реакции по менее активной кетонной функции оксоальдегида А. Альдегидную функцию защищают N-метиланилидом лития, затем проводят реакцию по кетогруппе. При водной обработке реакционной смеси временная защитная группа симается.
Еще один пример силилирования 3-формилфурана.