
спектр и фотометр
.pdf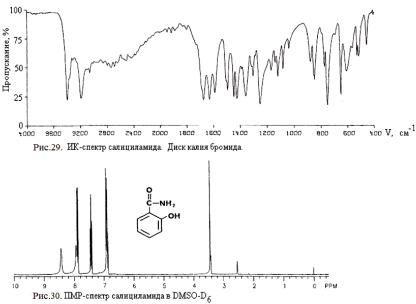
Производные салициламида и их лекарственные формы можно идентифицировать с помощью ИК-спектроскопии в области 3600-700 см-1.
Подлинность салициламида и осальмида подтверждают по
«амидным полосам поглощения», а также по поглощению в области 3600-3200 см-1, обусловленному наличием гидроксильных и аминогрупп. ФС рекомендует устанавливать подлинность салициламида и осальмида по совпадению полос поглощении ИК-спектров в области 4000-400 см-1 с прилагаемыми к ФС рисунками спектров.
Идентификация производных салициламида может быть выполнена также по характерным параметрам УФ-спектров поглощения (длина волны в максимуме и минимуме светопоглощения) в различных растворителях. Так, у 0,001%-ного водного раствора салициламида максимумы поглощения расположены в области 235 и 300 нм;у 0,002%-ного раствора осальмида в 0,1 М растворе гидроксида натрия – в области 310 и 335 нм.
По ФС подлинность салициламида устанавливают по УФ-спектру 0,0015%-ного раствора в смеси этанол – 0,01 М раствор хлороводородной кислоты (1:49). Он должен в области 220-350 нм иметь по два максимума (238 и 300 нм) и минимума (225 и 263 нм) поглощения. Раствор осальмида в этаноле в области 220-360 нм должен иметь максимум поглощения при 298 нм.
Известны методики спектрофотометрического количественного
определения салициламида и осальмида в указанных максимумах.
81
Посторонние примеси определяют в салициламиде методом ТСХ на пластинке со слоем силикагеля F-254. Испытуемое вещество и свидетель (растворы в метаноле) наносят на пластинку, сушат и хроматографируют в системе н-бутилацетат-хлороформ-кислота муравьиная (3:2:1). Пятно примеси по совокупности величины и интенсивности окраски не должно быть более, чем на 1% превышать пятно свидетеля.
Испытание выполняют методом ТСХ на пластинке «Силуфол УФ-254» или «Армсорб УФ-254», сравнивая пятна испытуемого вещества и СОВС (стандартный образец вещества-свидетеля) после хроматографирования в системе метанол-этилацетат (1:1). На хроматограмме после проявления парами йода должно появиться одно пятно, не превышающее по величине и интенсивности пятно СОВС.
Сложные эфиры кислоты салициловой
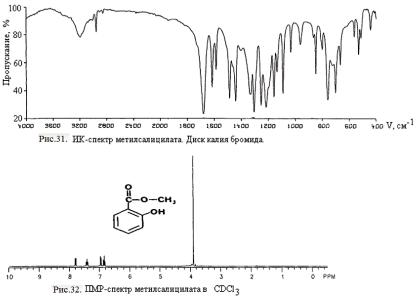
Mетилсалицилат синтезирован аналогичным способом, что и фенилсалицилат. Их структуры установлены исходя из данных ИК- и ПМР-спек- тров (см. рис. 31 и 32). Они обладают близкими физико-химическими и фармакологическими свойствами.
Подлинностькислоты ацетилсалициловой подтверждают по ИК-спек- тру в области 4000-400 см-1 (в дисках с бромидом калия). Он должен полностью совпадать с полосами поглощения прилагаемого к ФС спектра.
82
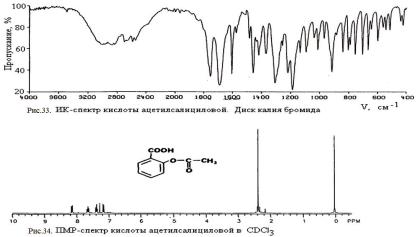
УФ-спектр 0,007%-ного раствора кислоты ацетилсалициловой в хлороформе имеет в области 260-350 нм максимум поглощения при 278 нм, а УФ-спектр 0,001%-ного раствора в 0,1 М растворе серной кислоты в области 220-350 нм – два максимума при 228 и 276 нм и один минимум поглощения при 257 нм (см. рис.33). Эти данные должны быть подтверждены также результатми анализа ПМР-спектра кислоты ацетилсалициловой
(см. рис. 34).
В результате исследования УФ-спектров поглощения растворов кислоты ацетилсалициловой и других сложных эфиров салициловой кислоты в различных растворителях (вода, этанол, хлороформ, дихлорэтан, 0,1 М раствор гидроксида натрия) разработаны методики их спектрофотометрического определения непосредственным и дифференциальным методами.
Описан УФ-спектрофотометрический способ определения кислоты ацетилсалициловой, основанный на предварительном ее гидролизе в щелочной среде до салицилата натрия в присутствии пероксида водорода. Последний ускоряет процесс гидролиза, окончание которого наступает через 15 мин. Затем измеряют оптическую плотность раствора на спектрофотометре в максимуме поглощения (290 нм).
Ибупрофен и диклофенак
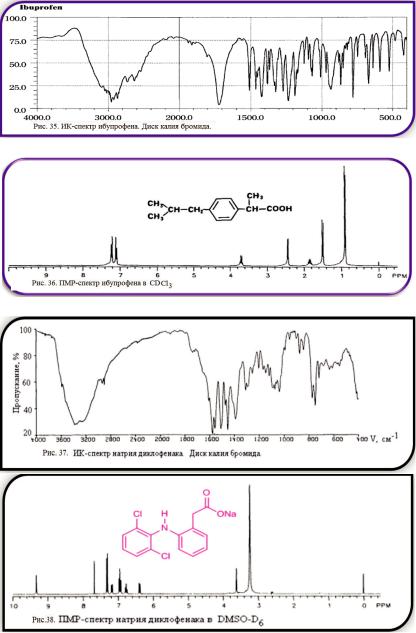
Строение ибупрофена установлено на основание данных ИК- и ПМР-спектров (см. рис. 35 и 36).
Строение натрия диклофенака установлено на основание данных ИК- и ПМР-спектров (см. рис. 37 и 38).
83
84
К ФС на натрия диклофенак и ибупрофен прилагаются рисунки ИК-спектров, полосы поглощения которых должны полностью соответствовать ИК-спектрам испытуемых лекарственных веществ в области
4000-400 см-1
Подлинность устанавливают также с помощью УФ-спектров. Растворы ибупрофена в 0,1М растворе натрия гидроксида в области 240-350 нм имеют максимумы поглощения при 256, 273 нм и плечо от 257 до 261 нм, а УФ-спектр натрия диклофенака в том же растворителе – максимум поглощения при 276 нм и минимум при 249 нм.
Подлинность ибупрофена подтверждают также методом ВЭЖХ, сравнивая со стандартным образцом. Наличие посторонних примесей в ибупрофене устанавливают методом ГЖХ (по отношению суммы площадей пиков, обусловленных примесями, к площади пика ибупрофена) и методом ТСХ на силикагеле по сравнению интенсивности окраски пятен растворов испытуемого вещества, содержащих 100 мг/мл и 1 мг/мл.
При испытании на чистоту натрия диклофенака устанавливают методом ВЭЖХ наличие примесей промежуточных продуктов синтеза: 2-[2,6-(дихлорфенил)-амино]-фенилуксусной кислоты и N-(2,6- дихлорфенил)-индолинона-2. Используют подвижную фазу: метанол – 0,1% раствор ортофосфорной кислоты (6:4), детектор – спектрофотометр (длина волны 254 нм).
Для количественного определения ибупрофена используют метод ВЭЖХ с подвижной фазой: хлоруксусная кислота – раствор аммиака – ацетонитрил, детектируют при длине волны 254 нм.
Аминопроизводные ароматического ряда Парацетамол
Подлинность парацетамола подтверждают по ИК-спектру (снятому в вазелиновом масле) в области 4200-400 см¯1 (см. рис. 39). Полосы поглощения должны полностью совпадать с прилагаемым к ФС рисунком спектра.
УФ-спектр 0,0005% раствора парацетамола в метаноле, подкисленном хлороводородной кислотой, в области 220-350 нм имеет максимум поглощения при длине волны 249 нм. Водный раствор имеет максимум поглощения при 243 нм, а раствор в 0,001М гидроксиде натрия – два максимума при 257 и 273 нм.
Разработан способ спектрофотометрического определения парацетамола в таблетках, основанный на использовании в качестве стандартного образца дихромата калия (при длине волны 243 нм). Положительные результаты при анализе парацетамола в лекарственных формах были достигнуты методом производной спектрофотометрии. Более селективным
85
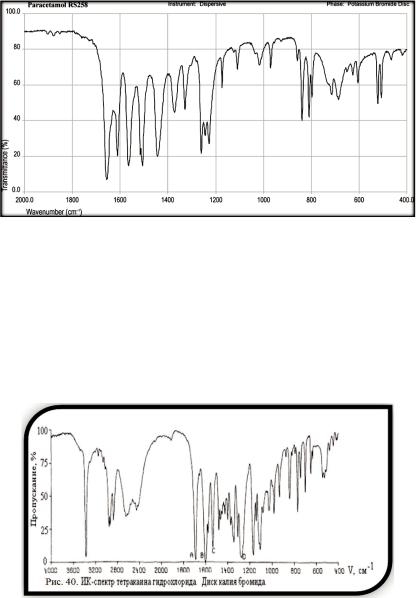
при определении парацетамола в присутствии продуктов разложения оказался метод ГЖХ.
Рис. 39. ИК-спектр парацетамола. Диск калия бромида
Аминокислоты ароматического ряда: анестезин, дикаин, новокаин амид и др.
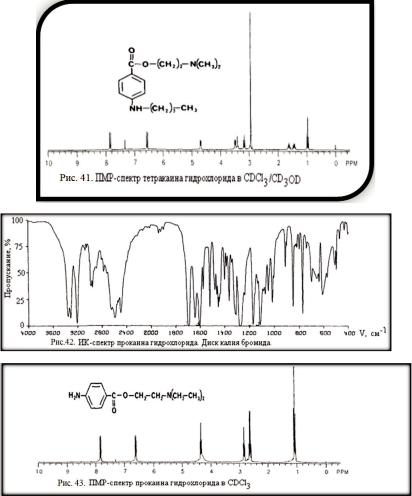
Строение тетракаина гидрохлорида однозначно определяется данными анализа его ИК- и ПМР-спектров (см. рис. 40 и 41).
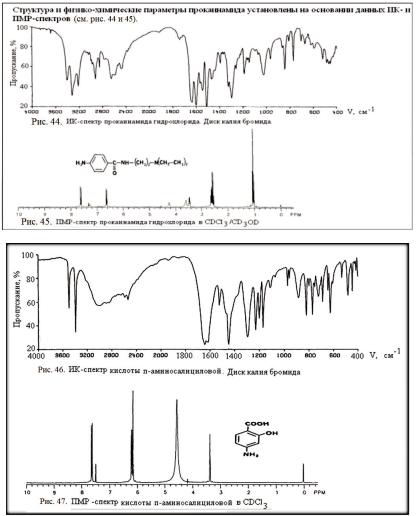
Структура и физико-химические параметры прокаина гидрохлорида установлены на основании ИК- и ПМР-спектров (см. рис. 42 и 43).
Строение и физико-химические параметрыПАСКи ее производных установлены в результате изучения их ИК- и ПМР-спектров (см. рис. 46 и 47).
86
Подлинность (по ФС) бензокаина, прокаина и тетракаина гидрохлоридов устанавливают по идентичности ИК-спектров, снятых после прессования в таблетках бромида калия в области 4000-400 см-1 и прилагаемых к ФС рисунков спектров стандартных образцов.
УФ-спектры испытуемых лекарственных веществ должны иметь характеристики, приведенные в соответствующих ФС.
Так, УФ-спектр 0,005%-ого бензокаина в хлороформе в области 230350 нм должен иметь максимум поглощения при 281 нм и минимум поглощения при 238 нм.
87
Водный 0,001%-ый раствор прокаина гидрохлорида имеет максимум поглощения при 290 нм.
Раствор тетракаина гидрохлорида в воде (в присутствии фосфатного буфера с рН=6) в области 220-350 нм должен иметь два максимума поглощения при 227 и 310 нм, а также минимум поглощения при 249 нм.
Для идентификации производных п-аминобензойной кислоты использованы также различные оптические характеристики электронных полос поглощения (сила осциллятора, фактор асимметрии и др.).
88
Разработан способ обнаружения и количественного определения прокаинамида гидрохлорида, основанный на использовании обращено-фа-
зового варианта ВЭЖХ с УФ-детектированием при длине волны 280
нм. Количественное определение выполняют, используя подвижную фазу метанол-буферный раствор с рН=4,0 (15:85). Внутренним стандартом служит прокаина гидрохлорид.
Газожидкостная хроматография использована в качестве под-
тверждающего метода по идентификации прокаинамида гидрохлорида, в т. ч. в биологических жидкостях. В лекар-ственных формах прокаинамида гидрохлорид количественно определяют методом УФ-спектрофото- метрии, используя в качестве растворителя воду. Параллельно измеряют оптическую плотность стандартного и испытуемого растворов при длине волны 278 нм.
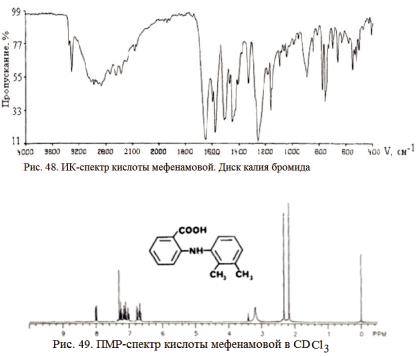
Структура и другие физико-химические параметры кислоты мефенамовой установлены на основании изучения ее ИК- и ПМР-спектров
(см. рис. 48 и 49).
89
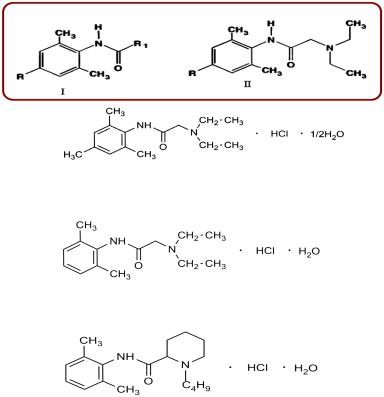
ПРОИЗВОДНЫЕ ДИЭТИЛАМИНОАЦЕТАНИЛИДА. ТРИМЕКАИН, КСИКАИН, УЛЬТРАКАИН
Кроме сложных эфиров п-аминобензойной кислоты местноанестезиру-
ющую активность проявляют производныедиметилфенилацетамида (I).
Тримекаина гидрохлорид и лидокаина гидрохлорид – производные диалкиламино-ацетанилида (II) и бупивакаина гидрохлорид – производное пиперидинкарбоксамида.
Тримекаина гидрохлорид (Trimecaine Hydrochloride)
2-(диэтиламино)-N-2’,4’,6’-триметилфенилацетамида гидрохлорид, гемигидрат
Лидокаина гидрохлорид (Lidocaine Hydrochloride)
2-(диэтиламино)-N-2’,6’-ацетоксилидида гидрохлорид, моногидрат
Бупивакаина гидрохлорид (Bupivacaine Hydrochloride)
1-бутил-2’,6’-диметилфенил-2-пиперидинкарбоксамида гидрохлорид, моногидрат.
Указанные лекарственные вещества имеют много общего в химической структуре. Это обуславливает общность их способов получения, свойств, испытаний и применения.
Структуру и физико-химические свойства лидокаина гидрохлорида определяют на основание данных ИК- и ПМР-спектров (см. рис. 50 и 51):
90
