
- •1 Основная часть
- •1.1 Аналитические обзор литературы
- •1.2 Характеристика сырья и готовой продукции
- •1.3 Физико-химические основы процесса
- •2 Специальная часть
- •2.1 Описание технологической схемы установки
- •2.2 Расчет материального баланса
- •2.3 Расчет теплового баланса
- •2.4 Аналитический контроль производства
- •2.5 Безопасность эксплуатации производства
1.3 Физико-химические основы процесса
Химический состав серной кислоты выражается формулой Н2SO4.
Молекулярный вес 98,08.
Структурная формула серной кислоты:
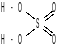
Серную кислоту следует рассматривать как соединение одной молекулы триоксида серы SО3 с одной молекулой воды Н2О. В технике под серной кислотой подразумевают любые смеси триоксида серы с водой. Смеси, в которых на 1 моль SО3 приходится больше 1 моля воды, являются водными растворами серной кислоты. Смеси, в которых на 1 моль SО3 приходится меньше 1 моля воды, называются олеумом, они содержат свободный триоксид серы.
Водные растворы серной кислоты характеризуют процентным содержанием Н2SO4 или SO3.Безводная серная кислота содержит 100 % Н2SO4 или 81,63 % SO3 и 18,37 % Н2О.
Таблица 3 - Виды товарной серной кислоты.
Вид товарной серной кислоты |
Концентрация,% |
Температура кристаллизации, °С |
Башенная кислота |
75% |
-29,5°С |
Контактная кислота |
92,5% |
-22,0°С |
Олеум |
20% своб. SO3 |
+2°С |
Плотность.
С увеличением содержания Н2SO4 плотность водных растворов серной кислоты повышается и достигает максимума при 98,3 % Н2SO4, затем несколько уменьшается и при 20 оС для 100 % Н2SO4 достигает 1,8305 г/см3. Плотность олеума возрастает с увеличением содержания SO3 до максимума при 62 % SO3 свободного, а затем уменьшается. С повышением температуры плотность серной кислоты уменьшается.
Таблица 4 - Плотность растворов серной кислоты в зависимости от температуры
Концентрация кислоты, % |
Т е м п е р а т у р а , оС |
|||||||||
5 |
10 |
20 |
25 |
30 |
40 |
50 |
60 |
70 |
80 |
|
95 |
1,8491 |
1,8439 |
1,8337 |
1,8286 |
1,8236 |
1,8137 |
1,8040 |
1,7944 |
1,7848 |
1,7751 |
96 |
1,8508 |
1,8457 |
1,8355 |
1,8305 |
1,8255 |
1,8157 |
1,8060 |
1,7965 |
1,7869 |
1,7773 |
97 |
1,8517 |
1,8466 |
1,8364 |
1,8314 |
1,8264 |
1,8166 |
1,8071 |
1,7976 |
1,7881 |
1,7785 |
98 |
1,8515 |
1,8463 |
1,8361 |
1,8310 |
1,8261 |
1,8163 |
1,8068 |
1,7978 |
1,7882 |
1,7786 |
99 |
1,8498 |
1,8445 |
1,8342 |
1,8282 |
1,8242 |
1,8145 |
1,8050 |
1,7958 |
1,7868 |
1,7778 |
"Справочник сернокислотчика" Изд. "Химия", Москва, 1971, стр. 88.
Упругость водяных паров над серной кислотой
Водные растворы серной кислоты, при температуре далекой от точек кипения, выделяют водяные пары. С повышением концентрации кислоты (при неизменной температуре) упругость водяных паров над кислотой понижается. Концентрированные растворы серной кислоты при низких температурах имеют невысокую упругость водяных паров. На этом основано применение концентрированной серной кислоты для осушки атмосферного воздуха.
С повышением температуры упругость водяных паров повышается и тем быстрее, чем ниже концентрация кислоты
Таблица 5 - Полное давление паров над растворами серной кислоты.
Концентрация кислоты, % |
Температура, оС |
|||||
20 |
40 |
60 |
80 |
100 |
120 |
|
( в мм.рт.ст) |
||||||
90 |
0,005 |
0,027 |
0,120 |
0,450 |
1,49 |
4,19 |
95 |
- |
0,002 |
0,013 |
0,061 |
0,257 |
0,79 |
98,3 |
2,10-4 |
10-3 |
5,10-3 |
0,02 |
0,07 |
0,22 |
Амелин А.Г. "Технология серной кислоты". Изд. "Химия", Москва, 1971
Теплоемкость.
С повышением концентрации растворов серной кислоты их теплоемкость уменьшается и достигает минимума для безводной серной кислоты 1,42 Дж/(г.град). С повышением температуры теплоемкость водных растворов серной кислоты несколько возрастает.
Таблица 6 - Теплоемкость растворов серной кислоты.
Концентрация кислоты, % |
Температура, оС |
|||||
20 |
22,5 |
25 |
40 |
60 |
80 |
|
( в ккал/кг.град) |
||||||
95 |
0,354 |
0,351 |
0,357 |
0,364 |
0,370 |
0,382 |
97,5 |
0,341 |
0,338 |
0,342 |
0,353 |
0,358 |
0,366 |
100 |
0,335 |
0,332 |
0,337 |
0,343 |
0,351 |
0,359 |
"Справочник сернокислотчика" Изд. "Химия", Москва, 1971.
При испарении и кипении водных растворов серной кислоты, содержащих до 70 % Н2SO4, выделяется в паровую фазу только вода. Над растворами с большим содержанием Н2SO4 в парах вместе с водой появляется SO3 и серная кислота.
Внешний вид технической серной кислоты
Концентрированная серная кислота – маслянистая жидкость от прозрачного до светло-коричневого цвета. Концентрированная серная кислота при воздействии на вещества животного и растительного происхождения обугливает их. Попав на кожу человека, если ее не смыть водой, причиняет ожог. При разведении концентрированной серной кислоты водой выделяется большое количество тепла, вследствие чего раствор сильно нагревается.
Регистрация продукта
Серная кислота зарегистрирована российским регистром потенциально опасных химических и биологических веществ (РПОХВ) – свидетельство о государственной регистрации серия АТ № 000058 от 17.06.1994 г. с постоянным сроком действия.
