
- •Химический контроль.
- •Физический – проверяют с помощью мерного цилиндра общий объем микстуры. Допустимые нормы отклонений в общем объеме жидких лекарственных форм свыше 50 мл ± 3% (приказ мз рф №305).
- •Химический контроль.
- •Физический – проверяют с помощью мерного цилиндра общий объем микстуры. Допустимые нормы отклонений в общем объеме жидких лекарственных форм объемом 102 мл ± 3% (приказ мз рф №305).
- •Химический контроль.
- •Химический контроль.
- •Химический контроль.
Химический контроль.
Качественный анализ
Натрия гидрокарбонат (Na+): графитовую палочку, смоченную микстурой, вносят в бесцветное пламя горелки. Пламя окрашивается в желтый цвет.
Натрия гидрокарбонат (HCO3): К 2 мл раствора прибавляют 5 капель насыщенного раствора магния сульфата. При кипячении образуется белый осадок.
2NaHCO3 –> Na2CO3+CO2+H2O
4Na2CO3+4MgSO4+4H2O ⇒ 3MgCO3⋅Mg(OH)2⋅3H2O↓+4Na2SO4+CO2↑
Натрия бензоат: к 1 мл микстуры прибавляют 1 каплю раствора метилового оранжевого, 2-3 мл эфира, разведенную соляную кислоту до розового окрашивания и взбалтывают. Эфирный слой отделяют и эфир отгоняют. К остатку прибавляют 1-1,5 мл раствора аммиака и выпаривают на водяной бане, сухой остаток растворяют в 1 мл воды и добавляют 1-2 капли раствора окисного железа хлорида. Образуется розовато-желтый осадок.
6C6H5COONa + 2FeCl3 + 10Н2О (C6H5COO)3Fe·Fe(OH)3·7Н2О + 6NaCl + 3C6H5COOH
Нашатырно-анисовые капли: органолептическое определение по характерному запаху анисового масла и аммиака.
Количественный анализ
Натрия гидрокарбонат: К 0,5 мл раствора прибавляют 5 мл свежепрокипяченной и охлажденной воды, 1 каплю раствора метилового оранжевого и титруют при встряхивании 0,1 н. раствором соляной кислоты до появления розовой окраски. 1 мл 0,1 н. раствора соляной кислоты соответствует 0,0084 г натрия гидрокарбоната.
NaHCO3+HCl –> NaCl + CO2↑ + H2O
m (навески) = 0,5
НДО ± 8%
0,5 – 100%
х – 8% => x = 0,04
X в.п. = 0,54
X н.п. = 0,46
X =
Vmax
=
=
 =
0,3 мл
=
0,3 мл
Vmin
=
=
 =
0,26 мл
=
0,26 мл
Vт1 = 0,27
Vт2 = 0,28
Vт3 = 0,29
Vтсред = 0,28 мл
Х =
 = 0,48
= 0,48
Натрия бензоат: К 1 мл раствора прибавляют 4,5 мл эфира, 3-4 капли смешенного индикатора (1 мл раствора метилового оранжевого и 1 мл раствора метиленового синего) и титруют 0,5 н. раствором соляной кислоты до появления сиреневой окраски в водном слое. В конце титрования содержимое колбы хорошо встряхивают. 1 мл 0,5 н. раствора соляной кислоты соответствует 0,07205 г бензоата натрия.

m (навески) = 0,5
НДО ± 8%
0,5 – 100%
х – 8% => x = 0,04
X в.п. = 0,54
X н.п. = 0,46
X =
Vmax
=
=
 =
0,22 мл
=
0,22 мл
Vmin
=
=
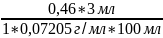 =
0,19 мл
=
0,19 мл
Vт1 = 0,19
Vт2 = 0,2
Vт3 = 0,21
Vтсред = 0,2 мл
Х =
 = 0,49
= 0,49
Вывод: лекарственная форма приготовлена удовлетворительно. (10,14,16)
