
- •Содержание
- •Введение
- •Глава 1 основы химизма и кинетики каталитического крекинга
- •1.1 Основные химические реакции различных компонентов сырья
- •1.2 Механизм протекания реакций в процессе каталитического крекинга
- •1.3 Образование кокса
- •1.4 Кинетика и термодинамика процесса
- •Глава 2 катализаторы крекинга
- •2.1 Строение и состав катализаторов крекинга
- •2.2 Промышленные катализаторы крекинга
- •Глава 3 Сырье и продукты процесса каталитического крекинга
- •Глава 4 Основные факторы процесса каталитического крекинга
- •Глава 5 Технологическая схема и основное оборудование процесса каталитического крекинга
- •5.1 Описание технологической схемы секции 2000
- •5.2 Технологическое оборудование секции 2000
- •Глава 6 пуск, эксплуатация и остановка установки mscc
- •6.1 Пуск установки
- •6.2 Эксплуатация установки
- •6.3 Автоматизация и управление процессом
- •6.4 Некоторые неполадки в работе установки
- •6.5 Плановая остановка установки
- •6.6 Особенности аварийной остановки установки
- •Глава 7 Охрана окружающей среды на нПз, имеющем установку каталитического крекинга
- •7.1 Выбросы в атмосферу
- •7.2 Выбросы в водный бассейн
- •7.3 Защита литосферы
- •Глава 8 Техника безопасности на установке каталитического крекинга
- •8.1 Противопожарные мероприятия
- •8.2 Характеристика токсичных, пожароопасных и экологоопасных свойств сырья и продуктов
- •8.3 Основные правила газобезопасности
- •8.4 Защитная одежда и защитные средства
- •8.5 Мероприятия по повышению взрывобезопасности установки каталитического крекинга
- •Рекомендуемая литература
1.2 Механизм протекания реакций в процессе каталитического крекинга
Реакции углеводородов на катализаторах крекинга протекают по карбокатионному механизму. Карбкатионы (карбоний-ионы) – это органические ионы с положительным зарядом на одном из атомов углерода. Они могут образоваться в результате отрыва от насыщенного углеводорода гидрид-иона (протона с двумя электронами) или присоединения к ненасыщенному углеводороду протона. Карбкатионы являются промежуточными продуктами в каталитическом крекинге и образуются только благодаря наличию у катализатора кислотных центров. Кислота – это вещество способное отдавать протон или принимать неподеленную пару электронов. В катализаторе крекинга отдают протоны кислотные центры Бренстеда, а принимают неподеленную пару электронов кислотные центры Льюиса (более подробно о кислотных центрах катализатора будет сказано в главе 2).
Реакция крекинга фактически не может иметь места, пока углеводород не приблизится к поверхности катализатора настолько, что окажется в зоне действия кислотного центра катализатора:
НАН+ + А–,
где НА – условное изображение алюмосиликатного катализатора в виде кислоты,
Н+ – протон (атом водорода без электрона, имеющий положительный заряд),
А– – отрицательно заряженная кристаллическая решетка цеолита, входящего в состав катализатора.
Участие в реакции протона водорода с катализатора (Бренстедовский кислотный центр) доказано с помощью меченых атомов. Карбкатионы являются активными промежуточными продуктами многих реакций, протекающих при каталитическом крекинге. Они содержат трехвалентный положительно заряженный атом углерода и легче всего образуются при взаимодействии протона катализатора с алкенами:
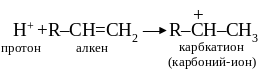
Небольшие количества алкенов могут образоваться при термическом распаде алканов при повышенных температурах в сырье, направляемом в реактор каталитического крекинга.
Образование карбоний-иона возможно также протонированием алкана бренстедовским кислотным центром:

Альтернативно в протонированном алкане может произойти расщепление связи С—С:

Ароматические углеводороды также могут быть акцепторами протонов, в результате чего образуется карбоний-ион:

В условиях каталитического крекинга карбоний-ионы могут существовать только в виде ионных пар: карбоний-ион – отрицательный активный центр поверхности катализатора.
Карбоний-ион, образующийся при взаимодействии углеводорода с кислотными центрами катализатора, претерпевает быстрые дальнейшие превращения:
скелетная изомеризация карбоний-ионов (перегруппировка атомов водорода или метильных групп):
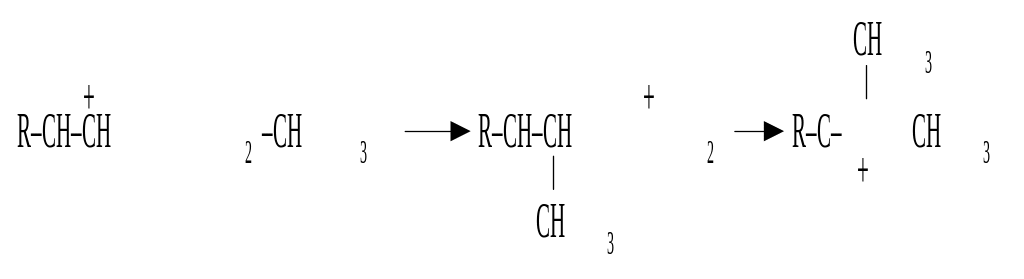
отрыв гидрид-иона от молекулы насыщенного углеводорода с образованием нового карбоний-иона:

распад карбоний-иона по связи в -положении относительно заряженного атома углерода с образованием -олефина и более мелких первичных карбкатионов с последующей их быстрой перегруппировкой в более устойчивые вторичные карбоний-ионы:
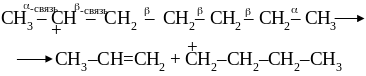
Последовательное превращение карбоний-иона продолжается до достижения наиболее устойчивой структуры:

Высокой стабильностью обладают карбоний-ионы с зарядом у третичного атома углерода (а) и с ароматическим фрагментом (б):

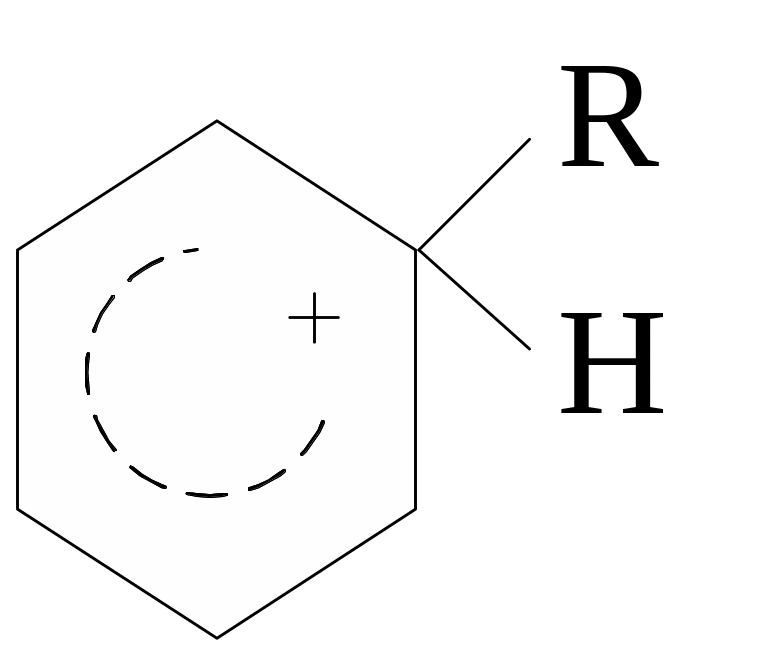
(а) (б)
Устойчивость карбоний-ионов определяет степень их участия в дальнейших реакциях. Например, высокая стабильность третичных карбониевых ионов обусловливает высокий выход изопарафиновых углеводородов в условиях промышленного каталитического крекинга:
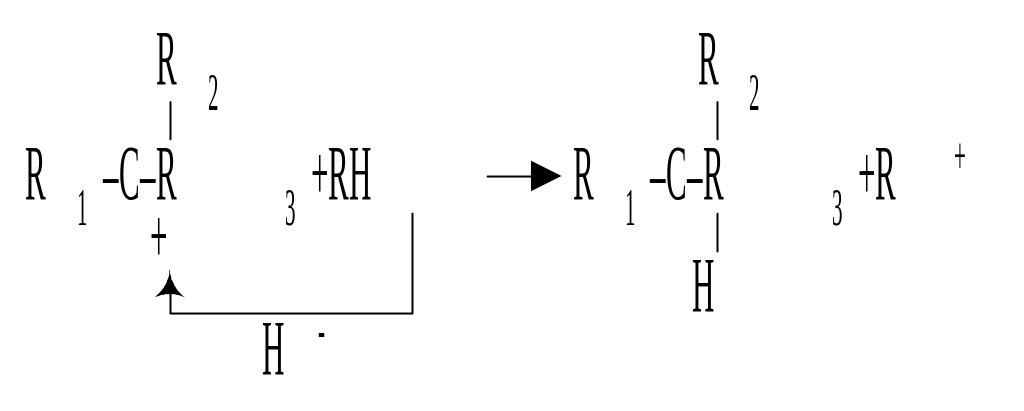
Реакция переноса гидрид-иона (Н-переноса) наряду с расщеплением и изомеризацией углеродного скелета в значительной степени определяет качество продуктов крекинга.
В результате изомеризации карбоний-иона образуются более разветвленные и, соответственно, более стабильные частицы, например:

и

В результате подобных превращений продукты каталитического крекинга обогащены изомерными углеводородами, за счет чего повышается октановое число бензина. Этот эффект усиливается вследствие перераспределения водорода между непредельными углеводородами и циклоалканами, присутствующими в реакционной массе:

алкен циклоалкан алкан арен
Арены, как и разветвленные алканы, повышают детонационную стойкость моторных топлив и это вносит дополнительный вклад в повышение октанового числа бензина.
Вследствие
малой устойчивости карбоний-ионов
![]() и
и
![]() в газах каталитического крекинга
преобладают углеводороды С3-С4.
в газах каталитического крекинга
преобладают углеводороды С3-С4.
Ниже приведены ряды классов углеводородов по убыванию их склонности к химическим превращениям при каталитическом крекинге:
алкены > арены с большим числом боковых цепей > циклоалканы > алканы.
Реакционная способность различных углеводородов в условиях промышленного процесса объясняется избирательностью адсорбции на поверхности катализатора – в первую очередь адсорбируются ненасыщенные углеводороды (алкены, арены). Наименьшей адсорбируемостью обладают алканы.
