
Практическая работа №6
Тема работы: энергетический баланс.
Цель работы: обрести навыки составления энергетического баланса предприятия.
Теоретические сведения
Энергетический баланс любого технического объекта (аппарата, установки, технологической линии транспортного средства, производства ) или экологической системы может быть описан уравнениями, связывающими приход и расход энергии. Энергетический баланс составляется на основе закона сохранения энергии, в соответствии с которыми в некоторой замкнутой системе сумма всех видов энергии постоянна :

Наиболее часто для технических, геотехнических и экологических систем составляется тепловой баланс, который для непрерывных процессов рассчитывается на единицу времени, а для периодических – на время цикла, процесса. Основой для расчета служит материальный баланс с учетом тепловых эффектов экзо – и эндотермических химических реакций, а также физических процессов испарения, конденсации, сублимации, растворения и др.
Методика расчета
Подобно материальному, тепловой баланс может быть представлен в виде таблиц, диаграмм в соответствии с уравнением:
 ,
,
где  –
количество теплоты, вносимое газообразными
(жидкими, твердыми) веществами в систему;
–
количество теплоты, вносимое газообразными
(жидкими, твердыми) веществами в систему;
 – количествотеплоты, выносимое из
системы;
– количествотеплоты, выносимое из
системы;
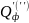 –теплотафизических
процессов, протекающих с выделением
(поглощением) тепла;
–теплотафизических
процессов, протекающих с выделением
(поглощением) тепла;
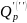 – количество
теплоты, выделяющееся
(поглощаемое) в экзотермических
(эндотермических) процессах;
– количество
теплоты, выделяющееся
(поглощаемое) в экзотермических
(эндотермических) процессах;
 –
количество
теплоты, подводимое к системе (отводимое
от системы).
–
количество
теплоты, подводимое к системе (отводимое
от системы).
Величины Qг, Qж, Qт рассчитываются для каждого вещества с учетом его количества (Ω), удельной теплоемкости (с) и температуры (Т) по формуле:

Теплоемкость смеси веществ рассчитывается на основании закона аддитивности:

Суммарная теплота физических процессов определяется по формуле:
 ,
,
где  – теплота фазовых переходов.
– теплота фазовых переходов.
Тепловой эффект химической реакции определяется как разница между суммой изобарных теплот образования исходных веществ и суммой изобарных теплот образования продуктов реакции по формуле:

5. Подвод
теплоты к системе
 учитывается
по потерям количества тепла теплоносителя:
учитывается
по потерям количества тепла теплоносителя:
-водой 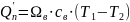
-паром 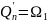
-теплопередачей
через стенку  ,
,
где  –коэффициент
теплопередачи;
–коэффициент
теплопередачи;
 – температура
теплоносителя на входе (выходе);
– температура
теплоносителя на входе (выходе);
F – поверхность теплообмена;
τ – время.
При определении низшей и высшей теплоты сгорания топлива в технических расчетах можно пользоваться формулами:
 =339,3⋅C+
1256⋅H – (O – S) – 25,2(9⋅H+ W);
=339,3⋅C+
1256⋅H – (O – S) – 25,2(9⋅H+ W);
 =
+25,2⋅(9⋅H+W)
=
+25,2⋅(9⋅H+W)
Теоретический расход воздуха (в кг/кг топлива) рассчитывается по формуле:
 =
0,116⋅С+ 0,348 ⋅Н +0,0135⋅(S–O)
=
0,116⋅С+ 0,348 ⋅Н +0,0135⋅(S–O)
Количество тепла, вносимого влажным воздухом, определяется по формуле:
 =
= ⋅
⋅(1,02+1,95⋅
⋅
⋅(1,02+1,95⋅ )
) ,
,
где – коэффициент избытка воздуха. Для твердого топлива α= 1,3...1,7; жидкого α= 1,0..1,2;
– влагосодержание воздуха (кг/кг сухого воздуха );
 – температура,
подаваемого в топочное устройство;
– температура,
подаваемого в топочное устройство;
1,02 – значение удельной теплоемкости воздуха;
1,95 – значение удельной теплоемкости водяных паров.
