
- •Програма курсу вступ
- •Тема 1. Основні поняття і закони хімії
- •Розділ 1. Будова речовини
- •Тема 2. Будова атома
- •Тема 3. Періодичний закон
- •Тема 4. Хімічний зв'язок
- •Тема 5. Основи хімічної термодинаміки
- •Тема 6. Хімічна кінетика
- •Тема 7. Хімічна рівновага
- •Розділ 3. Розчини та колоїдні системи
- •Тема 8. Розчини
- •Тема 9. Колоїдні системи
- •Розділ 4. Основи електрохімії
- •Тема 10. Окисно-відновні процеси
- •Тема 11. Електрохімічні процеси
- •Тема 12. Корозія та захист металів та сплавів
- •Розділ 5. Хімія елементів та їх сполук
- •Тема 13. Хімія металів та їх сполук
- •Тема 14. Хімія неметалічних елементів та їх сполук
- •Розділ 6. Хімія органічних сполук
- •Тема 15. Теорія хімічної будови
- •Тема 16. Вуглеводні
- •Тема 17. Оксигеновмісні органічні сполуки
- •Тема 19. Полімерні матеріали
- •Розділ 7. Тема 20. Хімія та охорона навколишнього середовища
- •Література
- •Вступ. Тема 1. Основні поняття і закони хімії
- •78 Г бензолу потребує 7,5 молей кисню
- •1000 Г бензолу потребує n молей кисню
- •Розділ 1. Будова речовини
- •Тема 2. Будова атома
- •Тема 3. Періодичний закон
- •Тема 4. Хімічний зв'язок
- •Розділ 2. Загальні закономірності хімічних процесів
- •Тема 5. Основи хімічної термодинаміки
- •Перший наслідок з закону Гесса:
- •Другий закон (постулат) термодинаміки:
- •Тема 6. Хімічна кінетика
- •Тема 7. Хімічна рівновага
- •Рівновага в гетерогенних системах
- •Розділ 3. Розчини та колоїдні системи
- •Тема 8. Розчини
- •Тема 9. Колоїдні системи
- •Тема 10. Окисно–відновні процеси
- •Тема 11. Електрохімічні процеси. Хімічні джерела струму. Електроліз
- •Тема 12 Корозія металів
- •Тема 13. Хімія металів. Класифікація та номенклатура неорганічних сполук
- •Лужні та лужно-земельні метали
- •Легкі конструкційні метали (Be, Mg, Al, Ti )
- •Важкі конструкційні метали. Хімічні властивості заліза.
- •Горіння металів
- •Тема 14. Хімія неметалів
- •1. Загальна характеристика неметалів
- •Хімічні властивості сульфуру
- •Розділ 6. Хімія органічних сполук
- •Тема 15. Теорія хімічної будови
- •Тема 16. Вуглеводні
- •Пожежна небезпека вуглеводів
- •Галогеновуглеводні вуглеводнів, їх застосування у пожежній справі
- •Номенклатура та ізомерія
- •Будова та реакційна здатність
- •Приклад 50.
- •Застосування галогенпохідних у пожежній справі
- •Тема 17. Кисневмісні органічні сполуки
- •Властивості карбонових кислот та їх похідних
- •Тема 18. Азотовмісні та елементорганічні сполуки
- •Класифікація амінів
- •Амінокислоти як мономери білків
- •Тема 19. Полімерні матеріали.
- •Середовища Роль хімії в розв'язанні екологічних проблем
- •Проблема радіоактивних відходів
- •Завдання для самостійного розв’язання
- •Додаток
- •Значення деяких фізико-хімічних констант
- •Значення електронегативностей елементів за Полингом)
- •Термодинамічні властивості деяких речовин.
- •Класифікація електролітів за їх силою
- •Добутки розчинності деяких сполук у воді при 298к
- •Стандартні електродні потенціали
- •Навчальне видання
- •Практикум
- •61023 М. Харків, вул. Чернишевського, 94
Горіння металів
На здатність металу до горіння впливають властивості як самих металів, так і властивості їх оксидів. Особливо великий вплив мають такі фактори: активність металу, захисні властивості оксидної плівки, що утворюється на поверхні металу, температура плавлення та кипіння металу та оксиду металу. За характером горіння розрізняють леткі та нелеткі метали.
Горіння летких металів (Li, Na, K, Mg, Ca). Леткі метали – це метали, які під час горіння нагріваються вище температури кипіння, тобто метали з низькими температурами кипіння. У більшості випадків температура плавлення оксидів таких металів вища, ніж температура кипіння оксиду. В такому випадку на поверхні рідкого металу знаходиться тверда оксидна плівка. Пари металу проходять крізь оксидну плівку і в повітрі реагують з киснем. Зона горіння встановлюється поблизу поверхні металу. Більша частина тепла передається металу, і він починає кипіти. Кипіння викликає руйнування твердої оксидної плівки. Інтенсивність горіння збільшується. Поступово температура горіння збільшується і починає випаровуватися оксид, що знаходиться на поверхні металу. Це, в свою чергу, призводить до ще більшого зростання інтенсивності горіння. Пари оксиду, що виходять з зони горіння, – конденсуються та утворюють маленькі частки – дим. Утворення щільного білого диму є ознакою горіння летких металів.
Горіння нелетких металів (Ti, Be). Нелеткі метали – це такі метали, температура кипіння яких перевищує температуру плавлення оксидів, що утворюються на поверхні металу. При горінні таких металів їх оксиди знаходяться на поверхні металу в рідкому стані. Тиск пари над такими металами невеликий. Тому великі частки таких металів не горять. Але нелеткі метали горять у порошкоподібному стані, у вигляді тонкої стружки або аерозолю. Вони горять без утворення щільного білого диму.
Деякі метали можуть самозайматися за звичайних умов. В компактному стані самозаймаються рубідій і цезій. У подрібненому стані можуть займатися не тількі ативні метали (лужні та лужно-земельні), але і метали середьої активності (цинкова, магнієва, алюмінієва та залізна пудра). Метали, здатні самозайматися при контакті з киснем повітря за звичайних умов, називають пірофорними.
Приклад 40.
Який об'єм газу (н.у.) вилучиться при реакції 10 г міді з надлишком концентрованого розчину азотної кислоти?
Розв'язання.
1. При реакції концентрованої азотної кислоти з неактивними металами вилучається оксид азоту (ІV):
Cu + 4 HNO3 = Cu(NO3)2 + 2NO2 + 2H2O.
З рівняння реакції видно, що при реакції 1 молю міді вилучається 2 моля, або 222.4=44.8 л диоксиду азоту.
2. Визначимо кількість міді: n=m/A=10/63.5=0,16 моль.
3. Визначимо об'єм диоксиду азоту: V=0,1644.8=7.1 л.
Приклад 41.
Записати рівняння реакцій за допомогою яких можна здійснити такі перетворення:
NaNa2ONaOHNaBrNaNO3.
Для кожної речовини дати назву, вказати до якого класу неорганічних речовин відноситься кожна сполука. Для окисно-відновних реакцій написати електроні рівняння, для іонообмінних – іонні рівняння.
Розв'язання.
4Na + O22Na2O,
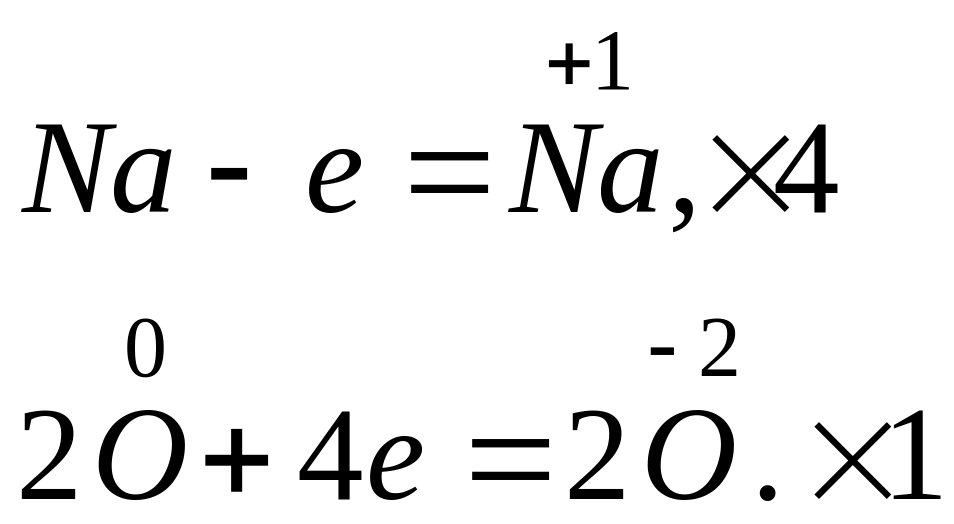
2. Na2O + H2O 2NaOH,
3. NaOH + HBr NaBr + H2O,
в іоному вигляді: Na++ OH– + H+ +Br – Na+ +Br – + H2O
в скороченому іоному вигляді: H+ + OH– H2O.
4. NaBr + AgNO3 NaNO3 + AgBr,
в іоному вигляді: Na++ Br – + Ag+ + NO3– Na+ + NO3– + AgBr,
в скороченому іоному вигляді: Ag+ + Br – AgBr.
Назви і класи сполук: Na – натрій, проста речовина – метал; Na2O – оксид натрію, клас – оксиди; NaOH – гідроксид натрію, клас – основи; NaBr – бромід натрію, клас – сіль; NaNO3 – нітрат натрію, клас – сіль.
Запитання для самоконтролю
Як змінюються металічні властивості в групах і періодах періодичної системи елементів?
Який елемент проявляє найбільші металічні властивості?
Які метали відносяться до лужних, лужноземельних, легких і важких конструкційних?
Які сполуки називаються гідридами?
Які метали відносяться до амфотерних?
Які існують методи добування металів?
Які метали найбільш поширені у земній корі?
Сформулюйте правила, які визначають можливість реакції металів з водою, кислотами та лугами?
Для гасіння яких металів не можна використовувати воду? Чому?
Які фактори впливають на горіння металів?
