
ГБОУ ВПО Тверская ГМА Минздрава России
Кафедра физики, математики и медицинской информатики
ИССЛЕДОВАНИЕ ПОВЕРХНОСТНОГО НАТЯЖЕНИЯ
Методические указания для лабораторной работы №5
Тверь 2014
Лабораторная работа
ИССЛЕДОВАНИЕ ПОВЕРХНОСТНОГО НАТЯЖЕНИЯ
ЦЕЛЬ РАБОТЫ:
Теоретически изучить явление поверхностного натяжения и методы определения коэффициента поверхностного натяжения (КПН).
Экспериментально освоить метод определения коэффициента поверхностного натяжения с помощью торсионных весов.
Экспериментально определить влияние примесей на коэффициент поверхностного натяжения.
Используя данные таблицы №1 определить влияние температуры на коэффициент поверхностного натяжения.
ПРИБОРЫ И ПРИНАДЛЕЖНОСТИ: торсионные весы с пластинкой Вильгельми, чашка Петри, дистиллированная вода, пинцет, глюкоза, мыльный раствор, пипетка, спиртовка, спички, термометр.
План занятия
Вводное слово преподавателя.
Собеседование по контрольным вопросам к лабораторной работе.
Выполнение лабораторной работы.
Оформление отчета по лабораторной работе.
Решение задач по теме лабораторной работы.
Информационный блок
На поверхности жидкости, вблизи границы, разделяющей жидкость и ее насыщенный пар, молекулы испытывают межмолекулярное взаимодействие не такое, как молекулы, находящиеся внутри жидкости.
Радиус сферы молекулярного действия приблизительно равен полутора диаметрам молекулы (радиус самих молекул приблизительно составляет 510-8 см). Следовательно, каждая молекула жидкости взаимодействует только с непосредственно прилегающими к ней соседними молекулами.
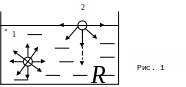
Молекула
1 на рис.1 расположена внутри жидкости,
со всех сторон ее окружает в среднем
одинаковое число молекул той же жидкости,
поэтому результирующая сил притяжения
![]() ,
действующих на молекулу, в среднем равна
нулю.
,
действующих на молекулу, в среднем равна
нулю.
Иначе обстоит дело с молекулой 2 на рис.1, лежащей на поверхности жидкости. Так как концентрация молекул, в расположенном над жидкостью газе, мала по сравнению с концентрацией молекул внутри жидкости, то равнодействующая сил, действующих на молекулу, оказывается не равной нулю и направленной внутрь жидкости перпендикулярно ее поверхности. В таком же положении находятся все молекулы, лежащие в поверхностном слое жидкости толщиной в радиус молекулярного действия. Это приводит к молекулярному давлению, которое производит поверхностный слой на жидкость.
Под действием сил молекулярного взаимодействия часть молекул с поверхностного слоя переходят в глубь жидкости. Расстояния, а значит и силы притяжения, между оставшимися на поверхности молекулами увеличиваются. Напряженное состояние поверхностного слоя жидкости называется поверхностным натяжением; оно вызвано силами взаимодействия между молекулами этого слоя.
Для того чтобы обнаружить действие сил поверхностного натяжения, проведем следующий опыт. «Натянув» на проволочную рамку пленку мыльной воды, положим на нее петлю (контур) из тонкой нитки (рис. 2) и затем проткнем пленку внутри петли (рис. 3). Под действием силы поверхностного натяжения, со стороны сохранившейся (внешней) части пленки, контур немедленно растянется, приняв форму окружности, так как длина периметра окружности имеет наименьшее значение при одинаковых площадях геометрических фигур
.
Силы поверхностного натяжения направлены вдоль поверхности, перпендикулярно любому контуру на этой поверхности и стремятся уменьшить величину поверхности жидкости.
Сумма сил притяжения, действующих на контур, ограничивающий поверхность жидкости, силой поверхностного натяжения поверхностного натяжения F. Эта сила пропорциональна числу молекул, прилегающих к контуру, которое, в свою очередь, пропорционально длине контура l; следовательно,
![]() (1)
(1)
где σ – коэффициент поверхностного натяжения.
Из формулы (1) следует, что
![]() ,
(2)
,
(2)
 т.е.
коэффициент
поверхностного натяжения жидкости
равен силе поверхностного натяжения,
действующей на единицу длины контура,
ограничивающего поверхность жидкости.
Измеряется
в Н/м. Если
погрузить в мыльную воду проволочный
каркас, а затем вынуть, то он затянется
мыльной пленкой. Пленка сразу же начнет
сокращаться и потянет за собой кверху
легкую подвижную перекладину с двумя
колечками а-а
(рис. 4). При сокращении поверхности
жидкости ее потенциальная энергия
уменьшается, так как молекулярные силы
сами совершают работу по затягиванию
«лишних» молекул с поверхности в глубь
жидкости.
т.е.
коэффициент
поверхностного натяжения жидкости
равен силе поверхностного натяжения,
действующей на единицу длины контура,
ограничивающего поверхность жидкости.
Измеряется
в Н/м. Если
погрузить в мыльную воду проволочный
каркас, а затем вынуть, то он затянется
мыльной пленкой. Пленка сразу же начнет
сокращаться и потянет за собой кверху
легкую подвижную перекладину с двумя
колечками а-а
(рис. 4). При сокращении поверхности
жидкости ее потенциальная энергия
уменьшается, так как молекулярные силы
сами совершают работу по затягиванию
«лишних» молекул с поверхности в глубь
жидкости.
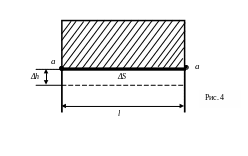
Пусть перекладинка длиной l поднялась на h ,при этом пленка совершила работу:
А = mgh
где т- масса перекладинки. К каждой точке перекладинки приложена сила поверхностного натяжения, направленная вверх. Так как мыльная пленка имеет две поверхности, то вся сила, действующая на перекладинку:
F=2l (3)
Работа, совершенная пленкой:
A=2lh (4)
![]() (5)
(5)
где
![]() -
изменение площади поверхности мыльной
пленки.
-
изменение площади поверхности мыльной
пленки.
![]() (6)
(6)
Можно дать еще одно определение коэффициента поверхностного натяжения.
Коэффициентом поверхностного натяжения жидкости называется работа, совершаемая при изотермическом изменении площади поверхности на единицу площади.
Но работа есть мера перехода одного вида энергии в другой или мера перехода энергии от одного тела к другому. В данном случае увеличится потенциальная энергия поднятой перекладинки.
Таким образом, сила поверхностного натяжения, приложенная к перекладинке. осталась прежней, а энергия пленки уменьшилась на величину:
2lh = 2S [Дж ] (7)
Уменьшилась и поверхность на величину
2lh = 2S [м2] (8)
Разделив (7) на (8), получим:
![]()
![]()
Видно, что коэффициент поверхностного натяжения может измеряться и как энергия, приходящаяся на единицу площади поверхности пленки, и как сила, действующая на единицу длины контура пленки. Противоречия в размерностях
![]()
Если мы увеличиваем поверхность жидкости, то мы совершаем работу, преодолевая силу молекулярного давления, при этом энергия поверхности жидкости увеличивается.
Коэффициент поверхностного натяжения у разных жидкостей различен: σ - одна из физических констант, по которым может быть установлена неизвестная жидкость.
Для чистых жидкостей σ зависит от:
природы жидкости (таблица 1),
температуры (уменьшается с ростом температуры),
давления газа на границе жидкость-газ (уменьшается при увеличении давления газа).
Для растворов σ еще зависит от:
природы растворенного вещества,
концентрации растворенного вещества.
Таблица 1. Поверхностное натяжение некоторых жидкостей на границе с воздухом.
Жидкость |
Температура, |
Коэффициент поверхностного натяжения σ, [Н/м] |
Ацетон |
20 |
0,0237 |
Метиловый спирт |
20 |
0,0226 |
Глицерин |
20 |
0,0634 |
Ртуть |
15 |
0,487 |
Мыльный раствор |
20 |
0,025 |
Желчь |
20 |
0,048 |
Сыворотка крови |
20 |
0,06 |
Моча |
20 |
0,066 |
Вода |
0 |
0,0756 |
Вода |
20 |
0,0728 |
Вода |
30 |
0,0712 |
Вода |
100 |
0,0588 |
Поверхностно-активными веществами (ПАВ) называются растворенные вещества, понижающие σ растворителя.
Если при растворении твердого или жидкого вещества в жидком растворителе силы притяжения между молекулами растворенного вещества и растворителя меньше сил притяжения между молекулами растворителя, то такие растворенные вещества называются поверхностно-активными. К ним принадлежит мыло при растворении в воде, ряд жирных кислот, желчь, спирты, белки и многие другие. Так как молекулы растворенного вещества притягиваются молекулами растворителя слабее, чем молекулы растворителя, то из поверхностного слоя внутрь жидкости преимущественно втягиваются молекулы растворителя, и в поверхностном слое увеличивается концентрация молекул растворенного вещества, уменьшая тем самым поверхностное натяжение раствора. Равновесие наступает тогда, когда число молекул растворенного вещества, втягиваемых из поверхностного слоя вглубь жидкости, будет равняться числу молекул, приходящих вследствие диффузии из глубинных слоев на поверхность. Поверхностный слой оказывается обедненным молекулами растворителя и обогащенным молекулами растворенного вещества. Это явление носит название адсорбции. Им объясняется устойчивость жидких пленок, пены и т.д.
Очень многие биологические соединения оказывают существенное влияние на поверхностное натяжение, то есть являются поверхностно-активными. Так нормальное функционирование легочных альвеол обеспечивается наличием в них специальных поверхностно-активных соединений сурфактантов. Важную роль играют такие вещества в пищеварении. Например, способность желчи содействовать перевариванию жиров зависит не только от ее химического воздействия. Желчные кислоты по отношению к жирам являются ПАВ: уменьшая поверхностное натяжение капель жира, они делают возможным раздробление их на значительно более мелкие; в результате поверхность соприкосновения ферментов с пищевыми веществами возрастает во много раз, и соответственно увеличивается скорость переваривания.
Поверхностно-неактивными веществами (ПНВ) называются вещества растворы, которых практически не изменяют σ растворителя.
По отношению к воде ПНВ является сахароза.
Поверхностно-инактивными веществами (ПИВ) называются вещества растворы, которых незначительно повышают σ растворителя.
По отношению к воде ПИВ являются кислоты, щелочи, соли.
Измерение КПН водных растворов поверхностно-активных веществ является наиболее чувствительным методом определения их концентрации в растворе. Методы измерения КПН подразделяются на статические (при неподвижных или медленно образующихся поверхностях раздела) и динамические (при движущихся и непрерывно обновляющихся поверхностях раздела). Динамические методы, основанные на применении измерений размеров колеблющихся струй и капель, практически не применяются из-за своей сложности. Используемый в данной работе метод относится к статическим методам.
