
Приложение к практическому занятию №4.
Расчет материального баланса
Расчёт ведём на 1 тонну, а затем на производительность
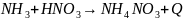
Определяем статьи прихода
1.Расчитываем теоретические расходные коэффициенты

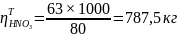
2.Расчитываемпрактические расходные коэффициенты
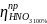 =787,5
=787,5 1,01=795,4
кг
1,01=795,4
кг
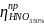 =795,4/0,5=1590,8
кг
=795,4/0,5=1590,8
кг
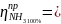 212,5
1,01=214,6 кг
212,5
1,01=214,6 кг
3. Находим общее количество реагентов, поступающих в аппарат
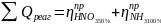 ,
,
где
 -
практические расходные коэффициенты,
кг
-
практические расходные коэффициенты,
кг
 =214,6+1590,8=1805,4
кг
=214,6+1590,8=1805,4
кг
4. Рассчитываем потери
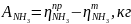
где
 -
практический расходный коэффициент,
кг
-
практический расходный коэффициент,
кг
 -
теоретический расходный коэффициент,
кг
-
теоретический расходный коэффициент,
кг
 =214,6-212,5=2,1
кг
=214,6-212,5=2,1
кг
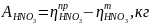
 =795,4-787,5=7,9
кг
=795,4-787,5=7,9
кг
Определяем статьи расхода
5. Определяем общее количество раствора
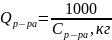
где
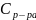 -
концентрация получавшегося раствора,
%
-
концентрация получавшегося раствора,
%
 =1000/0,7=1428,6
кг
=1000/0,7=1428,6
кг
6. Определяем количество сокового пара
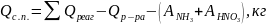
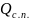 =1805,4-1428,6-(2,1+7,9)=366,8
кг
=1805,4-1428,6-(2,1+7,9)=366,8
кг
7. Находим общее количество продуктов, выходящих из аппарата

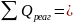 1428,6+366,8+(2,1+7,9)=1805,4
кг
1428,6+366,8+(2,1+7,9)=1805,4
кг
8. Составляем таблицу материального баланса
Таблица 1-Материальный баланс
Приход |
Расход |
||||||
Статьи |
кг |
м3 |
П |
Статьи |
кг |
м3 |
П |
Аммиак Азотная кислота в том числе потери: Аммиака Азотной кислоты
Итого |
214,6 1590,8 2,1 7,9
1805,4 |
|
|
70%-ный раствор амми- ачной селитры Соковый пар Потери: Аммиака Азотной кислоты Итого |
1428,6
366,8
2,1 7,9 1805,4 |
|
|
Расчет теплового баланса.
Определяем статьи прихода.
1.Определяем количество теплоты, приходящее с азотной кислотой
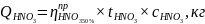
где - практический расходный коэффициент HNO3, кг
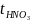 - температура
HNO3,0С
- температура
HNO3,0С
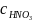 -
теплоемкость HNO3,
кДж/кг*К
-
теплоемкость HNO3,
кДж/кг*К
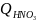 =1590,8
=1590,8 30
2,763=131861,4
кДж
30
2,763=131861,4
кДж
 =214,6
50
2,186=23455,8
кДж
=214,6
50
2,186=23455,8
кДж
Для этого согласно реакции по графику находим, что для 50% HNO3 количество теплоты нейтрализации будет 105,09
Qр-ции=
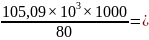 1313625
кДж
1313625
кДж
4. Находим общее количество приходящей теплоты

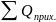 =23455,8+131861,4+1313625=1468942,2
кДж
=23455,8+131861,4+1313625=1468942,2
кДж
Определяем статьи расхода.
5. Определяем количество теплоты, уходящее с раствором
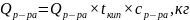
где - общее количество раствора, кг
 -
температура кипения раствора, 0С
-
температура кипения раствора, 0С
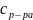 -
теплоемкость раствора, кДж/кг*К
-
теплоемкость раствора, кДж/кг*К
=1428,6 2,303 123,6=406652,1 кДж
6. Определяем количество теплоты, уходящее с соковым паром
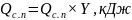
где
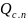 -
общее количество сокового пара, кг
-
общее количество сокового пара, кг
 -
энтальпия, кДж
-
энтальпия, кДж
=366,8 2684=984491,2 кДж
7. Определяем общее количество уходящей теплоты
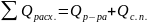 ,
кДж
,
кДж
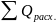 =406652,1+984491,2=131143,3
кДж
=406652,1+984491,2=131143,3
кДж
8. Определяем теплопотери
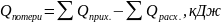
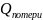 =1468942,2-131143,3=77798,9
=1468942,2-131143,3=77798,9
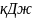
Теплота потери может быть рассчитана как разница между статьями прихода и расхода, прибавляются к статьям расхода, либо рассчитываются до 4% от суммы статей прихода.
9.Составляем таблицу теплового баланса
Таблица 2 – тепловой баланс
Приход |
Расход |
|||||||
Статьи |
кДж |
МДж |
П |
Статьи |
кДж |
МДж |
П |
|
Количество азотной кислоты Количество аммиака в том числе: Теплопотери Количество теплоты реакции |
131861,4
23455,8
77798,9 1313625 |
|
|
Количество 70%-ного раствора аммиачной селитры Количество сокового пара Теплопотери:
|
406652,1
984491,2
77798,9 |
|
|
|
Итого |
1468942,2 |
|
|
Итого |
1468942,2 |
|
|
|
