
- •Якісний аналіз
- •Методи якісного аналізу
- •Хімічні фізико-хімічні Фізичні
- •Класифікація методів якісного аналізу
- •Макрометод мікрометод напівмікрометод
- •Умови проведення аналітичних реакцій
- •Способи виконання аналітичних реакцій
- •Хід аналізу
- •Кислотно – лужна класифікація катіонів
- •Класифікація аніонів
- •Використання неорганічних речовин у медицині
- •Домішки в лікарських препаратах
- •Кількісний аналіз
- •Методи кількісного аналізу хімічні фізико-хімічні фізичні
- •Суть титриметричного аналізу
- •Методи титриметрії
- •Вимоги до хімічних реакцій
- •Способи титрування
- •Види робочих розчинів
- •Вимоги до первинних стандартів
- •Способи відбору проб для титрування
- •Розрахункові формули в титриметричному аналізі
- •Кислотно – основне титрування (метод нейтралізації)
- •2) Протофільні (основні):
- •3) Амфіпротні (амфотерні) :
- •Окисно – відновні реакції
- •Окисно – відновне титрування (оксидиметрія)
- •Перманганатометрія
- •Йодометрія
- •Броматометрія
- •Нітритометрія
- •Методи осадження
- •Аргентометрія
- •Метод Мора
- •Метод Фаянса
- •Тіоцианометрія (метод Фольгарда)
- •Комлексонометрія
- •Інструментальні методи
- •Рефрактометрія
- •Фотометрія
- •Фотоколориметрія
- •Хроматографія
- •Паперова хроматографія
- •Іонообмінна хроматографія
Хроматографія
це метод розділення й аналізу сумішей за допомогою сорбційних процесів. Метод ґрунтується на різному розподілі компонентів суміші між двома фазами – рухомою та нерухомою.
Сорбент – це нерухома фаза:
тверді речовини: Al2O3, SiO2, силікагель, крохмаль, іоніти;
рідкі речовини – нерухомі розчинники, що утримуються носіями (наприклад, вода в порах хроматографічного паперу).
Носії нерухомих розчинників – хроматографічний папір, спеціальні пластини.
Сорбат – це рухома фаза (потік рідини , що фільтрується крізь шар сорбенту.
Класифікація хроматографічних методів:
за механізмом розділення сумішей:
адсорбційна хроматографія – ґрунтується на принципі розділення суміші речовин за різною силою зв’язків, що утворюються між молекулами речовин та сорбентом. Чим слабкіші зв’язки, тим швидше рухається речовина крізь нерухому фазу;
молекулярна (розподільна) хроматографія – ґрунтується на принципі розділення за розмірами молекул. Крізь пори нерухомої фази можуть дифундувати тільки речовини, розміри молекул яких не перевищують розміри пор. Внаслідок цього молекули меншого розміру проходять більший шлях і пізніше виходять з колонки, ніж великі молекули;
осадова хроматографія – ґрунтується на утворенні малорозчинних сполук між речовинами суміші та осаджувачем, що знаходиться в порах сорбенту. Чим більша розчинність, тим швидше речовина вимиється з сорбенту;
іонообмінна хроматографія – ґрунтується на обміні іонів між досліджуваною речовиною та сорбентом.
за технікою виконання:
колоночна;
паперова;
тонкошарова;
капілярна.
Паперова хроматографія
Як носій нерухомої фази використовується хроматографічний папір, який утримує в своїх порах воду – нерухомий розчинник. На папір наносять краплю досліджуваного розчину. При обробці паперу рухомим розчинником нанесені речовини рухаються по капілярам паперу з різними швидкостями, утворюючи хроматографу. Хроматографування закінчують, коли розчинник досягає лінії фінішу. Папір висушують та обприскують розчином відповідного проявника (кольорова реакція).

лінія фінішу


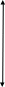
L


ℓ

лінія старту
L – відстань, яку пройшов розчинник
ℓ – відстань від лінії старту до центру плями
ℓ
Rf
=
L
х роматографічна
рухомість (індивідуальна характеристика
речовини)
роматографічна
рухомість (індивідуальна характеристика
речовини)
Аналіз суміші проводять на одному аркуші паперу з відомими речовинами – „свідками”:
1 2 3




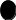

 ℓ2
ℓ2


ℓ1


1 та 2 – „свідки”
3 – суміш речовин
