
Ъ
.docxРоссийский химико-технологический университет им. Д.И.Менделеева
Кафедра общей химической технологии
Лабораторная работа
«Окисление SO2 в SO3»
Выполнили студенты К-41
Головкина А. И.
Кубарев П. М.
Эбергард А. В.
Москва 2019
Цель работы
Изучение основных закономерностей гетерогенно-каталититического процесса с обратимой экзотермической реакцией на примере окисления диоксида серы.
Анализ и выбор оптимальных условий функционирования химико-технологической системы.
Этапы исследования
-
Определение равновесной степени превращения
-
Определение скоpостиpеакции W(T) пpи заданном X
-
Определение оптимальной темпеpатуpыTоpt (X)Определение вpемени контакта в слое t (X) (pежимы ИС и ИВ)
Расчетная часть
-
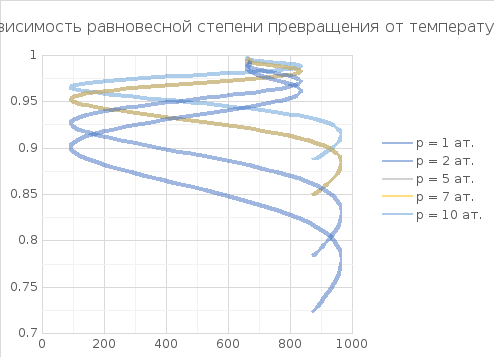
Рассчитываем равновесные данные для нашего процессапри разных давлениях
С (SO2) = 0,1 мол. д.
С (O2)= 0,11 мол. д.
В интервале температур: от 673 до 873 К
Шаг = 40
-
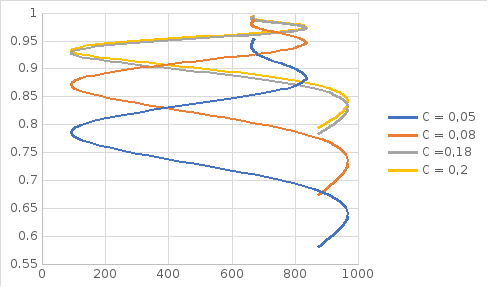
Рассчитываем равновесные данные для нашего процесса при разных концентрациях О2
-
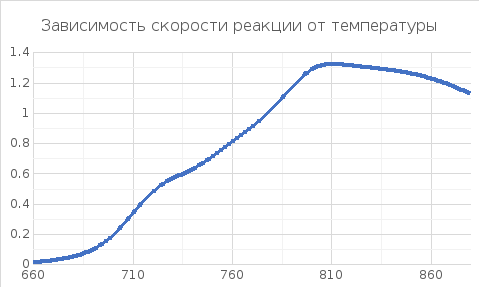
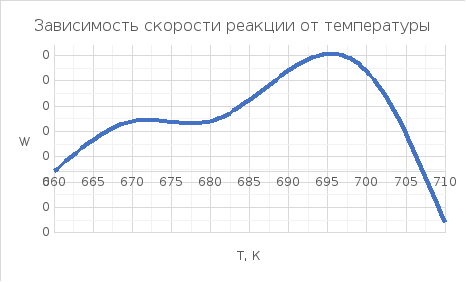
Рассчитываем скорость реакции при заданной степени превращения
С (SO2) = 0,1 мол. д.
С (O2)= 0,11 мол. д.
Р = 1 ат.
В интервале температур: от 660 до 890 К
Шаг = 20
-
Х = 0,5м.д.
|
Т, К |
W (X,T) |
|
660 |
0,014 |
|
680 |
0,054 |
|
700 |
0,196 |
|
720 |
0,483 |
|
740 |
0,631 |
|
760 |
0,812 |
|
780 |
1,03 |
|
800 |
1,287 |
|
820 |
1,314 |
|
840 |
1,284 |
|
860 |
1,229 |
|
880 |
1,132 |
-
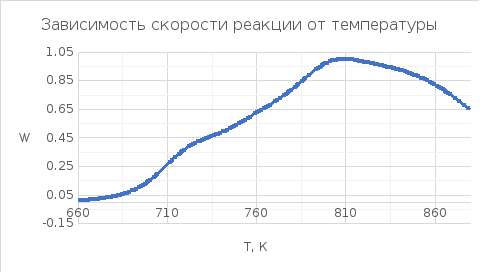
Х = 0,6
|
Т, К |
W (X,T) |
|
660 |
0,011 |
|
680 |
0,042 |
|
700 |
0,152 |
|
720 |
0,373 |
|
740 |
0,487 |
|
760 |
0,626 |
|
780 |
0,791 |
|
800 |
0,979 |
|
820 |
0,982 |
|
840 |
0,926 |
|
860 |
0,825 |
|
880 |
0,647 |
-
Х = 0,7
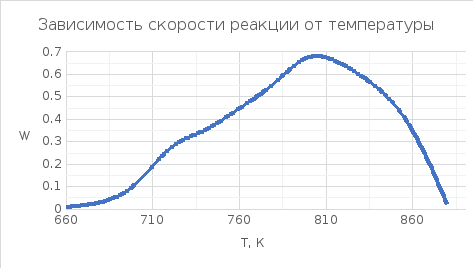
|
Т, К |
W (X,T) |
|
660 |
0,008 |
|
680 |
0,03 |
|
700 |
0,11 |
|
720 |
0,269 |
|
740 |
0,351 |
|
760 |
0,448 |
|
780 |
0,559 |
|
800 |
0,675 |
|
820 |
0,642 |
|
840 |
0,538 |
|
860 |
0,35 |
|
880 |
0,019 |
-
X = 0,8
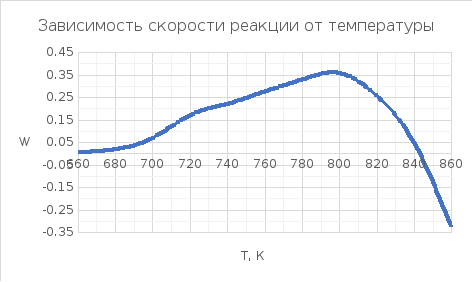
|
Т, К |
W (X,T) |
|
660 |
0,005 |
|
680 |
0,019 |
|
700 |
0,07 |
|
720 |
0,171 |
|
740 |
0,221 |
|
760 |
0,276 |
|
780 |
0,329 |
|
800 |
0,358 |
|
820 |
0,258 |
|
840 |
0,049 |
|
860 |
-0,328 |
-
Х = 0,9
Шаг = 10
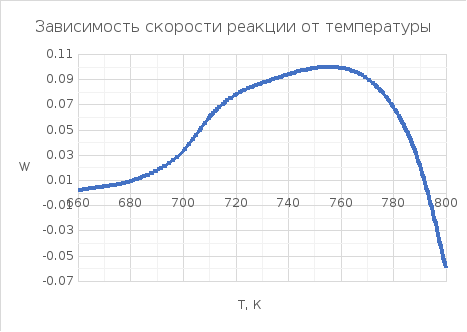
|
Т, К |
W (X,T) |
|
660 |
0,002 |
|
670 |
0,005 |
|
680 |
0,009 |
|
690 |
0,018 |
|
700 |
0,033 |
|
710 |
0,06 |
|
720 |
0,078 |
|
730 |
0,087 |
|
740 |
0,094 |
|
750 |
0,099 |
|
760 |
0,099 |
|
770 |
0,091 |
|
780 |
0,068 |
|
790 |
0,022 |
|
800 |
-0,06 |
-
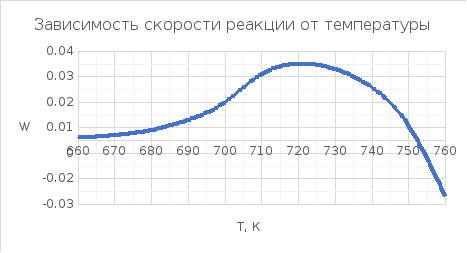 Х
= 0,95
Х
= 0,95
|
Т, К |
W (X,T) |
|
660 |
0,001 |
|
670 |
0,002 |
|
680 |
0,004 |
|
690 |
0,008 |
|
700 |
0,015 |
|
710 |
0,026 |
|
720 |
0,03 |
|
730 |
0,028 |
|
740 |
0,021 |
|
750 |
0,006 |
|
760 |
-0,022 |
-
Х = 0,95
|
Т, К |
W (X,T) |
|
660 |
0 |
|
670 |
0,001 |
|
680 |
0,001 |
|
690 |
0,002 |
|
700 |
0,002 |
|
710 |
-0,001 |
-
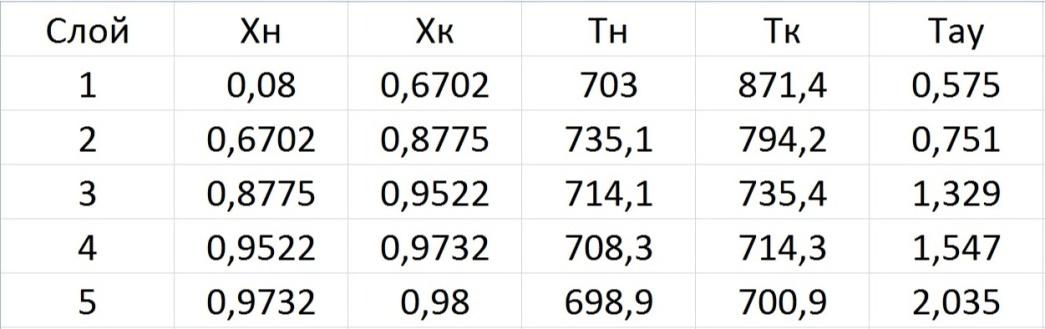
Рассчитаем оптимальные параметры для каждого слоя катализатора:
Режим идеального вытеснения с промежуточными теплообменниками
Катализатор: БАВ
С (SO2) = 0,1 м. д.
С (O2) = 0,11 м. д.
Р = 1 ат.
Т ад. = 285,3 К
n = 3
Xн = 0,08 м.д.
Тн = 703 К
Хк = 0,98 м. д.
|
слой |
Хн |
Хк |
Тн |
Тк |
τ |
|
1 |
0,08 |
0,6702 |
708 |
871,4 |
0,575 |
|
2 |
0,6702 |
0,8775 |
735 |
794,2 |
0,751 |
|
3 |
0,8775 |
0,9522 |
714 |
735,4 |
1,329 |
|
4 |
0,9522 |
0,9732 |
708 |
714,3 |
1,547 |
|
5 |
0,9732 |
0,98 |
698 |
700,9 |
2,035 |
|
|
|
|
|
|
6,237 |
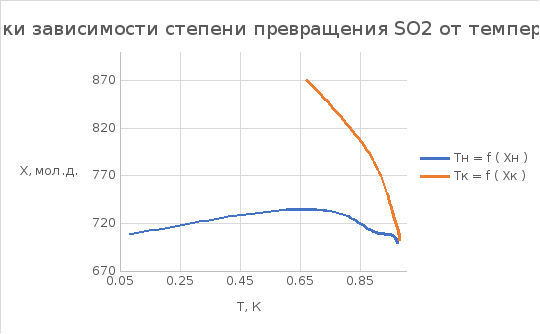
Тн – температура на входе в реактор
Тк – температура на выходе из реактора
Хн – степень превращения на входе в реактор
Хк - степень превращения на выходеиз реактора
τ – время контакта в слоях
-
Рассчитаем оптимальные параметры для каждого слоя катализатора:
Реактор идеального вытеснения с промежуточными теплообменниками и вводом холодного газа после 1-го слоя
Катализатор: БАВ
Т х.г. = 473 К
|
слой |
Хн |
Хк |
Тн |
Тк |
τ |
V |
|
1 |
0,08 |
0,6661 |
703 |
870,2 |
0,334 |
0,592 |
|
2 |
0,3943 |
0,8112 |
708,1 |
827,1 |
0,787 |
1 |
|
3 |
0,8112 |
0,9408 |
712,6 |
749,6 |
1,428 |
1 |
|
4 |
0,9408 |
0,9719 |
707,3 |
716,2 |
1,767 |
1 |
|
5 |
0,9719 |
0,98 |
699,5 |
701,9 |
2,287 |
1 |
|
|
|
|
|
|
6,603 |
|
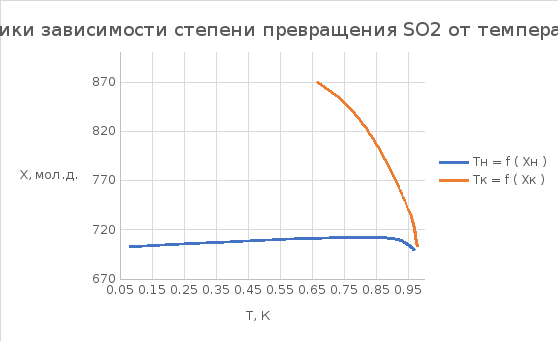
МНОГОСЛОЙНЫЙ РЕАКТОР ОКИСЛЕНИЯ SO2 с промежуточными теплообменниками
Оптимизация: Режим процесса в слое - РИВ Концентрации (доли): SO2 = 0,1 O2 =0,11 P = 1 ат Адиабатический разогрев Тад. = 285,3 Число слоёв катализатора n = 5 Условия процесса: Хн = 0,08 Тн= 703 Хк = 0,98
G(H2SO4)треб.
= 540
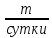 =
=
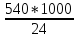 = 22500
= 22500
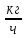
При n = 5 Xк= 0,98
G(SO2)=
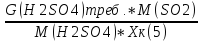 =
=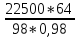 = 15000
= 15000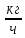
В целях энерего- и ресурсосбережения возьмём модель каскадного реактора, работающая по методу ДК/ДА - двойное контактирование - двойная абсорбция. Для неё примем Хк = 0,99.
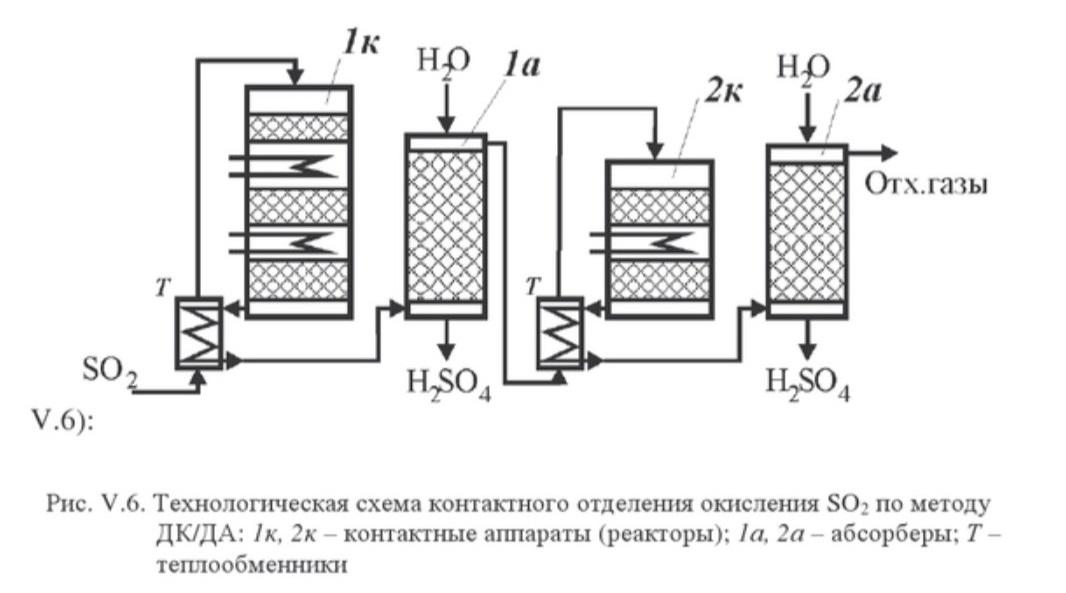
G(SO2)0,99
=
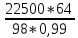 = 14840
= 14840
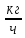
G(O2)
=
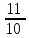 * 14840 = 16300
* 14840 = 16300
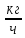
G(N2)
=
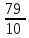 * 14840 = 117240
* 14840 = 117240
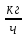
Х1 = 0,9522 - степень превращения 1-ого контактного аппарата; X2 - второго
Xобщ.
= 0,99 = Х1
+ X2
- Х1
*
X2
= 0,9522 + X2
- 0,9522 * X2
;
X2
= 0,99 - X1
+ X1
*
X2
= 0,99 - 0,9522 + 0,9522 * X2
=
0,04 + 0,95 * X2;
0,0378
= X2
* (1 - 0,9522) ;
X2
=
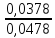 = 0,79.
= 0,79.
Выводы:
1)Понижение температуры повышает равновесную степень превращения и константу равновесия.
2)Оптимальная температура снижается с ростом степени превращения.
3) Суммарное время контакта растёт с увеличением степени превращения.
