
Теплоёмкость
называется отношение кол-ва теплоты поглощаемое или выделяемое системой при охлождении или нагревании к изменению температуры. Теплоёмкость к массе вещества называется удельной (г/К), к массе атома атомной теплоёмкостью, к молю молярной
В зависимости от условий различают Изохорную (CV) и изобарную(CP). При изохорном вся теплота уходит на изменение внутренней энергии. Изобарный часть энергии расходуется на внутреннюю энергию, а другая на работу против внешнего давления. По этой причине теплоёмкость при CP>CV на величину работы затраченной на совершение работы. CV=CP+A
Если мы совершаем работу против внешнего давления 1 моль идеального газа R=8.31 КДж/К
CP-CV=R=8.31. Различают среднюю и истинную теплоёмкость
Ссред=Q/(T2-T1)
Систи=δQ/dT


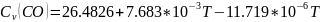





R=8.31
находим как разность между теплоёмкостями как алгебр сумму теплоёмкостей участвующих в реакции веществ

теперь подставим в эти значения Т 298+1000=1298
 (у препода -7,661)
(у препода -7,661)
средняя теплоёмкость относится к 0 град цельсия поэтому необходимо рассчитать теплоёмкость при Т-298

находим ΔCp от298 до 1298

рассчитать тепловой эффект реакции
1/2N2г+3/2 N2г=NH3
при постоянном
давлении и 1000К, если его значение при
стандарт усл 46,191КДж/Моль
46,191КДж/Моль

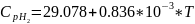

Влияние температуры на энтропию.
ΔS=ΔH/T
dS=d ΔH/T
ΔS=S2-S1=
если перейти к изохорной теплоёмкости то формула видоизменится
опред изменение энтропии моля NaCl при нагревании от 25 до 820. Его температура плавления 8000

при Т плавления и выше Cр при 800=66.55 Дж/Моль

изменение энтропии от 25 до 800 цельсия будет равнятся

так как Ср от 0 до 800 то мы теплоёмкость берём с поправкой

рассчитаем изменение энтропии в интервале температур от 800 до 820

суммарное изменение интервала

удельная
теплота плавления Fe
 0,2695Дж/гр
0,2695Дж/гр
от298К 15390 тампер плавления. найти изменении энтропии при плавлении 2 кг Fe
Черчение Графика на миллимитровом листе А4 сложенном попалам , с краёв отступить 2е большие клетки
зависимость пара над жидкостью изображается
ИЗучение равновесия между чистым веществом и давлением насыщенного пара изучается с помощью зависимости Pt
Пар в равновесии с жидкостью называется насыщенным паром. Такая зависимость давления насыщенного пара изображается кривой испарения. Каторая в низу ограниченна областью метастабильного состояния переохлаждённой жидкости, а вверху критической точкой. В случае твёрдого состояния повышение температуры также увеличивает давление насыщенного пара и зависимости Pt близки. Однако возможен переход из твёрдого состояния в пар. В этом случае эту кривую называют кривой сублимации или возгонки. В этом случае кривая ограниченна точкой плавления твёрдого вещества.
Для изучения
диаграмм состояния различных веществ
например 2х фаз используют уравнение
Клаперона-Клаузиуса, которое характеризует
равновесие 2х фаз

Н – теплота фазового перехода при P и t
 - мольные объёмы при усл что t2>t1
- мольные объёмы при усл что t2>t1
Применительно к жидкости ΔН испарения или к твёрдому веществу ΔН возгонки. Уравнение Клаузеуса-Клайперона позволяет сделать вывод:
Если фазовый перпеход сопровождается изменением ΔН>0, ΔV>0 , или ΔН<0, ΔV<0 то при увеличении давления температура превращения одной фазы в другую возрастает. Испарение, Сублимация, Возгонка, Кристаллизация подавляющего большинства чистых веществ.
ΔН<0 ΔV>0, ΔН>0 ΔV<0, то такие случаа характерны для плавления льда, галлия и висмута и некоторых сортов чугуна.
В тройной точке находятся в равновесии лёд, жидкость и пар (рис1). В однофазном состоянии система бивариантна (к=1 и число фаз с=к+2-ф). По линии АК и по линии АС происходят процессы кипения и возгонки сопровождающиеся изменением температуры и давления. Пр и понижении температуры происходит конденсация пара переход сначала в жидкую а потом в твёрдую фазу. Точка к (кипение) давление насыщенного пара равно внешнему давлению. Линия 3 указывает на переход твёрдой фазы в жидкую. Объём твёрдой фазы меньше жидкой.
