
4. Деградация и загрязнение почв
Деградация почв происходит в результате их прямого разрушения, главным образом при ведении различных строительных работ и добыче полезных ископаемых, а также вследствие развития эрозионных процессов преимущественно на пахотных угодьях. Для торфяных почв в случае их использования под пашню характерна ускоренная минерализация органического вещества.
Прямое разрушение почвенного покрова в связи с ведением строительных работ и добычей полезных ископаемых, так же как и в предыдущем году, не отличалось интенсивностью. Площадь нарушенных земель в стране продолжала сокращаться. По сравнению с 2006 г., она уменьшилась на 3,7% и составила 5,2 тыс.га. Причем половина из этой площади приходится на Минскую область и 29% на Брестскую.
Эродированные почвы охватывают примерно десятую часть пахотных земель. Деградированные торфяные -- почти четверть общей площади торфяных почв, используемых в сельском хозяйстве. Более 2/3 торфяных почв пахотных земель относятся к маломощным (с мощностью торфа до 1 м).
Наряду с развитием эрозионных процессов в Беларуси проявляются и такие негативные изменения почв, как снижение их плодородия из-за недостаточного внесения удобрений. Подобные изменения отмечаются примерно в половине районов страны.
Химическое загрязнение почв имеет место преимущественно в городах и зонах их влияния, в придорожных полосах транспортных магистралей, в зонах влияния полигонов складирования отходов, в местах нефтедобычи и на сельскохозяйственных землях.
В городах основными загрязнителями почв выступают нефтепродукты и тяжелые металлы и, в меньшей степени, -- сульфаты. Среди тяжелых металлов ведущая роль принадлежит кадмию, свинцу и цинку.
Проблемы новых вирусных инфекций (на примере ВИЧ, гепатита, герпесвирусов).
Новые вирусы: ВИЧ, гепатита С, гепатита GB, герпесвирусы 6, 7, 8, атипичной пневмонии, их характеристика и вызываемы ими заболевания.
Вирус иммунодефицита человека относится к ретровирусам, и для него характерны все особенности жизненного цикла вирусов данного семейства. Геном ВИЧ представлен одноцепочечной молекулой РНК. В инфицированной клетке с помощью вирусного фермента – обратной транскриптазы (ревертазы) – на матрице вирусной РНК синтезируется двухцепочечная молекула ДНК, которая затем встраивается в какой-либо участок одной из хромосом клетки-хозяина. Интегрированная ДНК-копия ретровирусного генома называется провирусом. В таком состоянии ретровирус может долгое время сосуществовать с инфицированным организмом, никак себя не проявляя. Однако, получив определенные молекулярные сигналы, с провирусной ДНК инициируется транскрипция вирусной РНК, а с нее – синтез вирусных белков. Затем следуют сборка многочисленных вирусных частиц и выход их из клетки, приводящий в итоге к гибели зараженных клеток. Отличительное свойство ВИЧ прояется в том, что он адсорбируется на поверхности только тех клеток, которые содержат мембранный белок, называемый антигеном CD4. Такой поверхностный антиген в основном содержат T4-лимфоциты, являющиеся T-хелперами/индукторами (хелпер от англ. helper – помощник) и играющие важнейшую роль в координации работы всей иммунной системы человека. Уничтожение вирусом лимфоцитов этого типа и обусловливает иммуносупрессорное действие ВИЧ.
До недавнего времени считалось, что вирусы ОРЗ, гепатита C и ВИЧ относятся к разным группам. Пол Элквист и его коллеги из Университета Висконсин–Мэдисон детально исследовали эти патогены и пришли к выводу, что все они произошли от одного предка.
О родстве патогенов свидетельствует cходство в строении белковых оболочек вирусных частиц. К тому же, у всех этих вирусов аналогичный механизм репликации – т.е. копирования новых частиц. Выявление общих черт наиболее распространенных в мире вирусов может привести к созданию высокоэффективных лекарственных препаратов нового поколения.
Тестирование ВИЧ-инфекции. Большинство вирусных инфекций (например, грипп, ветряная оспа) развиваются быстро, и врач их идентифицирует прежде всего по клиническим проявлениям у больного. В случае ВИЧ-инфекции такой подход неприменим, так как ее внешние проявления могут наблюдаться лишь спустя месяцы и годы после заражения. Поэтому всеобщее распространение получил метод обнаружения в крови человека антител к вирионным белкам ВИЧ. Первые варианты такого метода – метода иммуноферментного анализа (ИФА) были разработаны уже в 1984 г.
Метод ИФА используют для массовых обследований. В случае положительного результата обязательно выполняют дополнительные анализы методически независимыми способами, обеспечивающие достоверность результатов. В частности, для выявления провирусной ДНК в клетках крови используется более чувствительный метод полимеразной цепной реакции (ПЦР).
Стадии развития ВИЧ-инфекции. Разработка методов тестирования и многолетние наблюдения за ВИЧ-инфицированными пациентами позволили подробно изучить стадии развития данной инфекции. Согласно принятой классификации, заболевание в своем развитии проходит шесть стадий.
Первая стадия протекает, как правило, бессимптомно и длится 6–12 мес. после заражения. В это время происходит размножение ВИЧ, которое затем затухает. Содержание T4-лимфоцитов в крови при этом обычно близко к норме (около 800 клеток в 1 мл).
Вторая, самая протяженная по времени стадия (обычно 3–5 лет) характеризуется развитием хронической лимфо-аденопатии (увеличением лимфатических узлов) и постепенным снижением содержания T4-лимфоцитов в крови. Самочувствие больного на этой стадии все еще хорошее.
Снижение титра (концентрации) T4-лимфоцитов ниже 400 клеток/мл знаменует наступление третьей стадии, которая характеризуется скрытым (субклиническим) нарушением иммунной системы.
Четвертая стадия ВИЧ-инфекции по внешним проявлениям не отличается от предыдущей, но для нее характерны более глубокие изменения в иммунной системе, которые выявляются лишь дополнительными анализами.
На пятой стадии иммунная система больного угнетается настолько, что появляется клиническое проявление в виде грибкового поражения слизистых полости рта, называемого молочницей. К началу этой стадии концентрация T4-лимфоцитов в крови обычно становится менее 200 клеток/мл. Кроме молочницы на этой стадии часто развиваются стойкие вирусные и/или грибковые заболевания кожи и слизистых (например, хроническая инфекция вирусом простого герпеса).
Через 1-2 года после начала пятой стадии у больного развиваются так называемые хронические оппортунистические инфекции, вызываемые условно-патогенными микроорганизмами, что свидетельствует о глубоких нарушениях иммунной системы. Часто такой инфекцией является тяжелая пневмония, вызываемая простейшими Pneumocystis carinii (пневмоцистоз). Такие осложнения свидетельствуют о переходе ВИЧ-инфекции в последнюю шестую стадию, которая и называется СПИД. Содержание T4-лимфоцитов при этом обычно ниже 100 клеток/мл (у здорового человека – не менее 800 клеток/мл). Данная стадия длится, как правило, не более двух лет и завершается смертью больного.
В Африке катастрофа уже охватила сегодня до 30% населения некоторых стран. Официальная мировая статистика свидетельствует, что к концу 2002 г. от СПИДа уже умерли около 25 миллионов человек, и около 42 миллионов инфицированы. Россия, Украина и Беларусь при этом входят в число лидеров по темпам нарастания заболеваемости. В России, начиная с 1996 г., даже официальные данные регистрируют ежегодное увеличение количества больных в 2–3 раза. По разным подсчетам, в России на настоящий момент могут быть инфицированы от 220 тысяч до 1,5 миллионов человек. В настоящее время самыми неблагополучными по распространению ВИЧ-инфекции являются Калининградская, Ростовская, Нижегородская области, Краснодарский край и Москва. Устрашает прогноз Национального разведывательного совета США (US National Intelligence Council), обнародованный в октябре 2002 г. Если верить ему, к 2010 г. каждый десятый работоспособный россиянин может быть инфицирован ВИЧ.
Гепатит С. Слово "гепатит" происходит от греческого слова hepar, hepatos, которое в переводе означает "печень", а собственно термин "гепатит" обозначает название совокупности симптомов болезни – воспаления печени. Симптомы этой болезни известны с давних времен, но причины ее стали проясняться только в 1963 г., когда впервые была доказана инфекционная природа одного из видов гепатита – гепатита В. Опасность этого заболевания для человека подтверждает тот факт, что почти половину пациентов инфекционных клиник в нашей стране в настоящее время составляют больные гепатитами, а вторым по важности фактором канцерогенеза (т.е. способствующим возникновению рака фактором) после табакокурения является перенесение инфекции вирусом гепатита В.
Все вирусные гепатиты по способу их передачи от человека к человеку можно разделить на две группы:
передающиеся фекально-оральным путем (т.е. через загрязненные уже зараженным человеком воду, продукты питания, реже – предметы личного обихода) вирусы гепатитов А, Е и F. Поскольку эти вирусы стойки при температурах около 30°C, то они широко распространены в жарких странах;
передающиеся парентеральным (в том числе половым) или инъекционным путем, т.е. при пользовании без необходимой тщательной стерилизации многоразовыми шприцами и мединструментами, при многократных инъекциях крови и препаратов, полученных из донорской крови, половым путем и т.д. Сюда относятся гепатиты B, C и G.
Со времени открытия вирусной природы заболевания и обнаружения вирусов гепатитов А и В выяснилось, что лишь немногим более половины случаев этого заболевания обусловлены инфицированием именно этими типами возбудителей и, по всей вероятности, существуют и другие вирусы, вызывающие гепатиты у людей. Со временем даже возник термин – гепатит "ни-А, ни-В". Лишь в конце 1980-х гг. был обнаружен новый вирус, вызывающий заболевание печени, его назвали вирусом гепатита С (ВГС). В настоящее время установлено, что до 40% случаев посттрансфузионных гепатитов (т.е. гепатитов, возникающих после применения для лечения человека препаратов из донорской крови) вызывается этим вирусом.
По имеющимся данным, в мире около 3% населения являются хроническими носителями ВГС. Передается он от человека к человеку так же, как и гепатит В. В России при обследовании ежегодно выявляется 10–20 тысяч новых носителей этого вируса, однако ввиду того, что исследования начаты лишь в 1995 г., эта цифра представляется заниженной. Предполагаемое число носителей (по аналогии с другими странами) может достигать 2–3 миллионов.
В настоящее время ВГС относят к семейству флавивирусов. Долгое время его не могли обнаружить в крови в виде вирусной частицы, и лишь в последние годы это удалось сделать. Размер его вириона составляет 38–50 нм. Устройство генетического материала ВГС (рисунок 10) подобно геномам пести- и флавивирусов, типичными представителями которых являются вирусы желтой лихорадки и клещевого энцефалита.
Р исунок
10 – Строение геномной РНК виуса гепатита
С. C
– капсидный белок, Е1 и Е2 – поверхностные
белки, NS5
– РНК-полимераза
исунок
10 – Строение геномной РНК виуса гепатита
С. C
– капсидный белок, Е1 и Е2 – поверхностные
белки, NS5
– РНК-полимераза
Он состоит из одноцепочечной РНК, длиной около 9400 нуклеотидов. На 5'- и 3'- концах вирусной РНК находятся нетранслируемые (некодирующие) области. Между ними заключена единственная открытая протяженная рамка трансляции (рамка считывания генетического кода в аминокислотную последовательность), с которой считывается вирусный полипептид (3010 или 3011 аминокислот, начиная с первого остатка аминокислоты метионина). Последовательность генов в геноме ВГС подобна таковой у пести- и флавивирусов. Вирусная рамка считывания может быть разделена на структурную и неструктурную части.
Структурная часть состоит из генов белка вирусного нуклеокапсида C и гликопротеинов оболочки E1 и E2. Ген белка C среди различных изолятов ВГС весьма консервативен. Гены гликопротеинов E1 и E2 значительно менее консервативны и имеют очень изменчивые от изолята к изоляту районы. У представителей рода флавивирус, по названию которого получило название семейство, белок, соответствующий гликопротеину E2 оболочки вириона ВГС, не входит в состав вирусной частицы. Он является первым (по порядку расположения генов в вирусной РНК) неструктурным белком флавивирусов и обозначается NS1. Поэтому гликопротеин E2 вируса гепатита C обозначают также E2/NS1.
Неструктурная часть генома ВГС кодирует белки NSp2-Nsp5, большинство которых являются либо вирусспецифическими протеазами, либо ферментами, ответственными за размножение вируса.
Гепатит GB. В середине 90-х гг. обнаружены еще несколько вирусов, поражающих печень. В частности весной 1995 г. выявлен вирус гепатита, передающийся парентеральным путем, точнее сразу три его разновидности, объединенные именем гепатит GB: гепатиты GB-A, GB-B и GB-C. Все разновидности относятся, как и вирус гепатита С, к семейству флавивирусов, передаются от человека к человеку так же, как и гепатит С. Эти вирусы, по всей вероятности, являются причиной до 5% всех перентеральных гепатитов у людей. Обнаружены они, как и вирус гепатита С, методами молекулярной биологии.
Герпесвирусы 6, 7, 8. Герпетическая инфекция (син.: простой герпес) – собирательное название для инфекций, вызываемых вирусом простого герпеса первого типа (ВПГ-1) и вирусом простого герпеса второго типа (ВПГ-2). Термин «герпес» (от греческого herpes – ползучий) был использован Геродотом в 100 г. до н.э. для описания волдырей, сопровождающихся лихорадкой.
Вирусы, относящиеся к семейству герпесвирусов, очень широко распространены в природе. Они могут вызывать заболевания у различных видов диких и домашних животных (кошек, собак, лошадей, коров, кур, рыб и др.). В настоящее время известно более 100 герпесвирусов, 8 из них выделены от человека: вирусы простого герпеса первого и второго типов (HSV-1, HSV-2), ветряной оспы – опоясывающий герпес, цитомегаловирус (CMV), вирус Эпштейна–Барр, вирусы герпеса человека шестого, седьмого и восьмого типов (HHV-6, HHV-7, HHV-8).
К семейству Herpesviridae относятся три подсемейства: аlpha-Herpesviridae, beta-Herpesviridae, gamma-Herpesviridae.
Наиболее важным биологическим свойством герпесвирусов в патогенезе заболеваний является их способность к латентному существованию. Герпесвирусы способны пожизненно персистировать в организме человека и вызывать заболевания с многообразными клиническими проявлениями:
острые и хронические рецидивирующие инфекции с поражением кожных покровов и слизистых оболочек, внутренних органов, центральной нервной системы;
трансплацентарные инфекции с поражением плода;
лимфопролиферативные заболевания.
Одной из самых распространенных вирусных инфекций человека является простой герпес (ВПГ), представляющий собой серьезную медико-социальную проблему. Около 90% людей на земном шаре инфицированы ВПГ и около 20% имеют какие-либо клинические проявления инфекции. Все герпесвирусы имеют выраженное иммуносупрессивное действие, подавляют клеточные и гуморальные реакции иммунитета. Наименее изучены клинические проявления инфекций, вызванных герпесвирусами шестого, седьмого и восьмого типов, у детей.
HHV-6 – шестой член семейства герпесвирусов человека является причиной розеолы, имеет многообразные проявления у детей и взрослых. Хотя этот новый вирус был найден изначально в B-лимфоцитах иммуноскомпрометированных взрослых больных, впоследствии выяснилось, что он имеет первоначальное сродство с T-лимфоцитами, и его оригинальное название – человеческий В-лимфотропный вирус (HBLV) – было изменено на HHV-6.
HHV-6 входит в состав рода Roseolovirus, подсемейства beta-Herpesvirus. Подобно другим вирусам герпеса HHV-6 обладает характерным электронно-плотным ядром и икосаэдральным капсидом, окруженным оболочкой и внешней мембраной, местом расположения важных гликопротеинов и протеинов мембраны. Главный компонент клеточного рецептора для HHV-6 – CD46, который присутствует на поверхности всех ядерных клеток и позволяет HHV-6 инфицировать широкий ряд клеток. Главная цель HHV-6 – это зрелая клетка CD4+, но вирус может инфицировать естественных киллеров (NK), гамма-дельта T-лимфоциты, моноциты, древоподобные клетки, астроциты и разнообразные линии T и B клеток, мегакариоцитов, ткань эпителия и др.
Серологические исследования HHV-6 показали повсеместность случаев HHV-6-инфекции: ее обнаруживали во всех странах, где проводили исследования. Инфицирование происходит обычно на первом или втором году жизни, и соответственно около 95% взрослых имеют антитела к HHV-6. В Соединенных Штатах Америки, Японии установлено, что приобретенная HHV-6 инфекция встречается преимущественно у младенцев 6–18 месяцев жизни. Почти все дети инфицируются в возрасте до трех лет и сохраняют иммунитет на всю жизнь. Наиболее показательно, что инфекция HHV-6, приобретенная в детском возрасте, приводит к высокой частоте серопозитивности у взрослых.
HHV-7 – седьмой член семейства Herpesviridае – впервые идентифицирован в клетках здорового взрослого человека в 1990 г. HHV-7 также входит в состав рода Roseolovirus, подсемейства beta-Herpesvirus, имеет морфологическое, антигенное и геномное сходство с HHV-6. Он имеет нуклеокапсид, содержащий ДНК, окруженный плотной оболочкой и липидным покрытием. HHV-7 прежде всего заражает CD4+ T-клетки, такие как мононуклеары пуповинной и периферической крови. В эпителиальных клетках слюнных желез он пролиферирует с выбросом вирусов. Другие ткани, такие как кожа, молочная железа, легкие, также могут содержать антиген HHV-7.
HHV-7 является распространенной инфекцией детского возраста, которая проявляется несколько позже, чем HHV-6, и в более широком возрастном диапазоне. Серологические исследования показали, что большинство индивидуумов в Соединенных Штатах инфицируются HHV-7 к 6–10-му году жизни. HHV-7 выделяется в слюне у 95% взрослых, что указывает на высокий уровень инфицированности населения и склонность HHV-7 к персистенции. HHV-7 наиболее вероятно передается через слюну, в которой вирус активно реплицируется.
HHV-8 имеет более давнюю историю. В 1872 г. венгр Мориц Капоши впервые описал агрессивную пигментированную идиопатическую саркому кожи. Эта опухоль сегодня хорошо известна как саркома Капоши. Ранее в США и странах Западной Европы она была редкой патологией, ее частота составляла менее 0,06 на 100 тыс. человек, пока не возникла эпидемия СПИДа. Спустя сто лет, в начале 80-х гг., появились сообщения о высокой частоте саркомы Капоши у гомосексуальных мужчин, впоследствии этот показатель увеличился до 15–20% у гомосексуальных ВИЧ-зараженных мужчин. В течение некоторого времени предполагалась вирусная этиология саркомы Капоши. Ассоциация с HHV-8 и саркомой Капоши не предполагалась, пока. в 1994 г. не открыли герпесвирус, связанный с саркомой Капоши (KSHV), который сегодня классифицирован как HHV-8 в пределах подгруппы герпесвирусов гамма-2, группы Rhadinovirus.
Выявлены вариации HHV-8 инфекции, связанные с географическими и социоэкономическими факторами. Сероэпидемиологические исследования показали высокие уровни заболеваемости классической саркомой Капоши в странах Африки, особенно Центральной; низкие – в США, Японии и в некоторых северных европейских странах, средние – в большинстве средиземноморских стран. Основная группа риска в США – гомосексуальные мужчины, у которых серопозитивность составляет около 40%.
Передача HHV-8 происходит различными путями, но, вероятно, преобладает половой путь, а также передача через слюну. Это подтверждается выявлением HHV-8 в сперме. Дополнительные пути заражения обусловлены присутствием ДНК вируса HHV-8 в слюне и лимфоцитах периферической крови. В Африке, где существует эндемическая форма саркомы Капоши, инфицирование HHV-8 происходит обычно в детстве, относительно высокий уровень инфицирования отмечается также в период становления сексуальной активности. Перинатальный путь передачи отмечен в странах Африки и на острове Сардиния.
Атипичная пневмония. Этот термин применяется для обозначения двух различных заболеваний:
В медицинской литературе под атипичной пневмонией традиционно понимается воспаление легких, вызванное микоплазмами, хламидиями или легионеллами и имеющее необычное для него клиническое течение.
Новая болезнь, выявленная в ноябре 2002 г. в Китае, затем в Гонконге, получившая там эпидемическое распространение и зарегистрированная к маю 2003 г. в 30 других странах (численность заболевших превысила 7 тыс. чел., умерло – свыше 500), в средствах массовой информации получила название атипичной пневмонии. В медицинской литературе по предложению ВОЗ для обозначения ее применяется термин тяжелый острый респираторный синдром, или САРС (SARS – severe acute respiratory syndrom).
Возбудитель САРС – неизвестная ранее разновидность коронавируса (названного так в связи с внешним сходством вирусной частицы с короной: круглая форма с шипиками). В окружающей среде коронавирусы гибнут в течение нескольких часов, на пластиковых поверхностях могут сохраняться до двух суток. Заражение происходит воздушно-капельным путём, главным образом при близком контакте с кашляющим, чихающим больным. Вирус поражает не только верхние дыхательные пути, но и бронхи, бронхиолы, вызывая воспалительное утолщение их стенок, пропотевание жидкости в альвеолы, нарушение газообмена в лёгких и недостаточное поступление кислорода в кровь. На этом фоне возникает одно- или двусторонняя пневмония, которую вызывает, вероятно, бактериальная флора, населяющая дыхательные пути (аутофлора). Смерть больных (летальность составляет около 7%) обусловлена тяжёлой дыхательной недостаточностью.
Инкубационный период длится обычно от двух до семи суток, иногда до 10 суток. Болезнь проявляется остро: повышение температуры тела до 38 °С и выше, озноб, боли в мышцах, головная боль, общая слабость. Примерно у четверти больных наблюдаются боли в горле и насморк. Возможны головокружение, тошнота, рвота, боли в животе, жидкий стул. Чаще через два–три дня состояние больного улучшается, при тяжёлом течении болезни появляются кашель, сухой или с небольшим количеством мокроты, одышка и быстро развивается выраженная дыхательная недостаточность. При непосредственном исследовании больного и рентгенологически выявляют признаки пневмонии; в гемограмме чаще отмечается лейкопения. Смертность от атипичной пневмонии составляет 3,6%. У 10-20% заразившихся болезнь протекает в тяжелой форме и сопровождается осложнениями; 80-90% заболевших выздоравливают.
Лихорадка, кашель и затрудненное дыхание в сочетании с данными эпидемиологического анамнеза (контакт с больным или возможность такого контакта, например приезд из Китая, Гонконга или Тайваня) позволяют поставить предположительный диагноз тяжёлого острого респираторного синдрома. При подозрении на САРС больной подлежит госпитализации и строгой изоляции в специально оборудованном боксе. Проводят кислородотерапию, искусственную вентиляцию лёгких, лечение антибиотиками широкого спектра действия, а также противовирусными препаратами (однако их эффективность не доказана). С целью индивидуальной профилактики показаны применение противовирусных иммуностимулирующих препаратов: арбидол, амиксин, закаливание организма, рациональное питание, поливитамины.
Возможные причины появления новых и возникающих вирусных инфекций.
Несмотря на многолетнее изучение рассмотренных вирусных инфекций в ведущих лабораториях мира, до сих пор не удалось найти ответа на многие связанные с ними вопросы:
какие живые существа являются природными хозяевами этих вирусов?
почему возникают вспышки этих заболеваний?
каким образом и где заразились самые первые больные во время эпидемий?
почему неэффективны в борьбе против этих вирусов вакцинные препараты, полученные по технологиям, успешно апробированным на других возбудителях?
что является причиной высокой смертности от этих инфекций?
Ответы на вопросы ученые целенаправленно ищут много лет, но окончательных результатов до сих пор нет. Кроме того, набор довольно странных обстоятельств, сопутствовавших началу эпидемий в Африке, придал ореол мистики всему, что связано с этими вирусами. Может быть, именно поэтому полудокументальная книга о вирусах Ричарда Престона "Горячая зона" стала бестселлером в США в 1994 г., а снятый по ее мотивам фильм "Эпидемия" – одним из лидеров видеопроката во всем мире.
Некоторые исследователи считают, что возникновение вирусов, подобных ВИЧ, Эбола, является следствием разрушения экосистемы тропических лесов. Все вирусы возникали там, где экосистема была нарушена, особенно это относится к тропическим лесам – самым большим резервуарам жизни на планете. «Вырываясь из лесов, вирус проносится сквозь человечество, как эхо от криков умирающей природы», – говорится в одной интернет-статье.
Есть и другая точка зрения. В отношении ВИЧ-инфекции выдвинута научно обоснованная гипотеза о существовании в Африке глобального природного очага этого заболевания. Первенство здесь принадлежи белорусским ученым: академику РАМН и НАНБ В.И.Вотякову и его ученикам и последователям, сотрудникам НИИ эпидемиологии и микробиологии Минздава Республики Беларусь. Согласно этой гипотезе, в Центральной Африке издавна сформировался природный очаг вируса иммунодефицита обезьян (ВИО). Здесь обитает до 50 видов и подвидов обезьян (зеленые мартышки, павианы, мангобеи, мандрилы, шимпанзе и др.), каждый из которых обладает тем или иным вариантом вируса в латентном состоянии. Оказавшись у нового "хозяина" – обезьяны другого вида или человека – вирус активизируется и наносит ему, неприспособленному к данному типу вируса, непоправимый ущерб. Попадает такой вирус к человеку преимущественно через кровь в результате контактов с обезьянами, прежде всего при охоте на них (укусы, разделка мяса, снятие шкурок). Установлено, например, что перенос вируса от шимпанзе в человеческую популяцию произошел всего 50–80 лет назад. Мутациям, превращающим ВИО в ВИЧ, способствует и постоянное недоедание аборигенов и ослабленный вследствие этого иммунитет. Контакты же с европейцами сделали проблему ВИЧ-инфекции всемирной. Вполне возможно, что так же обстоит дело и с другими видами вирусов африканского происхождения, например, вирусами Эбола, Денге и т.п. У хантавирусов явно прослеживаются азиатские корни.
Вызывает опасение тот факт, что инфекции такого рода привлекают внимание военных биологов и потенциальных биотеррористов. Отсутствие средств эффективной профилактики и защиты против целой серии геморрагических лихорадок сочетается с достаточно высокой смертностью, легкостью распространения боевых рецептур (распыление). К счастью, вирусы культивировать труднее, чем бактерии, поэтому пока не приходится опасаться производства вирусов геморрагических лихорадок в промышленных масштабах.
Билет № 13
Проблемы иммунитета растений.
У РАСТЕНИЙ ЗАЩИТНЫЕ МЕХАНИЗМЫ ЕЩЕ БОЛЕЕ РАЗНООБРАЗНЫЕ
ДВЕ ЛИНИИ ЗАЩИТЫ:
ВРОЖДЕННЫЙ (ПЕРВИЧНЫЙ) ИММУНИТЕТ
Два типа патогенов:
Биотрофные (прижизненные) патогены и некротрофные патогены
Биотрофные приспособлены получать питание на живых тканях растений. Многие биотрофные патогены живут в межклеточном пространстве мезофильных клеток листьев
Некроторофные патогены живут на поврежденных тканях, на ранах, старых тканях. Они могут расти как сапрофиты вне ткани хозяина.
Первичная врожденная иммунная система
!!! В отличие от животных, растения не имеют адаптивной (приобретенной) иммунной системы
У РАСТЕНИЙ ДВА УРОВНЯ ВРОЖДЕННОГО ИММУНИТЕТА
Первичная врожденная иммунная система обеспечивается рецепторами, которые получили название Образ-распознающие рецепторы (ОРР), которые распознают, т.н. Патоген-ассоциированные молекулярные структуры (ПАМС) или (МАМС)
Физиология ответа
После распознавания ПАМС (флагеллин, липополисахариды (ЛПС), фактор элонгации TU (thermo-unstable) (EF-TU)) из Грам-отрицательных бактерий
происходит индукция иммунных ответов,
что включает
Изменения клеточной стенки, отложение каллозы (восстанавливает целостность клетки),
Аккумуляция защитных белков (хитиназ, глюканаз, протеаз)
Взаимодействие ОРР - ПАМС
ОРР распознают отдельные домены ПАМС
Для каждой ПАМС свой ОРР В настоящее время установлены:
ОРР, распознающий флагеллин, – FLS2
ОРР, распознающий elf - ERF
FLS2(flagellin-sensitive) – рецепторная киназа (RLK, receptor-like kinase), содержащая снаружи клетки повторы, богатые Leu, а внутри клетки Ser/Thr киназные домены (S/T K)
Другие ОРР- LRR (leucine- rich repeats),
содержащие рецепторы (Они структурно похожи на RLK, но не содержат киназного домена
LysM- распознает грибок хитин
Считается, что все ОРР – это либо RLK, либо LRR
Распознавание flg22 рецептором FLS2 приводит к ограничению роста бактериального патогена Pseudomonas syringae
У ЖИВОТНЫХ РОЛЬ ОРР играют Toll-подобные рецепторы FLS2 и TLR5. распознают флагеллин
Единый предок???
Как работают ОРР
Установлено, что N-конец флагеллина (22 ак остатка) достаточен для активации ОРР
Этот конец активирует MAPK-каскад, который активирует транскрипционный фактор WRKY, который запускает первичный иммунный ответ
!!! FLS2 – RLK-белок
Эффекторы патогенов подавляют первичный иммунный ответ
Чтобы обойти ОРР, они содержат TTSS (Type III secretion system)
Система секреции типа III
ССТТ
Как действует ССТТ?
Используя ССТТ, патогенные бактерии впрыскивают эффекторы, которые подавляют первичный иммунный ответ
В настоящее время известно около 30-40 эффекторов
P.Syringae эффекторы
Наиболее изучены, хотя механизмы недостаточно понятны: AvrPto, AvrRpt2, AvrRpm1, Avr2, Avr4.
Действие эффекторов
Эффекторы патогенов животных способны секретировать незначительное число эффекторов. У патогенов растений их значительно больше (20-30 в ряде случаев).
Установлено, что впрыскиванию предшествует разворачивание белков-эффекторов. Шапероны помогают сохранять белки в развернутом состоянии.
Эффекторы подавляют защитный эффект, инициируемый после распознавания
Считается, что ряд эффекторов влияет на транскрипцию в ядре.
Второй механизм.
Действие на сигнальные молекулы (салициловая кислота, жасмоновая кислота, этилен), регулирующие защиту
Третий механизм (см. AvrPto)
Некоторые эффекторы подавляют сверхчувствительный ответ (СЧО), действуя как E3-убиквиттин-лигаза, подавляющая апоптоз
Убиквитин-зависимая система протеолиза: деградация белков
Убиквитин-зависимая система протеолиза проводит поиск потенциальной мишени для протеолитической деградации среди внутриклеточных белков. Белки несут специфические сигналы деградации по аналогии с сигнальными последовательностями, которые направляют вновь синтезируемые белки к определенным микрокомпартментам клетки.
Распознанные данной системой белки-субстраты маркируются путем ковалентного присоединения к ним молекул стабильного 76- звенного белка - убиквитина . Убиквитин соединяется C-концом с боковыми остатками лизина в субстрате. Наличие такой метки в белке является первичным сигналом сортировки, направляющей образовавшиеся конъюгаты к протеасомам. В большинстве случаев к субстрату присоединяется несколько молекул убиквитина, которые организованы в виде бусинок на нитке. Молекулы белков, содержащие убиквитин, по-видимому, являются для протеасом предпочтительными субстратами.
Ген-на– ген теория
Каждому гену эффектора соответствует R-ген, каждому эффектор-белку соответствует R-белок
В течение долгого времени ведется дискуссия относительно является ли взаимодействие эффектора и R-белка прямым или опосредованным
Установлено, что LRR определяет распознавание
HR(hypersensitive response) СЧО(сверхчувствительный ответ)
СЧО- растительный апоптоз, связанный с активацией исполнительных каспаз
Физиологический смысл – уничтожить плохое, чтобы сохранить остальное
ЗАКЛЮЧЕНИЕ:
Идет постоянная эволюционная борьба между механизмами противодействия патогенам и эффекторами патогенов
Бихевиоризм, гештальтпсихология, когнитивная психология
Понятие о когнитивной психологии. Когнитивная психология (латинское cognitio – знание, познание) – направление в психологии, возникшее в США в конце 50-х – начале 60-х гг. XX в. в противовес бихевиоризму. Возникновению бихевиоризма способствовали разработки в области условных рефлексов и развитие зоопсихологии. Бихевиоризмом не принимались во внимание врожденные качества человека, его убеждения и другие личностные качества, основой всего считалось поведение. Развитие когнитивной психологии стало возможным благодаря предшествовавшим работам в области гештальтпсихологии, привлекшим внимание к вопросам восприятия и эффективному творческому мышлению, исследование которого является одной из основных задач науки. Когнитивная психология во многом основывается на аналогии между преобразованием информации в вычислительном устройстве и осуществлением познавательных процессов у человека – для пояснения этой аналогии было введено понятие компьютерной метафоры. Когнитивная система человека рассматривается как комплекс, имеющий устройства ввода, хранения и вывода информации. Информация, достигшая когнитивной системы, преобразуется, обрабатывается, кодируется, хранится, запоминается и забывается, а затем преобразуется в знание. Методологическая платформа когнитивной психологии основана на компьютерных технологиях и новых теоретических исследованиях в области психологии.
Весь описанный эпизод занял бы не более двух минут, но то количество информации, которую восприняли и проанализировали эти два человека, просто поражает. Как должен психолог рассматривать такой процесс? Один выход – это просто на языке «стимул–реакция» (S-R): например, светофор (стимул) и поворот налево (реакция). Некоторые психологи, особенно представители традиционного бихевиористского подхода уверены, что всю последовательность событий можно адекватно (и гораздо более детально) описать в таких терминах. Однако, хотя эта позиция и привлекает своей простотой, она не в состоянии описать те когнитивные системы, которые участвуют в подобном обмене информацией. Чтобы это сделать, необходимо определить и проанализировать конкретные компоненты когнитивного процесса и затем объединить их в большую когнитивную модель.
Восприятие. Отрасль психологии, непосредственно связанная с обнаружением и интерпретацией сенсорных стимулов, называется психологией восприятия. Из экспериментов по восприятию мы хорошо знаем о чувствительности человеческого организма к сенсорным сигналам и о том, как интерпретируются эти сенсорные сигналы. Описание, данное полицейским в приведенной уличной сцене, значительно зависит от его способности «видеть» существенные признаки окружения.
Распознавание образов. Стимулы внешней среды не воспринимаются как единичные сенсорные события; чаще всего они воспринимаются как часть более значительного паттерна (так в психологии называют набор сенсорных стимулов, принадлежащих одному классу объектов). То, что мы ощущаем (видим, слышим, обоняем или чувствуем вкус), почти всегда есть часть сложного паттерна. Так, когда полицейский говорит водителю «проехать через железнодорожный переезд мимо озера… рядом со старой фабрикой», его слова описывают сложные объекты (переезд, озеро, старая фабрика). В какой-то момент полицейский описывает плакат и предполагает при этом, что водитель грамотный.
Внимание. Полицейский и водитель сталкиваются с несметным количеством признаков окружения. Если бы водитель уделял внимание им всем (или почти всем), он никогда бы не добрался до хозяйственного магазина. Хотя люди – это существа, собирающие информацию, очевидно, что в нормальных условиях мы очень тщательно отбираем количество и вид информации, которую стоит принимать в расчет.
Память. Мог бы полицейский описать дорогу, не пользуясь памятью? Вряд ли. В нашем примере ответ полицейского стал результатом работы двух типов памяти. Первый тип – кратковременная память (КВП) удерживает информацию ограниченное время, пока ее не заменит новая – достаточно долго, чтобы поддержать разговор. C другой стороны, значительная часть содержания ответов полицейского получена из его долговременной памяти (ДВП). Наиболее очевидная часть здесь – знание им языка. Он не называет озеро лимонным деревом, место выставок – автопокрышкой, а улицу – баскетболом; он извлекает слова из своей ДВП и использует их более-менее правильно.
Воображение. Для того, чтобы ответить на вопрос, полицейский построил мысленный образ окружения. Этот мысленный образ имел форму когнитивной карты: т.е. мысленного представления множества зданий, улиц, дорожных знаков, светофоров и т.п. Он был способен извлечь из этой когнитивной карты значимые признаки, расположить их в осмысленной последовательности и преобразовать в языковую информацию, которая позволила бы водителю построить сходную когнитивную карту. Эта когнитивная карта дала бы водителю вразумительную картину города, которая могла быть преобразована в акт вождения автомобиля по определенному маршруту.
Язык. Чтобы правильно ответить на вопрос, полицейскому нужны были обширные знания языка. Это подразумевает знание правильных названий для ориентиров и, что тоже важно, знание синтаксиса языка — т.е. правил расположения слов и связей между ними. Приведенные словесные последовательности могут не удовлетворить педантичного профессора филологии, но вместе с тем они передают некоторое сообщение. Почти в каждом предложении присутствуют существенные грамматические правила. Полицейский не сказал: «них ну это хозяйственном в у»; он сказал: «Ну, это у них в хозяйственном», – и мы можем понять, что имеется в виду.
Приведенные положения можно объединить в более крупную систему, или когнитивную модель. Модель, которой обычно пользуются когнитивные психологи, называется моделью переработки информации.
Однако пока не ясно, как применять когнитивную теорию в прикладных задачах «на интеллект». И потому на практике для измерения интеллекта по-прежнему используются традиционные тесты, основанные на феноменологических теориях интеллекта полувековой давности.
А раз мы не можем четко определить, что такое человеческий интеллект, его машинное моделирование представляется также крайне затруднительным. Здесь уместно привести цитату из интернет-публикации Александра Соловьева (http://soloviev.nevod.ru/), где он справедливо отмечает, что «самое трудное – это не разместить в машине знания, а извлечь их "из человека", чтобы было что размещать в машине».
Билет № 14
Стволовые клетки эмбриона и взрослого организма, их использование для восстановления органов.
Стволовые клетки эмбриона и взрослого организма.
Стволовые клетки эмбриона и взрослого организма
Из истории стволовых клеток. Открытие стволовой клетки находится в одном ряду с такими великими достижениями человечества, как открытие двухспиральной цепочки ДНК. Однако про стволовые клетки известно уже почти сто лет. В 1908 г. собственную концепцию их развития предложил русский ученый Александр Максимов. Первые в мировой науке работы по стволовым клеткам в 1960–70-е гг. выполнили советские ученые И.Чертков и А.Фриденштейн, но мировая шумиха вокруг них началась только в конце 90-х гг., когда стволовые клетки заново “открыли” в США. Американские исследователи сумели выделить эмбриональные стволовые клетки и доказать, что они могут по команде превращаться в любые другие. Когда стало ясно, что стволовые клетки могут быть внесены в организм искусственно, начался настоящий бум исследований, первые итоги которого отражает Нобелевская премия 2007 г., присужденная англичанину Мартину Эвансу (Martin J. Evans) и американцам Марио Капеччи (Mario R. Capecchi) и Оливеру Смитису (Oliver Smithies) “за их открытия принципов введения специфических генных модификаций у мышей с помощью эмбриональных стволовых клеток”.
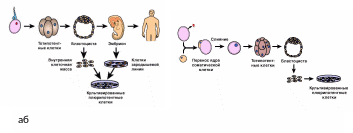
Получение плюрипотентных клеток. В настоящее время линии плюрипотентных клеток человека получают из двух источников с помощью методов, отработанных на животных моделях. В первом случае плюрипотентные клетки выделяют непосредственно из внутренней клеточной массы эмбриона человека на стадии бластоцисты (рисунок 8а). Сам эмбриональный материал получали в больших количествах в клинических, а не исследовательских целях для осуществления экстракорпорального оплодотворения, всякий раз испрашивая разрешение на его использование у обоих доноров. Клетки внутренней клеточной массы культивировали и получали линию плюрипотентных клеток. По этому методу плюрипотентные клетки можно выделять также из ткани плода. Разрешение на это давалось обоими супругами уже после того, как они сами приняли решение прервать беременность. Клетки отбирались из той области плода, которая должна была развиться в яичники или семенники.
Рисунок 8 – Различные способы получения плюрипотентных эмбирональных клеток: из клеточной массы эмбирона или ткани плода (а); путем переноса в яйцеклетку ядра соматической клетки (б)
Несмотря на то, что плюрипотентные клетки в двух указанных случаях происходили из разных источников, полученные клеточные линии были идентичными.
Еще одним способом получения плюрипотентных клеток может стать метод, основанный на переносе в энуклеированную (лишенную ядра) яйцеклетку ядра соматической клетки (рисунок 8б). Соответствующие опыты уже проведены на животных. Сама яйцеклетка с новым ядром и ее непосредственные «потомки» способны при соответствующих условиях развиться в полноценный организм, т.е. являются тотипотентными. Из них формируется бластоциста, которая и служит источником плюрипотентных клеток.
Молекулярные основы тотипотентности эмбриональных стволовых клеток (ЭСК). Геном зиготы и ЭСК находится в так называемой "нулевой точке", откуда стартуют две главные программы эмбриогенеза: 1) гаструляция + органогенез; 2) рестрикционное созревание дифференцированных клеточных линий.
Эти две программы задействуют примерно 5000 генов. Каким образом реализуется тотипотентность генома, т.е. способность выбирать одну из многих траекторий развития? Серийный анализ генной экспрессии (SAGE) в культуре ЭСК, мезенхимальной, нейрональной и гематогенной стволовых клетках (МСК, НСК, ГСК соответственно) выявил важнейшую закономерность. Во всех перечисленных стволовых клетках присутствовали сходные наборы предсинтезированных мРНК следующих классов генов:
ранних генов экто-, мезо- и эндодермы;
набор мРНК гомеотических (Нох) генов, контролирующих сегментацию и трехмерную карту зародыша;
пять наборов мРНК генов тотипотентности. Каждый набор факторов тотипотентности увязан с комплементарным набором факторов и рецепторов пролиферации на прогениторных клетках в клоне. Особенно существенны спаренные блоки генов, контролирующие пролиферацию соседних слоев прогениторных клеток в клоне (типа Delta/Notch);
мРНК генов апоптоза, контролирующих численность прогениторных клеток в клоне. Баланс клеток достигается за счет их миграции и частичной гибели в клоне. Пролиферация постоянно уравновешивается миграцией и апоптозом клеток;
набор мРНК контрольных генов (master genes) рестрикционного созревания специализированных клеточных линий;
наборы мРНК генов миграции и навигации миграторных клеток.
Таким образом, в основе тотипотентности ЭСК, МСК и других типов стволовых клеток выявлен универсальный механизм: направленная активация и последующий импорт мРНК в ядро. Детали импорта/экспорта информации между ядром и цитоплазмой в ЭСК пока плохо изучены. Однако эта концепция тотипотентности подтверждается новыми наблюдениями, выполненными на одиночных клонах мезенхимальных стволовых клеток специальной техникой MICRO-SAGE. Микрометод верифицировал присутствие мРНК 1200 ключевых генов эмбриогенеза в одном клоне МСК.
Стволовые клетки взрослого организма. В клонах МСК из взрослой гематогенной ткани идентифицированы практически все наборы мРНК зародышевых листков, органогенеза, а также мРНК master-genes, контролирующих рестрикционное созревание линий мезенхимального, мезодермального происхождения, экто- и эндодермы. Клоны МСК, по сути, представляли собой библиотеки мРНК ранних этапов органогенеза и рестрикционного созревания специализированных линий.
Если программы органогенеза обеспечивает направленный импорт мРНК в ядро для включения новых котранскриптаз, транскриптаз и транскрипционных комплексов, то рестрикционное созревание клеточных линий связано с экспортом мРНК из ядра в цитоплазму с последующей модификацией белкового фенотипа прогениторных клеток.
Различия в потенции стволовых клеток разного происхождения. В зародыше и взрослом организме потенции генома стволовых клеток существенно варьируют по "ассортименту" фенотипа специализированных клеток. Более ранние, тотипотентные ЭСК дифференцируются в любую из 250 линий специализированных клеток органов. Необходимо подчеркнуть, что ЭСК in vitro не продуцируют клеток трофобласта, плаценты, т.е. потенции генома ЭСК меньше зиготы. Соответственно биологический статус ЭСК меньше статуса раннего зародыша. Плюрипотентные ЭСК дают более ограниченный спектр фенотипов. Например, мезенхимальные стволовые клетки (МСК), локализованные в опорно-сосудистом каркасе органов, дифференцируются в культуре только в клетки хряща, кости, кардиомиоциты и миоциты. Монопотентные стволовые клетки (мышц, жировой ткани, периферических нервов) созревают до одного преобладающего фенотипа клеток.
Стволовые региональные клетки взрослого организма наделены мультипотентностью – пластичной плюрипотентностью, которая сильно варьирует в зависимости от конкретного органа-реципиента. Так, пересадки гематогенных стволовых клеток в мозг, сердечную или скелетную мышцу приводили к образованию тканеспецифичных ростков донорской ткани в органах реципиента. Большое внимание уделяется сегодня мультипотентным МСК взрослых органов, поскольку эти клетки хорошо мигрируют и многократно химеризуют ткани. В свою очередь пересадки нейрональных стволовых клеток в печень, мышцу или иммунную систему сопровождались тканеспецифичной перестройкой фенотипа донорских клеток.
В качестве примера можно назвать следующие типы региональных клеток взрослого организма.
Гематопоэзные стволовые клетки (ГСК): способные производить все клетки крови; находятся в красном костном мозге.
Мышечные стволовые клетки (МСК).
Обонятельные стволовые клетки (ОСК) – дают начало обонятельным клеткам. Располагаются в слизистой оболочке носа.
Стволовые клетки печени (СКП). В нормальном состоянии клетки печени делятся очень медленно, но под влияниям повреждений или инфекции пролиферация клеток усиливается многократно. Выделяют три популяции клеток, способных восстановить печень.
Пищевые цепи и трофические уровни в экосистемах.
Пищевые цепи и пищевая сеть
В функционирующей природной экосистеме не существует отходов. Все организмы, живые или мертвые, потенциально являются пищей для других организмов: гусеница ест листву, дрозд питается гусеницами, ястреб способен съесть дрозда. Когда растения, гусеница, дрозд и ястреб погибают, они в свою очередь перерабатываются редуцентами.
Пищевая цепь – последовательность организмов, в которой каждый из них съедает или разлагает другой. Пищевые цепи – это также движение питательных веществ от продуцентов, консументов (травоядных, плотоядных и всеядных) к редуцентам и обратно к продуцентам.
Все организмы, пользующиеся одним типом пищи, принадлежат к одному трофическому уровню (от греческого слова trophos – «питающиеся»).
Организмы природных экосистем вовлечены в сложную сеть многих связанных между собой пищевых цепей. Такая сеть называется пищевой сетью.
Движение энергии в экосистемах происходит посредством двух связанных типов пищевых сетей: пастбищной и детритной.
В пастбищной пищевой сети живые растения поедаются фитофагами, а сами фитофаги являются пищей для хищников и паразитов.
В детритной пищевой сети отходы жизнедеятельности и мертвые организмы разлагаются детритофагами и деструкторами до простых неорганических соединений, которые вновь используются растениями.
Пирамиды энергетических потоков
С каждым переходом из одного трофического уровня в другой в пределах пищевой цепи или сети совершается работа и в окружающую среду выделяется тепловая энергия, а количество энергии высокого качества, используемой организмами следующего трофического уровня, снижается.
Правило 10% (правило Линдемана)
При переходе с одного трофического уровня на другой 90% энергии теряется, и 10% передается на следующий уровень. Чем длиннее пищевая цепь, тем больше теряется полезной энергии. Поэтому длина пищевой цепи обычно не превышает 4-5 звеньев.
Пирамиды численностей и биомасс
Можно собрать все образцы организмов в экосистеме и подсчитать численность всех видов, обнаруженных на каждом трофическом уровне. Такая информация необходима для создания пирамиды численностей для экосистем.
Обобщенные пирамиды численностей в экосистемах
Сухой вес всех органических веществ, содержащихся в организмах экосистемы, называется биомассой. Каждый трофический уровень пищевой цепи или сети содержит определенное количество биомассы. Ее можно вычислить, если собрать все живые организмы с различных произвольно выбранных участков. Собранные экземпляры необходимо рассортировать по трофическим уровням, высушить и взвесить. Полученные данные в дальнейшем используются для построения пирамиды биомасс для определенной экосистемы.
Обобщенные пирамиды биомасс в экосистемах. Размер каждого слоя пропорционален сухой массе на квадратный метр всех организмов на данном трофическом уровне
Биологической продукцией называют то количество органического вещества, которое создается в единицу времени на определенном трофическом уровне. Различают первичную и вторичную биологическую продукцию. Первичную создают растения из неорганических компонентов. Валовая первичная продукция определяется скоростью фотосинтеза, которая зависит и от вида растений, и от условий среды. Значительную часть валовой первичной продукции (в среднем 50–60%) растения тратят на поддержание собственной жизнедеятельности, а оставшаяся часть идет на рост – увеличение массы. Эту часть, заключенную в созданной биомассе, называют чистой первичной продукцией. За счет чистой первичной продукции в конечном счете и существуют все гетеротрофные организмы биоценоза.
Вторичная биологическая продукция – это органическое вещество, создаваемое гетеротрофами, т.е. переработчиками. Она возникает за счет первичной чистой продукции и, по правилу передачи энергии по цепям питания, составляет не более 10% от растительной. Таким образом, в природе на создание 1 кг массы травоядного животного тратится в 10 раз больше солнечной энергии, чем на создание 1 кг массы растений, а на 1 кг массы хищника – по крайней мере в 100 раз.
В сельском хозяйстве законы передачи энергии по цепям питания выражаются в том известном всем обстоятельстве, что 1 кг пшеницы вырастить гораздо дешевле, чем получить 1 кг говядины или свинины. По этой же причине на мясо не разводят хищных животных, а среди одомашненных растительноядных для этой цели используют в основном тех, которые наиболее эффективно перерабатывают пищу на собственный прирост: кур, индеек, уток, свиней, крупный и мелкий рогатый скот и т.п. Как уже сказано, 10% – это усредненная величина, а конкретные живые организмы могут характеризоваться разной величиной этого показателя. Среди сельскохозяйственных животных, у свиней например, КПД использования 1 кг кормов на прирост 1 кг живой массы может достигать 20% и более. Для других видов, несмотря на старания селекционеров, достичь таких результатов не удается. Фазанов и павлинов разводят почти исключительно в декоративных целях, поскольку доля энергии, использующаяся на прирост, у них составляет всего 2–3%.
Эффективность функционирования начальных звеньев пищевой цепи
В каждую экосистему входят группы организмов разных видов, различимые по способу питания:
автотрофы;
гетеротрофы;
консументы – потребители органического вещества живых организмов;
детритофаги, или сапрофаги, - организмы, питающиеся мертвым органическим веществом – остатками растений и животных;
редуценты – бактерии и низшие грибы – завершают деструктивную работу консументов и сапрофагов, доводя разложение органики до ее полной минерализации и возвращая в среду экосистемы последние порции двуокиси углерода, воды и минеральных элементов.
Все эти группы организмов в любой экосистеме тесно взаимодействуют между собой, согласуя потоки вещества и энергии.
Прослеживая пищевые взаимоотношения между членами биоценоза, можно построить пищевые цепи и пищевые сети питания различных организмов. Различают несколько типов пищевых систем:
пастбищные пищевые цепи (цепи эксплуататоров);
цепи паразитов;
детритные цепи.
Благодаря определенной последовательности пищевых отношений различаются отдельные трофические уровни переноса веществ и энергии в экосистеме, связанные с питанием определенной группы организмов. Так, первый трофический уровень во всех экосистемах образуют продуценты – растения, второй – первичные консументы- фитофаги, третий – вторичные консументы- зоофаги и т.д.
Вход системы – поток солнечной энергии. Часть энергии, поглощенная на первом трофическом уровне растениями, преобразуется фотосинтезом в энергию химических связей углеводов и других органических веществ. Это валовая первичная продукция (ВПП, брутто-продукция) экосистемы. Часть ее веществ окисляется в процессе дыхания растений и освобождает энергию. Эта энергия используется в других биохимических процессах в растении и в конечном счете также рассеивается в виде тепла. Оставшаяся часть новообразованных органических веществ обусловливает прирост биомассы растений – чистую первичную продукцию (ЧПП, нетто-продукцию) экосистемы. Отношение чистой продукции к валовой (коэффициент эффективности фотосинтеза) зависит от типа растительности.
“Правило 1%”: для биосферы в целом доля возможного потребления чистой первичной продукции (на уровне консументов высших порядков) не превышает 1%.
Билет № 15
Иммобилизация ферментов и клеток. Промышленные процессы, основанные на использовании иммобилизованных ферментов и клеток. Тест-методы и биосенсоры.
Что такое вообще иммобилизованные клетки? Иммобилизованными называют такие клетки, для которых созданы искусственные ограничения подвижности во внешней среде, а материальный посредник, обеспечивающий эти ограничения подвижности, считается носителем. В целом система клетка–носитель называется иммобилизованным биокатализатором.
Проблема использования ферментативной активности иммобилизованных микроорганизмов имеет глубокие корни. Более 150 лет назад быстрый способ получения уксуса был основан на применении микроорганизмов, адсорбированных на древесной стружке. В 70-х годах XX в. появились первые научные публикации об иммобилизации клеток микроорганизмов, а первое промышленное применение иммобилизованных клеток было осуществлено в Японии в 1974 г. С их помощью получали аспарагиновую кислоту.
Существуют по меньшей мере четыре области, в которых могут найти применение иммобилизованные ферменты и клетки, а именно: промышленность, охрана окружающей среды, различные анализы и производство лекарственных препаратов. Примерами первой области являются синтез аминокислот, антибиотиков, трансформация стероидов, производство сахарных сиропов и молочных продуктов. К применениям для охраны окружающей среды относятся обработка сточных вод и гидролиз городских, промышленных и сельскохозяйственных стоков, содержащих целлюлозу, гемицеллюлозу и лигнин. Помимо того что эти процессы имеют социальное значение, они выгодны с экономической точки зрения, так как при этом утилизируется энергия в форме метана или этанола.
Использование иммобилизованных клеток позволяет избежать необходимости выделения и очистки требуемых ферментов. Более того, поскольку ферменты функционируют в нативном окружении, их денатурация в процессе работы сводится к минимуму. Еще одним преимуществом использования клеток является также возможность регенерации кофакторов в подходящих условиях. Это расширяет число применяемых ферментов и позволяет осуществлять как процессы синтеза, так и процессы деградации. Кроме того, появляется возможность протекания многостадийных (т.е. последовательных) ферментативных реакций.
Конечно, использование иммобилизованных клеток не лишено недостатков; при этом исследователи сталкиваются с рядом трудностей. Так, например, клеточная стенка, плазматическая или внутриклеточная мембрана могут препятствовать проникновению субстрата к соответствующему ферменту, а также диффузии продукта из клетки. Кроме того, возникает необходимость поддержания целостности клетки и удержания клеток в той фазе роста, в которой синтезируются требуемые ферменты. Наконец, из-за большого числа присутствующих в клетке ферментов (что в ряде случаев рассматривается как достоинство) возможно протекание нежелательных побочных реакций.
Итак, можно подытожить, что иммобилизованные клетки имеют ряд преимуществ как перед иммобилизованными ферментами, так и перед свободными клетками, а именно:
отсутствие затрат на выделение и очистку ферментов;
снижение затрат на выделение и очистку продуктов реакции;
более высокая активность и стабильность;
возможность создания непрерывных и полунепрерывных автоматизированных процессов;
способность к длительному функционированию полиферментных систем без экзогенных кофакторов.
Для иммобилизации могут быть использованы клетки в различном состоянии: живые и поврежденные в той или иной степени. Одностадийные реакции могут осуществлять и живые, и поврежденные клетки. Полиферментные реакции проводят с применением живых клеток, которые могут длительное время регенерировать АТФ и коферменты (НАДФ, НАД).
Различают два направления в исследованиях по иммобилизованным микроорганизмам:
создание катализаторов процессов биотрансформации различных органических соединений;
создание катализаторов для реализации процессов биосинтеза различных органических соединений, в том числе первичных и вторичных метаболитов.
В зависимости от типа клеток и решаемых задач различают следующие виды иммобилизации:
на поверхности носителя;
в массе носителя;
в полимерном геле;
в полимерных пленках;
с использованием мембранных технологий;
с помощью плоских мембран;
с использованием пористых и полых волокон;
с применением микрокапсулирования.
Иммобилизация клеток путем включения в различные гели, мембраны, волокна основана на химических и физических взаимодействиях. Химический метод основан на образовании ковалентных связей с активированным носителем, на поперечной сшивке клеток за счет активных групп в клеточной оболочке с бифункциональными реагентами (например, глутаровым альдегидом). К физическим методам относятся адсорбция и агрегация.
Химические методы используются реже по сравнению с другими методами и малопригодны для иммобилизации живых клеток. Гораздо большее распространение получило включение клеток в состав гелей, мембран и волокон. При таком способе иммобилизации клетки могут сохранять жизнеспособность и в присутствии питательной среды размножаться в приповерхностных слоях гелей.
Наибольшее количество исследований по иммобилизации клеток микроорганизмов проведено японскими исследователями. Особые успехи были достигнуты ими в области синтеза аминокислот, органических кислот и антибиотиков. В Московском государственном университете был разработан метод получения аспарагиновой кислоты, который по эффективности не уступает японским. Клетки E.coli, включенные в армированный полиакриламидный гель, были с успехом использованы для получения аспарагиновой кислоты, период полужизни катализатора – 110 суток. Иммобилизовать можно не только клетки микроорганизмов, но и клетки растительных и животных тканей, используя их для синтеза физиологически активных соединений.
По принципу действия все искусственные твердофазные биокатализаторы на основе микробных клеток разделяются на 4 типа:
Одноферментные системы без кофакторов.
Олигоферментные системы регенерацией разных кофакторов (обычно НАД и НАДН).
Мультиферментные системы с регенерацией нескольких кофакторов.
Мультиферментные системы, катализирующие сложные сиснтетические процессы, непосредственно связанные с основным метаболизмом клетки.
Методы иммобилизации клеток делят на 4 категории:
Иммобилизация клеток или субклеточных органелл в инертном субстрате. Например, клетки Catharanthus roseus, Digitalis lanata в альгинатных, агарозных шариках, в желатине и т.д. Метод предполагает обволакивание клеток одной из различных цементирующих сред – альгинат, агар, коллаген, полиакриламид.
Адсорбция клеток на инертном субстрате. Клетки прилипают к заряженным шарикам из альгината, полистирола, полиакриламида. Метод применялся в экспериментах с животными клетками, а также клетками Saccharomyces uvarum, S. cerevisiae, Candida tropicalis, E. coli.
Адсорбция клеток на инертном субстрате с помощью биологических макромолекул (таких, как лектин). Применяется редко, есть сведения об экспериментах с различными линиями клеток человека, эритроцитами крови барана, адсорбированными на покрытой белком агарозе.
Ковалентное связывание с другим инертным носителем типа КМЦ. Очень редко применяется, известна удачная иммобилизация для Micrococcus luteus. В основном проводились эксперименты по иммобилизации клеток животных и микроорганизмов.
Конструкции реакторов
За исключением некоторых специальных случаев, чаще всего гель, в который включают клетки, состоит из сферических частиц, а не из волокна, мембран или блоков. Одностадийные биопревращения с использованием иммобилизованных ферментов или мертвых клеток осуществляют обычно (1) в проточных реакторах с перемешиванием, (2) в реакторах с псевдоожиженным слоем или (3) в реакторах с полыми волокнами. Каждая из этих систем имеет определенные ограничения в отношении величин перепадов давления и неравномерного распределения катализатора.
Для увеличения площади поверхности и, следовательно, улучшения диффузии (которая в одностадийных реакциях является лимитирующим фактором) применяют малые сферические частицы одинакового размера. Однако, при этом увеличивается перепад давления по длине колонки. Если используют иммобилизованные живые клетки, критическим фактором является диффузия газов, а не других компонентов реакции. Газ, выделяемый живыми клетками, может захватываться шариками, вызывая их всплывание и тем самым снижая их каталитическую активность. В этом случае не следует применять стандартный реактор колоночного типа, так как под давлением выделяющегося газа он может разрушиться.
Физиолого-биохимические особенности иммобилизованных биокатализаторов, их практическое использование
Выбор способа иммобилизации микробных клеток определяется как физиолого-биохимическими особенностями иммобилизованных биокатализаторов, так и стоящими перед исследователем или производственником задачами и осуществляется:
По принципу действия иммобилизованных клеточных систем (так наибольший прогресс отмечается в использовании иммобилизованных клеток как катализаторов биотрансформации).
По масштабам биотехнологического процесса (для проведения процессов «большой» биотехнологии, т.е. крупнотоннажного производства таких продуктов, как аминокислоты, органические кислоты, спирты и т.д.).
По специфике биотехнологического процесса (для очистки сточных вод в биофильтрах – только адсорбционный метод).
Биокаталитическая активность целых иммобилизованных клеток в настоящее время может быть использована в различных отраслях науки и техники:
при биосинтезе и трансформации таких соединений, как аминокислоты, органические кислоты, антибиотики, стероиды углеводы, углеводороды, нуклеотиды и нуклеозиды;
в пивоварении и виноделии;
при очистке сточных и природных вод;
при извлечении металлов из сточных вод;
в биогеотехнологии;
при ассимиляции солнечной энергии;
при изготовлении водородных солнечных элементов;
в азотфиксации;
в аналитических целях при изготовлении биоселективных электродов.
Биомедицинское применение искусственных препаратов, содержащих иммобилизованные ферменты, белки, клетки и другие биологически активные материалы.
Применение ферментов и других физиологически активных веществ (ФАВ) белковой природы в терапии имеет давние традиции. Современная медицина все шире использует высокоочищенные препараты ФАВ белковой природы в самых различных отраслях клинической медицины в качестве перспективных средств медикаментозного лечения вследствие их исключительно высокой активности и специфичности. В настоящее время наметились следующие основные направления энзимотерапии: 1) устранение дефицита ферментов с целью компенсации врожденной или приобретенной функциональной недостаточности; 2) удаление нежизнеспособных, денатурированных структур, клеточных и тканевых осколков; 3) лизис тромбов; 4) комплексная терапия злокачественных новообразований; 5) детоксикация организма.
В настоящее время принято выделять два принципиальных подхода к получению иммобилизованных терапевтических ферментов.
При различных системных поражениях, когда присутствие терапевтического фермента необходимо в разных органах и тканях, целесообразно использовать тем или иным способом стабилизированные водорастворимые препараты иммобилизованных ферментов, обладающие повышенной стабильностью в физиологических условиях и замедленным выведением из организма. Сюда же будут относиться и различные ферментсодержащие искусственные клетки типа микрокапсул, теней эритроцитов или липосом.
2.С другой стороны, для терапии локальных поражений, когда присутствие фермента требуется лишь в месте поражения, целесообразно создание биосовместимых ферментсодержащих полимерных частиц, которые могут быть локализованы в определенном месте и оставаться там заданное время, непрерывно выделяя в окружающую среду терапевтический фермент, предпочтительно дополнительно стабилизированный. Самостоятельный случай – использование иммобилизованных ферментов в аппаратах для экстракорпоральной перфузии типа искусственной почки, в перевязочных и дренирующих материалах для ускорения заживления ран и ожогов и для модификации внутренней поверхности протезов кровеносных сосудов с целью понижения тромбообразования.
Стабилизация терапевтических ферментов в ряде случаев может осуществляться без использования полимерных носителей, просто за счет целенаправленной химической модификации белковой глобулы низкомолекулярными реагентами или за счет введения в глобулу внутримолекулярных скобок из бифункциональных реагентов, затрудняющих денатурационное разворачивание молекулы белка. Этот подход особенно важен, если терапевтический фермент для осуществления своей функции должен провзаимодействовать с рецептором клеточной мембраны (например, пара тромбин–тромбоцит) или проникнуть внутрь клетки (ферменты, применяемые для терапии многочисленных наследственных ферментных недостаточностей печени), а наличие полимерного носителя может резко снизить эффективность ферментного препарата
В ряде случаев применяют межмолекулярное сшивание ферментов бифункциональными реагентами типа глутарового альдегида, что можно также рассматривать как иммобилизацию одной молекулы фермента на другой. Такая модификация фермента приводит к повышению его стабильности и эффективности, например, таким образам удалось стабилизировать альфа-галактозидазу, применяемую для лечения болезни Фабри.
Наиболее распространенным способам получения растворимых стабилизированных ферментных препаратов является их модификация растворимыми полимерами. Наиболее удобны в качестве носителей полисахариды, в частности декстраны, из-за их высокой биосовместимости.
Определенные перспективы открывает использование в качестве носителей природных соединений, которые сами по себе обладают полезной физиологической активностью или способны усиливать действие связанного с ними фермента. Так, для иммобилизации тромболитических ферментов может использоваться антикоагулянт гепарин.
Еще один перспективный метод применения модифицированных форм ферментов для лечения — это создание различного типа искусственных клеток. Исторически первым подходом к этой проблеме было микрокапсулирование ферментов, т.е. их включение в полимерные микрокапсулы, обеспечивающие надежное удержание и защиту фермента и свободное проникновение относительно низкомолекулярных субстратов и продуктов ферментативной реакции.
Основные преимущества микрокапсулирования следующие:
микрокапсула исключает контакт фермента с биологическими жидкостями;
в микрокапсулу могут быть включены относительно высокие концентрации фермента, достижение которых в кровотоке при использовании фермента в нативном виде невозможно;
в микрокапсулу могут включаться различные ферменты одновременно;
фермент в микрокапсулах может быть дополнительно стабилизирован внутри- или межмолекулярным сшиванием или модификацией растворимыми полимерами.
Вторым по старшинству методом создания искусственных клеток является включение ферментов в липосомы – искусственные фосфолипидные микропузырьки. Ферменты, включенные в липосомы, также предохранены от инактивирующего воздействия внешней среды, а сами липосомы, состоящие из природных соединений, полностью утилизуются в организме. В отличие от микрокапсул, однако, липосомы обладают уникальной способностью доставлять включений в них препарат внутрь клеток, с которыми они взаимодействуют по механизму слияния или эндоцитоза.
Еще одна большая область применения ферментов в медицине, которая открылась только в результате разработки методов их иммобилизации, – это использование иммобилизованных ферментов в различных экстракорпоральных аппаратах для перфузионной очистки различных биологических жидкостей. Частным случаем этого общего подхода является создание ферментных реакторов, которые могут использовать как тромбобезопасные протезы кровеносных сосудов.
Основными преимуществами реакторов на основе иммобилизованных ферментов являются следующие:
возможность избежать непосредственного контакта организма с чужеродным белком и таким образом уменьшить нежелательные реакции на этот белок;
возможность многократного использования реактора;
возможность проведения долговременного лечения.
К недостаткам таких реакторов следует отнести не до конца решенные проблемы тромбообразования или сорбции белков крови на чужеродных поверхностях.
Биосенсоры – это аналитические устройства, использующие биологические материалы (ферменты, ткани, бактерии, дрожжи, антигены / антитела, липосомы, органеллы, рецепторы, ДНК) для "узнавания" определенных молекул и выдающие информацию об их присутствии и количестве в виде электрического сигнала.
Микроэволюция и макроэволюция. Градуализм и сальтации.
Градуализм и пунктуализм
Хотя сам факт биологической эволюции давно признан биологами и не вызывает ни малейших сомнений, многие ключевые вопросы эволюционной теории до сих пор остаются спорными. Одним из самых острых вопросов такого рода является вопрос о равномерности темпов эволюции. Сам Дарвин, как и многие его последователи, видели эволюцию как процесс в основном плавный, постепенный. Когда в результате синтеза классического дарвинизма с генетикой и молекулярной биологией родилась синтетическая теория эволюции, эта точка зрения (градуализм) значительно укрепилась. Главным, даже единственным источником наследственной изменчивости стали считать случайные мутации — ошибки при копировании ДНК. Многие исследователи полагали, что, поскольку мутационный процесс совершенно случаен и ненаправлен, то и идти он должен примерно с одинаковой скоростью у всех живых организмов. Это предположение легло в основу принципа «молекулярных часов», который активно используется и по сей день.
Альтернативой градуализму является пунктуализм, или теория прерывистого равновесия, сформулированная в 1972 году Стивеном Гоулдом (Stephen Jay Gould, 1941-2002) и Нильсом Элдриджем (Niles Eldredge, р. 1943). Эта концепция предполагает, что в эволюции видов чередуются длительные периоды стабильности, когда основные черты вида сохраняются неизменными, и короткие периоды быстрых изменений, в ходе которых вид преобразуется — либо целиком превращается в другой вид, либо делится на два или более новых вида, либо «отпочковывает» их от себя. Точка зрения пунктуалистов, основанная на обширном палеонтологическом материале, имеет и достаточно веские теоретические обоснования. В самых общих чертах их можно свести к следующему. Вид представляет собой относительно устойчивую самоподдерживающуюся систему. Чтобы на месте старой системы возникла новая, старая должна быть разрушена. Нужна некая «встряска», приводящая к разрушению внутренних связей, к дестабилизации.
С равнительная
характеристика теории филетического
градуализма (вверху) с теорией прерывистого
равновесия (внизу): прерывистое равновесие
достигается за счёт быстрых изменений
в морфологии.
равнительная
характеристика теории филетического
градуализма (вверху) с теорией прерывистого
равновесия (внизу): прерывистое равновесие
достигается за счёт быстрых изменений
в морфологии.
Британские биологи придумали удивительно простую методику, позволяющую разрешить давний спор между приверженцами теории постепенной эволюции (градуализм) и сторонниками скачкообразной эволюции (пунктуализм). Оказалось, что соотношение градуалистической и пунктуалистической составляющих эволюционного процесса можно оценить количественно, сопоставив длины ветвей «эволюционных деревьев» — стандартных реконструкций эволюционного развития различных групп организмов, которые строятся на основе сравнения нуклеотидных последовательностей ДНК. Проанализировав деревья, построенные для 122 групп, ученые пришли к выводу, что в среднем 22% различий в ДНК возникает во время кратких периодов интенсивного видообразования, а остальные 78% постепенно накапливаются во время долгих «градуалистических» периодов. Скачкообразность эволюции в большей мере свойственна растениям и грибам и в меньшей — животным.
Поначалу споры градуалистов с пунктуалистами были довольно бурными, но сегодня эти две концепции довольно мирно уживаются в пределах единой развивающейся эволюционной теории. Они справедливо считаются не противоречащими друг другу, а взаимодополнительными, и быстро обрастают всевозможными примерами, уточнениями, дополнениями и обоснованиями. Большинство специалистов признают, что эволюция иногда может идти по пунктуалистическому, иногда — по градуалистическому сценарию.
По своей сути пунктуализм отнюдь не эквивалентен сальтационизму, вообще отрицающему наличие переходов между видами. Однако, как ни странно, это отличие не всегда улавливается, и многие сальтационисты объявили себя сторонниками пунктуалистской концепции, которая быстро завоевала исключительно широкую популярность.
Билет № 16
Версии происхождения эвкариот. Вероятные предшественники с учетом имеющихся в клетке эвкариот геномов.
Эволюции клеточных органелл и происхождение эукариот с позиций геномики.
В последнее десятилетие с помощью молекулярно-биологических подходов получены убедительные доказательства того, что все живые существа должны быть разделены на три надцарства (домена): бактерии, археи и эукариоты. Причем первые два домена - бактерии и археи - являются прокариотами. С помощью молекулярно-биологических методов были получены весомые доказательства в пользу того, что бактерии и археи возникли на Земле от общего предка - так называемого прогенота - около 4 млрд лет назад, а эукариоты имеют более позднее происхождение. По данным палеонтологов, эукариоты, в частности дрожжеподобные организмы, появились на Земле примерно через 500 млн лет после прокариот. Причем, по современным представлениям, в возникновении эукариотических клеток, скорее всего, участвовали как бактерии, так и археи.
Наиболее существенные доказательства происхождения важнейших органелл эукариотических клеток - хлоропластов и митохондрий из прокариот получены в последние годы при изучении структуры одного из наиболее консервативных (в отношении возможности изменений в процессе эволюции) компонентов живых клеток - рибосомальных РНК. Выдающийся американский молекулярный биолог К. Воз с сотрудниками показал уже в 1980-х гг., что структура так называемой 16S РНК из рибосом хлоропластов растений совершенно непохожа на соответствующую ей 18S РНК из цитоплазматических рибосом растений и почти идентична структуре аналогичной РНК из некоторых цианобактерий. Эта группа исследователей также установила, что 16S РНК рибосом, полученных из митохондрий разных эукариотических организмов, непохожа по своей структуре на 16S РНК рибосом из цитозоля тех же самых биологических объектов, но чрезвычайно схожа с 16S РНК некоторых бактерий, в частности бактерий рода Paracoccus. Интересно, что и набор дыхательных ферментов указанной бактерии очень похож на "дыхательный ансамбль" митохондрий животных.
Вопрос О ПРИРОДЕ КЛЕТКИ-ХОЗЯИНА в этом эндосимбиозе до сих пор остается дискуссионным. Ведь клетки эукариот обладают хорошо сформированным ядром, имеющим оболочку, а прокариоты такого ядра не имеют. Вместе с тем Л. Маргелис, например, считает, что роль хозяйских клеток, возможно, сыграли прокариоты - предшественники современных бактерий, относящиеся к микоплазмам (очень примитивно построенным прокариотам, практически лишенным клеточных стенок).
Предположительная схема происхождения эукариот путем многократного симбиоза аэробных и анаэробных, фотосинтезирующих и нефотосинтезирующих прокариотических организмов, рассмотрена Альбертсом, Уотсоном и др. (1986). На этой гипотетической схеме все как бы понятно, но остается неясным, откуда же или по крайней мере когда возникает клеточное ядро.
последнее время появились и широко обсуждаются работы японского исследователя Т. Ошимы. На основании тщательного изучения структуры рибосомных 16S РНК многих про- и эукариот, в том числе и многих представителей до сих пор малоизученного надцарства архей, этот автор приходит к выводу, что хозяйской клеткой являлся один из предков современных архей. Кстати, следует сказать, что у представителей именно этого надцарства (в отличие от бактерий) имеется очень много общих с эукариотами биохимических и молекулярно-биологических особенностей. На слудующем рисунке представлена схема происхождения эукариотических клеток по Ошиме (1994).
В его последних работах приводятся доводы в пользу того, что хозяйской клеткой при возникно-вении эукариот являлся предок архей, подобный одному из современных представителей этих древних прокариот - термоплазме.
Биоэтика и клонирование.
Биоэтика – комплексное понятие, которое в широком смысле относится к исследованию социальных, экологических, медицинских и социально-правовых проблем, касающихся не только человека, но и любых живых организмов, включенных в экосистемы, окружающие человека.
В узком смысле термин «биоэтика» обозначает весь круг этических проблем во взаимодействии врача и пациента. Неоднозначные ситуации, постоянно возникающие в практической медицине в результате прогресса биологической науки и медицинского знания, требуют постоянного обсуждения как в медицинском сообществе, так и в кругу широкой общественности.
Первоначально биоэтика представляла собой попытку выработать стандарты поведения медицинских профессионалов и юристов в спорных вопросах современной медицины. Со временем содержание нового термина расширилось, и в настоящее время биоэтика – область междисциплинарных исследований этических, философских и антропологических проблем, возникающих в связи с прогрессом биомедицинской науки и внедрением новейших технологий в практику здравоохранения.
Развитие биоэтики обусловлено тем, что в современном мире медицина претерпевает процесс грандиозных преобразований. Она становится качественно иной, не только более технологически оснащенной, но и более чувствительной к правовым и этическим аспектам врачевания. Этические принципы для новой медицины хотя и не отменяют полностью, но радикально преобразуют основные положения «Клятвы Гиппократа», которая на протяжении веков была эталоном врачебной морали. Традиционные ценности милосердия, благотворительности, ненанесения вреда пациенту и другие получают в новой культурной ситуации новое значение и звучание. Именно это и определяет содержание биоэтики.
Проблемы биоэтики
К основным в биоэтике можно отнести следующие проблемы:
• защиты прав пациентов (в том числе ВИЧ инфицированных, психиатрических больных, детей и др. больных с ограниченной компетентностью);
• справедливости в здравоохранении;
• взаимоотношения с живой природой (экологические аспекты развития биомедицинских технологий);
• аборта, контрацепции и новых репродуктивных технологий (искусственное оплодотворение, оплодотворение «в пробирке» с последующей имплантацией эмбриона в матку, суррогатное материнство);
• проведения экспериментов на человеке и животных;
• выработки критериев диагностики смерти;
• трансплантологии;
• современной генетики (генодиагностики, генной терапии и инженерии);
• манипуляций со стволовыми клетками;
• клонирования (терапевтического и репродуктивного);
• оказания помощи умирающим пациентам (хосписы и организации паллиативной помощи);
• самоубийства и эвтаназии (пассивной или активной, добровольной или насильственной).
В ЮНЕСКО действуют два комитета по биоэтике — международный и межправительственный. В Совете Европы этой тематикой занимается Руководящий комитет по биоэтике. Рабочая группа по биоэтике существует и в рамках Всемирной Организации Здравоохранения.
Этическое и правовое регулирование в области Б. осуществляется на основе международных нормативных документов. Важнейшие из них: Всеобщая декларация о геноме человека и правах человека (ЮНЕСКО, 1997); Всеобщая декларация о биоэтике и правах человека (ЮНЕСКО, 2005); Декларация о клонировании человека (ООН, 2005); юридически обязывающая Конвенция о защите прав и достоинства человека в связи с применением достижений биологии и медицины: Конвенция о правах человека и биомедицине (Совет Европы, 1997) и дополнительные протоколы к ней, касающиеся запрета клонирования человека, трансплантологии, биомедицинских исследований. Высоким международным авторитетом пользуется такой документ, как Хельсинкская декларация Всемирной медицинской организации (1964, последняя редакция — 2000) «Этические принципы проведения научных медицинских исследований с участием человека».
Технологические трудности и ограничения
Самым принципиальным ограничением является невозможность повторения сознания, а это значит, что речь не может идти о полной идентичности личностей, как это показывается в некоторых кинофильмах, но только об условной идентичности, мера и граница которой ещё подлежит исследованию, но для опоры за базис берётся идентичность однояйцевых близнецов. Невозможность достичь стопроцентной чистоты опыта обуславливает некоторую неидентичность клонов, по этой причине снижается практическая ценность клонирования.
Социально-этический аспект
Опасения вызывают такие моменты, как большой процент неудач при клонировании и связанные с этим возможности появления людей-уродов. А также вопросы отцовства, материнства, наследования, брака и многие другие.
Этико-религиозный аспект
С точки зрения основных мировых религий (христианство, ислам, иудаизм) клонирование человека является или проблематичным актом или актом, выходящим за рамки вероучения и требующим у богословов чёткого обоснования той или иной позиции религиозных иерархов.
Ключевым моментом, который вызывает наибольшее неприятие, является здесь тот факт, что для получения клона одного человека необходимо убить находящийся на самой ранней стадии развития, но уже начавший формироваться эмбрион другого человеческого зародыша.
Отношение в обществе
Большинство аналитиков сходится в том, что клонирование в той или иной форме уже стало частью нашей жизни. Но прогнозы касательно клонирования человека высказываются достаточно осторожно.
Ряд общественных организаций (Российское трансгуманистическое движение, WTA) выступает за снятие ограничений на терапевтическое клонирование.
Биологическая безопасность
Обсуждаются вопросы биологической безопасности клонирования человека. Такие как: долгосрочная непредсказуемость генетических изменений, опасность утечки технологий клонирования в криминальные или/и международные террористические структуры.
Законодательство о клонировании человека
В некоторых государствах использование данных технологий применительно к человеку официально запрещено — Франция, Германия, Япония. Эти запреты, однако, не означают намерения законодателей названных государств воздерживаться от применения клонирования человека в будущем, после детального изучения молекулярных механизмов взаимодействия цитоплазмы ооцита-реципиента и ядра соматической клетки-донора, а также совершенствования самой техники клонирования.
1996—2001
Единственный международный акт, устанавливающий запрет клонирования человека, — Дополнительный Протокол [7] к Конвенции о защите прав человека и человеческого достоинства в связи с применением биологии и медицины, касающийся запрещения клонирования человеческих существ, который подписали 12 января 1998 г. 24 страны из 43 стран-членов Совета Европы. 1 марта 2001 г. после ратификации 5 странами этот Протокол вступил в силу.
2005
19 февраля 2005 г. Организация Объединённых Наций призвала страны-члены ООН принять законодательные акты, запрещающие все формы клонирования, так как они «противоречат достоинству человека» и выступают против «защиты человеческой жизни». Декларация ООН о клонировании человека [8], принятая резолюцией 59/280 Генеральной Ассамблеи от 8 марта 2005 г., содержит призыв к государствам-членам запретить все формы клонирования людей в такой мере, в какой они несовместимы с человеческим достоинством и защитой человеческой жизни.
В ходе дискуссии на уровне ООН рассматривалось несколько вариантов декларации: Бельгия, Британия, Япония, Южная Корея, Россия и ряд других стран предлагали оставить вопрос о терапевтическом клонировании на усмотрение самих государств; Коста-Рика, США, Испания и ряд других выступили за полный запрет всех
Уголовная ответственность
В настоящее время в мире активно развернулся процесс криминализации клонирования человека. В частности, такие составы включены в новые уголовные кодексы Испании 1995 г., Сальвадора 1997 г., Колумбии 2000 г., Эстонии 2001 г., Мексики (федеральный округ) 2002 г., Молдовы 2002 г., Румынии 2004). В Словении соответствующая поправка в УК внесена в 2002 г., в Словакии — в 2003 г.
Во Франции дополнения в Уголовный кодекс, предусматривающие ответственность за клонирование, были внесены в соответствии с Законом о биоэтике от 6 августа 2004 г.
В некоторых странах (Бразилия, Германия, Великобритания, Япония) уголовная ответственность за клонирование установлена специальными законами. Так, например, Федеральный закон ФРГ о защите эмбрионов 1990 г. называет преступлением создание эмбриона, генетически идентичного другому эмбриону, происходящему от живого или мертвого лица.
В Великобритании соответствующие уголовные нормы содержит Закон о репродуктивном клонировании человека 2001 г. (Human Reproductive Cloning Act 2001), который предусматривает санкцию в виде 10 лет лишения свободы. При этом терапевтическое клонирование человека разрешено.
В США запрет на клонирование впервые был введен ещё в 1980 г. В 2003 г. Палата представителей Конгресса США приняла закон (Human Cloning Prohibition Act of 2003), по которому клонирование, нацеленное как на размножение, так и на медицинские исследования и лечение, рассматривается как преступление с возможным 10-летним тюремным заключением и штрафом в 1 млн долларов. В январе 2009 года запрет на терапевтическое клонирование был снят[3].
В Японии парламентом 29 ноября 2000 г. был принят «Закон, регулирующий применение технологии клонирования человека и других сходных технологий», содержащий уголовные санкции.
Клонирование человека в России
Хотя Россия и не участвует в вышеуказанных Конвенции и Протоколе, она не осталась в стороне от мировых тенденций, ответив на вызов времени принятием Федерального закона «О временном запрете на клонирование человека» от 20 мая 2002. Как было указано в его преамбуле, закон вводил временный (сроком на пять лет) запрет на клонирование человека, исходя из принципов уважения человека, признания ценности личности, необходимости защиты прав и свобод человека и учитывая недостаточно изученные биологические и социальные последствия клонирования человека. С учетом перспективы использования имеющихся и разрабатываемых технологий клонирования организмов, предусматривается возможность продления запрета на клонирование человека или его отмены по мере накопления научных знаний в данной области, определения моральных, социальных и этических норм при использовании технологий клонирования человека.
Под клонированием человека в Законе понимается «создание человека, генетически идентичного другому живому или умершему человеку, путем переноса в лишенную ядра женскую половую клетку ядра соматической клетки человека», то есть речь идет только о репродуктивном, а не терапевтическом клонировании.
Однако в конце марта 2010 г. запрет на клонирование человека в России был продлён.
Новый законопроект вносит в федеральный закон «О временном запрете на клонирование человека» поправки, продлевающие мораторий на клонирование на неопределенный срок — до вступления в силу закона, устанавливающего порядок применения биотехнологий в этой области.
Причина запрета указывается в пояснительной записке к законопроекту: «Клонирование человека встречается с множеством юридических, этических и религиозных проблем, которые на сегодняшний день еще не имеют очевидного разрешения».
В новом законе оговорено, что клонирование других организмов, а также любых клеток, в том числе человеческих, в исследовательских целях не запрещено. [10]
Клонирование человека в Австралии
В декабре 2006 года в Австралии был снят запрет на клонирование человеческого эмбриона. Но использование эмбрионов, не пригодившихся при экстракорпоральном оплодотворении, а также создание и использование других эмбрионов в исследованиях, запрещено законодательством Австралии. Под запретом находится и клонирование человека в репродуктивных целях.
В сентябре 2008 года правительство Австралии выдало лицензию, разрешающую ученым создавать клонированные эмбрионы человека для получения эмбриональных стволовых клеток.[18]
Билет № 17
Современный взгляд на проблемы коммуникации в физиологии и психологии. Когнитивная психология как интегративная наука.
Современное состояние научной разработки проблемы коммуникации в физиологии и психологии.
Психофизиология как наука. Психофизиология – пограничная область психологии, изучающая роль всей совокупности биологических свойств, прежде всего, свойств нервной системы, в детерминации психической деятельности и устойчивых индивидуально-психологических различий. Главная задача – причинное объяснение психических явлений путем раскрытия лежащих в их основе нейрофизиологических механизмов.
Психофизиология включает несколько областей исследования, к которым отностся:
Психофизиология ощущений и восприятий, изучающая нервные процессы в анализаторах, начиная с рецепторов и кончая корковыми отделами. Установлены специфические аппараты цветового зрения, специфические рецепторы и проводящие пути тактильной и болевой чувствительности, открыты нейроны, реагирующие на отдельные свойства зрительных и слуховых стимулов.
Психофизиология речи и мышления, которая изучает функциональную роль разных областей мозга и их взаимосвязей в осуществлении речевых процессов. Принципиально важным стало установление тесной связи мыслительных процессов с деятельностью речедвигательного анализатора.
Психофизиология эмоций, исследующая нейрогуморальные механизмы возникновения эмоциональных состояний. Открыты нервные "центры" удовольствия и неудовольствия, расположенные в подкорковых областях мозга. Установлено, что важная роль в эмоциональном поведении принадлежит гормонам, выделяемым железами внутренней секреции (гипофизом, корой и мозговым слоем надпочечников и др.), а также различными биологически активными веществами.
Психофизиология внимания, исследующая нейрофизиологические корреляты внимания (изменение электроэнцефалограммы и вызванных потенциалов), изменение кожно-гальванической и др. реакций). Психофизиология внимания тесно связана с проблемами изучения ориентировочного рефлекса и второй сигнальной системы.
Психофизиология произвольных действий, которая вскрывает физиологическую структуру и механизмы их осуществления.
Дифференциальная психофизиология, изучающая зависимость индивидуальных особенностей психики и поведения от индивидуальных различий в деятельности мозга. В развитии дифференциальной психофизиологии В.М.Русалов выделяет четыре этапа: допавловский, павловский (с 1927 г.), тепловско-небылицинский (с 1956 г.) и современный (с 1972 г.). Последний связан прежде всего с развитием системных представлений в психофизиологии.
В арсенале психофизиологии сосредоточены разнообразные методы исследования:
работы головного мозга;
электрической активности кожи;
работы сердечно-сосудистой системы;
активности мышечной системы;
активности дыхательной системы;
реакции глаз;
использования детектора лжи (рисунок 1).
Методы изучения работы головного мозга. Электроэнцефалография (ЭЭГ) – метод регистрации и анализа электроэнцефалограммы, т.е. суммарной биоэлектрической активности, отводимой как со скальпа, так и из глубоких структур мозга.
Основные ритмы и параметры энцефалограммы:
альфа-волна – одиночное двухфазовое колебание разности потенциалов длительностью 75–125 мс.; по форме приближается к синусоидальной;
альфа-ритм – ритмическое колебание потенциалов с частотой 8-13 Гц, выражен чаще в задних отделах мозга при закрытых глазах в состоянии относительного покоя; средняя амплитуда 30–40 мкВ, обычно модулирован в веретена;
бета-волна – одиночное двухфазовое колебание потенциалов длительностью менее 75 мс и амплитудой 10–15 мкВ (не более 30);
бета-ритм – ритмическое колебание потенциалов с частотой 14-35 Гц. Лучше выражен в лобно-центральных областях мозга;
дельта-волна – одиночное двухфазовое колебание разности потенциалов длительностью более 250 мс;
дельта-ритм – ритмическое колебание потенциалов с частотой 1–3 Гц и амплитудой от 10 до 250 мкВ и более;
тета-волна – одиночное, чаще двухфазовое колебание разности потенциалов длительностью 130–250 мс;
тета-ритм – ритмическое колебание потенциалов с частотой 4–7 Гц, чаще двухсторонние синхронные, с амплитудой 100–200 мкВ, иногда с веретенообразной модуляцией, особенно в лобной области мозга.
Магнитоэнцефалография (МЭГ) – регистрация параметров магнитного поля, обусловленных биоэлектрической активностью головного мозга.
Вызванные потенциалы (ВП) – биоэлектрические колебания, возникающие в нервных структурах в ответ на внешнее раздражение и находящиеся в строго определенной временной связи с началом его действия.
Топографическое картирование электрической активности мозга (ТКЭАМ) – область электрофизиологии, оперирующая множеством количественных методов анализа электроэнцефалограммы и вызванных потенциалов.
Компьютерная томография (КТ) – новейший метод, обеспечивающий точные и детальные изображения малейших изменений плотности мозгового вещества. КТ соединила в себе последние достижения рентгеновской и вычислительной техники, отличаясь принципиальной новизной технических решений и математического обеспечения.
Ядерно-магнитно-резонансная томография мозга. Компьютерная томография стала родоночальницей ряда более совершенных методов исследования: томографии с использованием эффекта ядерного магнитного резонанса (ЯМР-томография), позитронной эмиссионной томографии (ПЭТ), функционального магнитного резонанса (ФМР).
Электрическая активность кожи. Возникновение электрической активности кожи, или кожно-гальванической реакции (КГР) обусловлено, главным образом, активностью потовых желез в коже человека, контролируемых симпатической нервной системой.
Показатели работы сердечно-сосудистой системы включают целый ряд методов: электрокардиограмму (ЭКГ) – запись электрических процессов, связанных с сокращением сердечной мышцы, плетизмографию – метод регистрации сосудистых реакций организма.
Показатели активности мышечной системы – это электромиография – метод исследования функционального состояния органов движения путем регистрации биопотенциалов мышц.
Показатели активности дыхательной системы. Для измерения интенсивности (амплитуды и частоты) дыхания используют специальный прибор – пневмограф. Этот метод обеспечивает хорошую запись изменений частоты и амплитуды дыхания.
Р исунок
1 – Детектор лжи
исунок
1 – Детектор лжи
Примечание. Это условное название прибора полиграфа, одновременно регистрирующего комплекс физиологических показателей (КГР, ЭЭГ, плетизмограмму и др.) с целью выявления динамики эмоционального напряжения.
Реакции глаз. Для психофизиолога наибольший интерес представляют три категории глазных реакций: сужение и расширение зрачка, мигание и глазные движения:
пупиллометрия – метод изучения зрачковых реакций;
мигание (моргание) – периодическое смыкание век;
движение глаз – разнообразные по функции, механизму и биомеханике вращения глаз в орбитах;
электроокулография – метод регистрации движения глаз, основанный на графической регистрации изменения электрического потенциала сетчатки и глазных мышц.
Понятие о когнитивной психологии. Когнитивная психология (латинское cognitio – знание, познание) – направление в психологии, возникшее в США в конце 50-х – начале 60-х гг. XX в. в противовес бихевиоризму. Возникновению бихевиоризма способствовали разработки в области условных рефлексов и развитие зоопсихологии. Бихевиоризмом не принимались во внимание врожденные качества человека, его убеждения и другие личностные качества, основой всего считалось поведение. Развитие когнитивной психологии стало возможным благодаря предшествовавшим работам в области гештальтпсихологии, привлекшим внимание к вопросам восприятия и эффективному творческому мышлению, исследование которого является одной из основных задач науки. Когнитивная психология во многом основывается на аналогии между преобразованием информации в вычислительном устройстве и осуществлением познавательных процессов у человека – для пояснения этой аналогии было введено понятие компьютерной метафоры. Когнитивная система человека рассматривается как комплекс, имеющий устройства ввода, хранения и вывода информации. Информация, достигшая когнитивной системы, преобразуется, обрабатывается, кодируется, хранится, запоминается и забывается, а затем преобразуется в знание. Методологическая платформа когнитивной психологии основана на компьютерных технологиях и новых теоретических исследованиях в области психологии.
Весь описанный эпизод занял бы не более двух минут, но то количество информации, которую восприняли и проанализировали эти два человека, просто поражает. Как должен психолог рассматривать такой процесс? Один выход – это просто на языке «стимул–реакция» (S-R): например, светофор (стимул) и поворот налево (реакция). Некоторые психологи, особенно представители традиционного бихевиористского подхода уверены, что всю последовательность событий можно адекватно (и гораздо более детально) описать в таких терминах. Однако, хотя эта позиция и привлекает своей простотой, она не в состоянии описать те когнитивные системы, которые участвуют в подобном обмене информацией. Чтобы это сделать, необходимо определить и проанализировать конкретные компоненты когнитивного процесса и затем объединить их в большую когнитивную модель.
Восприятие. Отрасль психологии, непосредственно связанная с обнаружением и интерпретацией сенсорных стимулов, называется психологией восприятия. Из экспериментов по восприятию мы хорошо знаем о чувствительности человеческого организма к сенсорным сигналам и о том, как интерпретируются эти сенсорные сигналы. Описание, данное полицейским в приведенной уличной сцене, значительно зависит от его способности «видеть» существенные признаки окружения.
Распознавание образов. Стимулы внешней среды не воспринимаются как единичные сенсорные события; чаще всего они воспринимаются как часть более значительного паттерна (так в психологии называют набор сенсорных стимулов, принадлежащих одному классу объектов). То, что мы ощущаем (видим, слышим, обоняем или чувствуем вкус), почти всегда есть часть сложного паттерна. Так, когда полицейский говорит водителю «проехать через железнодорожный переезд мимо озера… рядом со старой фабрикой», его слова описывают сложные объекты (переезд, озеро, старая фабрика). В какой-то момент полицейский описывает плакат и предполагает при этом, что водитель грамотный.
Внимание. Полицейский и водитель сталкиваются с несметным количеством признаков окружения. Если бы водитель уделял внимание им всем (или почти всем), он никогда бы не добрался до хозяйственного магазина. Хотя люди – это существа, собирающие информацию, очевидно, что в нормальных условиях мы очень тщательно отбираем количество и вид информации, которую стоит принимать в расчет.
Память. Мог бы полицейский описать дорогу, не пользуясь памятью? Вряд ли. В нашем примере ответ полицейского стал результатом работы двух типов памяти. Первый тип – кратковременная память (КВП) удерживает информацию ограниченное время, пока ее не заменит новая – достаточно долго, чтобы поддержать разговор. C другой стороны, значительная часть содержания ответов полицейского получена из его долговременной памяти (ДВП). Наиболее очевидная часть здесь – знание им языка. Он не называет озеро лимонным деревом, место выставок – автопокрышкой, а улицу – баскетболом; он извлекает слова из своей ДВП и использует их более-менее правильно.
Воображение. Для того, чтобы ответить на вопрос, полицейский построил мысленный образ окружения. Этот мысленный образ имел форму когнитивной карты: т.е. мысленного представления множества зданий, улиц, дорожных знаков, светофоров и т.п. Он был способен извлечь из этой когнитивной карты значимые признаки, расположить их в осмысленной последовательности и преобразовать в языковую информацию, которая позволила бы водителю построить сходную когнитивную карту. Эта когнитивная карта дала бы водителю вразумительную картину города, которая могла быть преобразована в акт вождения автомобиля по определенному маршруту.
Язык. Чтобы правильно ответить на вопрос, полицейскому нужны были обширные знания языка. Это подразумевает знание правильных названий для ориентиров и, что тоже важно, знание синтаксиса языка — т.е. правил расположения слов и связей между ними. Приведенные словесные последовательности могут не удовлетворить педантичного профессора филологии, но вместе с тем они передают некоторое сообщение. Почти в каждом предложении присутствуют существенные грамматические правила. Полицейский не сказал: «них ну это хозяйственном в у»; он сказал: «Ну, это у них в хозяйственном», – и мы можем понять, что имеется в виду.
Психология развития. Это еще одна область когнитивной психологии, которая весьма интенсивно изучалась. Недавно опубликованные теории и эксперименты по когнитивной психологии развития значительно расширили наше понимание того, как развиваются когнитивные структуры. В нашем случае мы можем только заключить, что говорящих объединяет такой опыт развития, который позволяет им (более или менее) понимать друг друга.
Мышление и формирование понятий. На протяжении всего приведенного эпизода полицейский и водитель проявляют способность к мышлению и формированию понятий. Когда полицейского спросили, как попасть в «Плати-Пакуй», он ответил после некоторых промежуточных пояснений: вопрос полицейского «Вы знаете, где цирк?» показывает, что если бы водитель знал этот ориентир, то его легко можно было бы направить в «Плати-Пакуй». Но раз он не знал, полицейский выработал еще один план ответа на вопрос. Наконец, употребление им некоторых слов (таких как «железнодорожный переезд», «старая фабрика», «железная ограда») свидетельствует, что у него были сформированы понятия, близкие к тем, которыми располагал водитель.
Человеческий интеллект. И полицейский, и водитель имели некоторые предположения об интеллекте друг друга. Эти предположения включали — но не ограничивались этим — способность понимать обычный язык, следовать инструкциям, преобразовывать вербальные описания в действия и вести себя соответственно законам своей культуры.
Искусственный интеллект. В нашем примере нет непосредственной связи с компьютерными науками; однако специальная сфера компьютерных наук, именуемая «Искусственный интеллект» (ИИ) и моделирующая познавательные процессы человека, оказала огромное влияние на развитие когнитивной науки – особенно с тех пор, как для компьютерных программ ИИ потребовались знания о том, как мы обрабатываем информацию. Соответствующая и весьма захватывающая тема затрагивает вопрос: может ли «совершенный робот» имитировать человеческое поведение? Как бы ответил на вопрос водителя сверхробот, овладевший всеми способностями человека, связанными с восприятием, памятью, мышлением и языком? Если бы робот был идентичен человеку, то и ответы его были бы идентичны. Но как разработать программу, которая ошиблась бы – так же, как это сделал полицейский («вы поворачиваете налево»), – и затем, заметив эту ошибку, исправила бы ее («нет, направо»)?!
Получение и использование трансгенных организмов. Генетически модифицированные организмы. Проблемы биобезопасности.
Основой «зеленой» биотехнологии является генная, или генетическая инженерия, – совокупность приемов, методов и технологий получения ре-комбинантных РНК и ДНК, выделения генов из организма (клеток) или биохимического синтеза генов на основе знания об их строении, осуществления манипуляций с генами и введения их в другие организмы, – имеющая своим результатом создание генетически модифицированных организмов (ГМО). Рекомбинантная ДНК – это искусственно созданная человеком последовательность ДНК, части которой синтезируются химическим путем с помощью полимеразной цепной реакции (ПЦР) или клонируются из ДНК различных организмов. Эти рекомбинантные ДНК встраивают в состав бактериальных плазмид или вирусных векторов, которыми затем трансформируют клетки живых организмов (микроорганизмов, растений, животных). Генетически модифицированные животные и растения обычно содержат рекомбинантные гены, встроенные непосредственно в их хромосомы.
В технологии рекомбинантных ДНК используются следующие методы:
• специфическое расщепление ДНК рестрицирующими нуклеазами, ускоряющее выделение и манипуляции с отдельными генами;
• изучение нуклеотидной последовательности (секвенирование) в очищен-ном фрагменте ДНК, что позволяет определить границы гена, его струк-турные элементы и аминокислотную последовательность, кодируемую этим геном;
• конструирование рекомбинантной ДНК;
• гибридизация нуклеиновых кислот, позволяющая выявлять специфиче-ские последовательности РНК или ДНК с большой точностью и чувстви-тельностью, основанная на их способности связывать комплементарные последовательности нуклеиновых кислот;
• клонирование ДНК: амплификация in vitro с помощью полимеразной цепной реакции (ПЦР) или введение фрагмента ДНК в бактериальную клетку, которая после такой трансформации воспроизводит этот фрагмент в миллионах копий;
• введение рекомбинантной ДНК в клетки или организмы (трансформа-ция).
Методом генной инженерии уже получен ряд препаратов медицин-ского назначения, в том числе инсулин человека и противовирусный препарат интерферон путем создания рекомбинантных плазмид, несущих соответствующие целевые гены. Поскольку плазмидная ДНК представляет собой замкнутую кольцевую молекулу, кольцо сначала разрывают, чтобы его свободные концы были в химическом отношении реакционноспособными. Это достигается с помощью различных ферментов, называемых нуклеазами (рестриктазами). Затем фрагменты ДНК соединяют с помощью лигаз – ферментов, исправляющих повреждения в ДНК и сшивающих концы ее разорванных нитей. Именно таким путем на заре генной инженерии плазмиды из штамма Esherichia coli, устойчивого к тетрациклину, и плазмиды из штамма, устойчивого к другому антибиотику, канамицину, были соединены и был получен штамм E. coli, устойчивый к обоим антибиотикам. Перенос плазмид с нужными генами в микроорганизмы превращает их в биореакторы по производству искомых веществ.
Начиная с 1982 г. фирмы США, Японии, Великобритании и ряда других стран производят генно-инженерный инсулин для лечения диабета. Из тысячи литров бактериальной культуры получают приблизительно 200 г инсулина, что равно количеству, получаемому из 1600 кг поджелудочной железы животных. Интерферон – белок, синтезируемый организмом в ответ на вирусную инфекцию, – изучают сейчас как возможное средство лечения рака и СПИДа. Всего один литр бактериальной культуры дает такое количество интерферона, для получения которого потребовалось бы ~10 тыс. литров крови человека. Методами генной инженерии удалось создать и ряд вакцин, которые испытываются для проверки эффективности их воздействия на вирус иммунодефицита человека (ВИЧ). С помощью рекомбинантной ДНК получают и человеческий гормон роста, являющийся единственным средством лечения редкой детской болезни – гипофизарной карликовости. В Беларуси в РНПЦ эпидемиологии и микробиологии создан лиофилизированный препарат рекомбинантного нуклеокапсидного белка вируса гепатита С, который обладает антигенными и иммуногенными свойствами и будет использован в качестве антигена в диагностической иммуноферментной тест-системе отече-ственного производства для выявления антител к вирусу гепатита С.
Большим преимуществом данных генно-инженерных лекарственных препаратов является отсутствие при их использовании негативных побочных эффектов, характерных для препаратов, полученных из тканей животных или человека.
Технология рекомбинантных ДНК сделала возможным нетрадицион-ный подход белок–ген, получивший название обратной генетики. При та-ком подходе из клетки выделяют белок, синтезируют и клонируют ген этого белка, модифицируют его, создавая мутантный ген, кодирующий измененную форму белка. Полученный ген вводят в клетку. Если он экспрессируется, несущая его клетка и ее потомки будут синтезировать измененный белок. Таким образом можно исправлять дефектные гены и лечить наследственные заболевания.
Если гибридную ДНК ввести в оплодотворенную яйцеклетку живот-ных, могут быть получены трансгенные организмы, экспрессирующие модифицированный ген и передающие его потомкам. С помощью генетической инженерии созданы линии животных, устойчивых к вирусным заболеваниям, а также породы с полезными для человека признаками. Например, микроинъекция рекомбинантной ДНК, содержав-шей ген соматотропина быка, в зиготу кролика позволила получить трансгенное животное с гиперпродукцией этого гормона. Полученные животные обладали ярко выраженной акромегалией. Кроме чисто практической полезности генетической трансформации животных, она позволяет решать и некоторые задачи фундаментальной науки. Например, она может оказать большую помощь в установлении роли отдельных генов и их белковых продуктов как в регуляции активности других генов, так и в различных патологических процессах.
Методы физического переноса ДНК. Агробактериальная трансфор-мация – наиболее эффективная технология введения трансгенов в клетки растений, применяемая сегодня. Однако она имеет ограничения, связанные с кругом хозяев агробактерий. Специально отобранные штаммы Agrobacterium с широким кругом хозяев могут инфицировать приблизительно половину двудольных видов растений, а также некоторые из голосеменных. Многие двудольные и голосеменные и практически все однодольные растения устойчивы к агробактериальной инфекции и никогда не образуют опухолей. Тем не менее совершенствование этого метода продолжается. В результате разработаны протоколы для агробактериальной трансформации риса. Выделены вступающие в симбиоз с растениями микроорганизмы, отличные от агробактерий (Rhizobium, Sinirhizobium, Mesorhizobium), которые после соответствующей генетической модификации способны к горизонтальному переносу генов.
Для трансформации устойчивых (рекальцитрантных) к агробактери-ям растений разработаны методы прямого физического переноса ДНК в клетку, многие из которых перенесены из практики работы с клетками бактерий или животных. Эти методы достаточно разнообразны: они включают бомбардировку микрочастицами или баллистический метод (иначе – баллистическая трансфекция; биолистика); электропорацию; обработку полиэтиленгликолем; перенос ДНК в составе липосом и др.
Баллистический и агролистический методы переноса ДНК. Наиболее продуктивным и чаще всего используемым является метод бомбардировки микрочастицами, обработанными препаратом ДНК, предназначенной для переноса в растение. При достаточной скорости эти частицы могут непосредственно проникать в ядро, что значительно повышает эффективность трансформации. Этим же методом можно трансформировать и другие ДНК-содержащие клеточные органеллы – хлоропласты и митохондрии.
Баллистическая трансфекция основана на обстреле органов и тканей микрочастицами тяжелых металлов (золото, вольфрам), покрытых плазмидной ДНК. Микрочастицы проходят через клеточные слои и переносят генетическую конструкцию непосредственно в ядра клеток. «Генная пушка» (gene gun) по устройству сходна со стрелковым оружием. Глубина проникновения микрочастиц, как правило, невелика – до 1 мм. На рисунках 5 и 6 представлены принципиальная схема баллистического метода и конкретный пример использования современной «генной пушки».
В последнее время разработан и успешно применяется также комбинированный метод трансформации, названный агролистическим. При этом чужеродная ДНК вводится в ткани каким-либо физическим ме-тодом, например, баллистическим. Вводимая ДНК включает как Т-ДНК вектор с целевым и маркерным геном, так и агробактериальные гены вирулентности, поставленные под эукариотический промотор. Временная экспрессия генов вирулентности в растительной клетке приводит к синтезу белков, которые правильно вырезают Т-ДНК из плазмиды и встраивают ее в геном растения-хозяина, как и при обычной агробактериальной трансформации.
Аргументы сторонников расширения практического применения технологии создания трансгенных растений сводятся к следующему. В ближайшие несколько десятилетий продукцию растениеводства необходимо увеличить в 2–3 раза. Решение этой проблемы классическими селекционно-генетическими и агротехническими методами невозможно, по их мнению, так как генетический потенциал растений исчерпан для классической селекции. Кроме того, существует настоятельная необходимость быстрого введения в практику новых сортов высокопродуктивных устойчивых растений. Именно генетическая инженерия растений способна решить все эти задачи, причем путем, принципиально сходным с классическим селекционно-генетическим процес-сом.
Перечислим возможности генной инженерии растений:
• улучшение качества запасных белков, в частности их аминокислотного состава;
• производство белков животного происхождения;
• повышение содержания жиров, изменение их спектра;
• увеличение содержания полисахаридов;
• создание гербицидоустойчивых растений;
• повышение устойчивости растений к стрессовым условиям;
• повышение эффективности биологической азотфиксации;
• повышение эффективности фотосинтеза;
• получение растений с новыми свойствами.
Однако внесение в растения чужеродной ДНК из микроорганизмов или животных продолжает вызывать возражения у противников генетической инженерии. Так, например, все больше раздается голосов об опасности присутствия в геноме ГМО так называемого «технологического мусора», в частности остатков векторов, с помощью которых был осуществлен перенос трансгена, а также маркерных генов, в качестве которых обычно выступают гены устойчивости к антибиотикам.
Биологическая безопасность и сохранение биоразнообразия. В дискуссии о безопасности использования трансгенных растений и животных в сельском хозяйстве участвуют правительственные комиссии и неправительственные организации типа «Гринпис». На рисунке 13 представлена карта мира с указанием стран, в которых использование генетически модифицированных организмов разрешено или запрещено, а в таблице 2 – аргументы за и против использования ГМО.
Таблица 2 – Аргументы сторонников и противников использования генетически модифицированных организмов
За ГМО |
Против ГМО |
Пищевая безопасность |
|
Контроль безопасности |
|
Опыт использования организмов, полученных с помощью биотехнологии |
Недостаточность исследований по биобезопасности |
Небезопасность продуктов традиционного сельского хозяйства |
|
Экологическая безопасность |
|
Безопасные технологии выращивания ГМО (на изолированных полигонах) |
Вытеснение естественных видов и распространение гибридов с ГМО |
Распространённость горизонтального переноса генов в природе (ничего нового генная инженерия не добавляет) |
|
Конвенция о биологическом разнообразии и Картахенский протокол по биобезопасности. Одним из важных документов, регламентирующих генно-инженерную деятельность (ГИД) и одновременно регулирующих межгосударственные отношения, является Конвенция о биологическом разнообразии (КБР, Рио-де-Жанейро, июнь 1992 г.). В ней провозглашается ответственность человечества за сохранение, устойчивое использование и долгосрочное развитие биологического разнообразия. В Конвенцию также включены проблемы сохранения природных мест обитания, рационального использование биологических ресурсов, восстановления деградировавших экосистем и исчезающих видов, строгого контроля над современными биотехнологиями, разработки национальных экологических сетей и законодательной институциональной базы. В соответствии с принципом принятия мер предосторожности, в 2000 г. был разработан, 11 сентября 2003 г. вступил в силу и, по состоянию на август 2010 г., ратифицирован большинством стран-сторон КБР (160 из 192 государств-членов ООН) Картахенский протокол по биобезопасности (КПБ) к КБР. Цель КПБ – содействие правительствам стран в обеспечении надлежащего уровня защиты в области безопасной передачи, обработки и использования живых (генетически) измененных организмов (ЖИО/ГИО), являющихся результатом применения современной биотехнологии (в том числе генетической модификации, ГМ) и способных оказать неблагоприятное воздействие на сохранение и устойчивое использование биологического разнообразия, с учетом рисков для здоровья человека и проявления особого внимания к их трансграничному перемещению.
Наряду с очевидными позитивными возможностями генно-инженерной деятельности, существует также потенциальный риск негативного влияния живых измененных организмов (ЖИО по терминологии Картахенского протокола) при их выпуске в окружающую среду. Этот аспект ГИД вызывает огромное беспокойство у ученых и общественности, так как известно, что наличие трансгенных конструкций в геноме может приводить к непредсказуемым изменениям в составе нуклеиновых кислот и балансе экспрессии генетического материала.
Возможные отрицательные явления можно подразделить на две составляющие. Во-первых, у самих ЖИО (в том числе в продуктах из них) могут проявиться или усилиться токсичность и аллергенность, патогенность и инвазивность (например, у микроорганизмов); биологическая агрессивность – опасность вытеснения ими ценных и редких аборигенных видов или утрата последних в результате засорения генами, перенесенными от ЖИО; ядовитое воздействие на нецелевые виды (например, на пчел, бабочек, муравьев, жужелиц и др.). Во-вторых, возникновение ряда нежелательных и даже вредных последствий от использования измененных организмов, как в сфере природопользования (например, акселерация появления суперрезистентных вредителей; опасность превращения ЖИО в сорняк, возникновение более вредоносных сорняков в результате переноса трансгенов другим видам); накопление в почве и воде токсинов трансгенных растений; так и сельскохозяйственного производства (неблагоприятные психолого-экономические взаимоотношения между производителями продукции из ГИО (фермерами, например) и поставщиками семян трансгенных растений и химикатов к ним (биотехнологические и химические фирмы); неожиданные ситуации, например, непредвиденные дополнительные расходы на пестициды для уничтожения вредителей ″второй волны″, размножившихся после снятия конкурентного прессинга основного насекомого-вредителя, или накопление в зоне выращивания ГМ-растений и прилегающих зонах гербицидов, к которым данные ГМ-растения устойчивы; накопление в почве и воде токсинов трансгенных растений и иные неблагоприятные воздействия на экосистемы.
