
- •Київський національний університет будівництва і архітектури
- •Методичні вказівки
- •Самостійна робота № і
- •Самостійна робота № 2 вуглеводні аліфатичного ряду
- •Самостійна робота № 3
- •Самостійна робота № 4 ароматичні вуглеводні та їх похідні
- •Самостійна робота № 5 Високомолекулярні органічні сполуки ( вмс, полімери).
- •Методичні вказівки
Самостійна робота № 4 ароматичні вуглеводні та їх похідні
Задачі цього розділу мають на меті поглибити знання студентів при вивченні специфічного розділу органічної хімії - ароматичні сполуки. До останніх відносяться вуглеводні та їх похідні, що містять в своєму складі ароматичну систему – планарну циклічну систему, в якій всі атоми циклу приймають участь в утворенні єдиної кон’югованої системи, яка утримує, згідно правила Хюккеля, 4n+2 – електронів (n – ціле позитивне число). До найбільш поширених ароматичних сполук відносяться такі, що утримують 6 – π-електронів (бензен та його гомологи). Детальним розглядом цих сполук ми і обмежимося. При вивченні цієї теми, а також в процесі розв’язання задач потрібно уяснити, що специфічність властивостей ароматичних сполук та їх похідних є наслідком того, що в ароматичній системі – електрони за рахунок «бокового» перекриття сусідніх р-орбіталей, які орієнтовані перпендикулярно до площини циклу, утворюють стійку електронну систему. Для повної і однозначної ідентифікації ароматичних сполук особливу увагу потрібно звернути на специфіку номенклатури.
Ароматичні вуглеводні належать до карбоциклічних сполук, в молекулах яких міститься особлива циклічна група із шести атомів карбону, що називається бензеновим ядром, або кільцем. Першим представником з ароматичних сполук є бензен C6H6.

 За
складом його відносять до ненасичених
сполук, але за хімічною здатністю
його можна віднести до насичених
вуглеводнів. Так, він не знебарвлює
бромну воду й розчин
калій
перманганату, але вступає в реакцію
електрофільного заміщення: нітрування,
сульфування, галогенування, алкілування,
ацилювання тощо.
Під
час вивчення реакції електрофільного
заміщення треба враховувати правила
заміщення в бензеновому ядрі. Кожний
замісник у бензеновому кільці має певну
орієнтуючу дію. Замісники першого ряду
(–N(CH3)2,
–NHCH3,
–NH2,
–OH,
СH3,
–CnH2n+1,
–Hal)
спрямовують електрофільний замісник
переважно в орто- і пара-положення.
Замісники другого ряду (–NO2,
–CN,
–SO3H,
–CHO,
–COOH
та ін.) спрямовують електрофільний
намісник у мета-положення.
За
складом його відносять до ненасичених
сполук, але за хімічною здатністю
його можна віднести до насичених
вуглеводнів. Так, він не знебарвлює
бромну воду й розчин
калій
перманганату, але вступає в реакцію
електрофільного заміщення: нітрування,
сульфування, галогенування, алкілування,
ацилювання тощо.
Під
час вивчення реакції електрофільного
заміщення треба враховувати правила
заміщення в бензеновому ядрі. Кожний
замісник у бензеновому кільці має певну
орієнтуючу дію. Замісники першого ряду
(–N(CH3)2,
–NHCH3,
–NH2,
–OH,
СH3,
–CnH2n+1,
–Hal)
спрямовують електрофільний замісник
переважно в орто- і пара-положення.
Замісники другого ряду (–NO2,
–CN,
–SO3H,
–CHO,
–COOH
та ін.) спрямовують електрофільний
намісник у мета-положення.
Фенолами називають похідні ароматичних вуглеводнів, у яких один або кілька атомів Гідрогену бензенового кільця заміщені на гідроксильну групу. За кількістю гідроксильних груп розрізняють одно-, двох-, і багатоатомні феноли. У разі заміни атома гідрогену в боковому ланцюзі на гідроксильну групу одержують ароматичні спирти. Більшість фенолів та їх похідних мають тривіальні назви. У промисловості феноли добувають із кам'яновугільної смоли. Найбільше значення із синтетичних методів має отримання фенолів із галогенопохідних, солей сульфокислот (лужна плавка), первинних ароматичних аміносполук через діазосполуки. Феноли — тверді кристалічні речовини з характерним запахом, добре розчинні в спирті, етері, бензені. Легко відганяються з водяною парою і є антисептиками, антиоксидантами
Реакції, які характеризують хімічні властивості фенолів, поділяють на два типи: реакції за рахунок фенольного гідроксилу та реакції за рахунок бензенового кільця. До першого відносять реакції утворення фенолятів, алкілювання й ацилювання; до другого — реакції електрофільного заміщення атомів гідрогену в бензеновому кільці: нітрування, сульфування, галогенування та ін. Крім того, феноли здатні до реакцій гідрування, поліконденсації (фенолоформальдегідні полімери) й окиснення.
Діазосполуки — органічні речовини загальною формулою Ar-N2-X, де Ar — ароматичний залишок, X — неорганічний залишок. Діазосполуки залежно від середовища існують у кількох ізомерних формах: [Ar-N+=N]X- — сіль діазонію (кисле середовище), Ar-N=N-OH — діазогідрат (у середовищах, близьких до нейтральних), Ar-N=N-OMe — діазотат (лужне середовище). Ці форми легко переходять одна в іншу залежно від середовища:
 Діазосполуки
добувають реакцією діазотування
первинних ароматичних амінів. Солі
діазонію дуже реакційноздатні. Розрізняють
два види хімічних перетворень діазосполук:
- реакції, які проходять із виділенням
нітрогену (діазореакції). Важливими
реакціями цього типу є добування
фенолів, галогенопохідних, нітрилів,
ароматичних кислот, вуглеводнів,
металоорганічних сполук тощо;
Діазосполуки
добувають реакцією діазотування
первинних ароматичних амінів. Солі
діазонію дуже реакційноздатні. Розрізняють
два види хімічних перетворень діазосполук:
- реакції, які проходять із виділенням
нітрогену (діазореакції). Важливими
реакціями цього типу є добування
фенолів, галогенопохідних, нітрилів,
ароматичних кислот, вуглеводнів,
металоорганічних сполук тощо;
- реакції, які проходять без виділення нітрогену. Серед них: реакції азосполучення солей діазонію з фенолами й ароматичними амінами й утворенням азобарвників.
Азосполуками називають органічні речовини, які містять у молекулі азогрупу -N=N-, вільні валентності якої з'єднані з ароматичними залишками. Найпростіший представник — азо-бензен. Найважливішими похідними азобензену є аміноазосполуки й оксіазосполуки, широко використовувані як барвники.
Завдання для самостійної роботи № 4.
1. Які сполуки відносяться до гомологічного ряду аренів ? Правило Хюккеля. Будова бензену. Номенклатура аренів.
А) Напишіть структурні формули всіх ізомерних ароматичних вуглеводнів загальної формули С9Н12. Назвіть їх згідно з правилами IUPAC.
Б) Напишіть структурні формули сполук: 1,3,5,-триметилбензену; ізопропілбензену; вінілбензену; тринітрофенолу; 1,4-диметилбензену; транс-дифенілетилену ( наведіть приклади можливих тривіальних назв цих сполук)
2. Чому бензен – ненасичений вуглеводень, не вступає в реакції, які характерні для алкенів та алкінів? Напишіть реакції, що пояснюють ці висновки:
А) Порівняйте хімічні властивості толуену, 1- гептену та 1-гептину.
Б) Порівняйте реакційну здатність в реакціях приєднання, заміщення та окиснення для – бензену, 1- гексену та 1-гексину.
3. Реакції електрофільного заміщення в бензеновому кільці. Класифікація реакцій заміщення за природою реагенту. Напишіть можливі реакції:
А) толуену з вказаними реагентами : Br2(FeBr3);НBr;Н2О( Н+); H2SO4; HNO3(H2SO4);CH3Cl(AlCl3); CH3COCl (AlCl3)
Б) бензену з : Cl2(FeCl3); Cl2(сонячне світло); H2SO4(олеум); HNO3(H2SO4); C3H7Br(AlBr3);C2H5COCl (AlCl3); Br2 (Н2О)
4. Методи отримання ароматичних сполук ( промислові та лабораторні). Запропонуйте декілька схем синтезу: А) бензену, толуену, стирену, аніліну, кумену (ізопропілбензену)
Б) параксилену, фенолу, ортофталевої кислоти, стирену, сульфанілової кислоти
5. Хімічні властивості гомологів бензену. Класифікація замісників в бензеновому кільці ( замісники 1- та 2-го роду). Напишіть реакції та структурні формули головних продуктів , що утворюються при взаємодії:
А) толуену, нітробензену, мета-нітротолуену з HNO3(H2SO4) та C3H7Br(AlBr3)
Б) аніліну, мета-нітрофенолу, бензальдегіду з Br2(FeBr3)та H2SO4(олеум)
6. Способи одержання та хімічні властивості фенолів. Напишіть реакції та назви сполук.
А) За допомогою якого реагента можна відрізнити фенол від етанолу
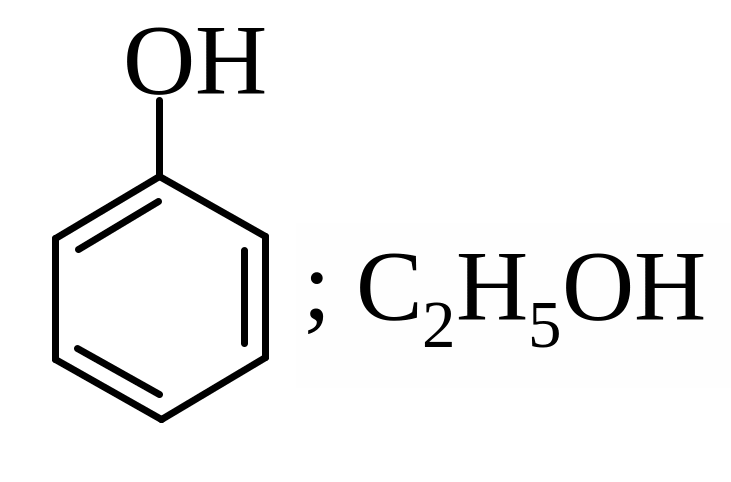
Б) Резорцин (1,3-дигідроксибензен) входить до складу мазей та водних або спиртових розчинів, які використовують при шкірних захворюваннях. За допомогою якого із реагентів можна виявити в структурі резорцину (1,3-дегідроксифендолу) фенольний гідроксил
7. Правила орієнтації замісників в реакціях електрофільного заміщення для похідних бензену. Навести приклади реакцій:
А) Як впливає карбоксильна група на реакційну здатність бензенового кільця та в яке положення направляє наступні замісники в реакціях SE?
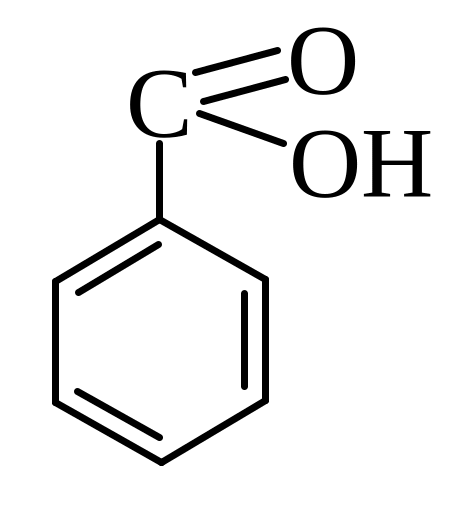
Б) В молекулі п-амінобензальдегіду який вплив альдегідної та аміно- груп на швидкість реакції та орієнтацію входження третього замісника?

8.Карбонові кислоти ряду бензену. Напишіть методи отримання, хімічні властивості та застосування наступних сполук:
А) пара-амінобензенова кислота (етиловий етер пара-амінобензенової кислоти (анестезин) використовується як анестезуючий засіб. Яка формула відповідає цій назві ?)
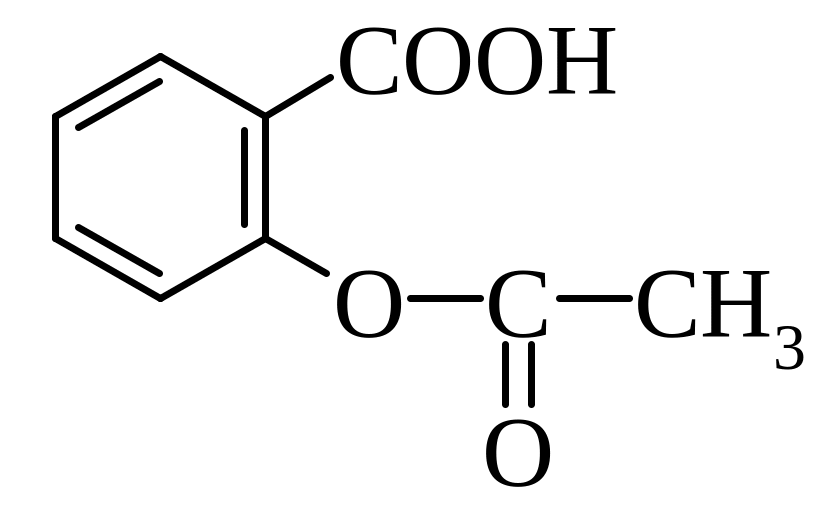
Б) саліцилова кислота (саліцилова кислота є сильнішою кислотою ніж її мета- і пара-ізомери. Чим пояснюються її більш виражені кислотні властивості? Якісна реакція на цю кислоту ?

аспірин (ацетилсаліцилова кислота) – наведіть схему синтеза
9.Розташуйте ароматичні сполуки в ланцюг зростання їх активності в реакціях електрофільного заміщення. Напишіть рівняння реакцій нітрування та галогенування ( в присутності кислот Льюіса) та поясніть відповідь:
А) С6Н6, С6Н5Сl, С6Н5ОН; C6H5NO2
Б) C6H5NH2, C6H6, С6Н5СООН.; С6Н5СН3,
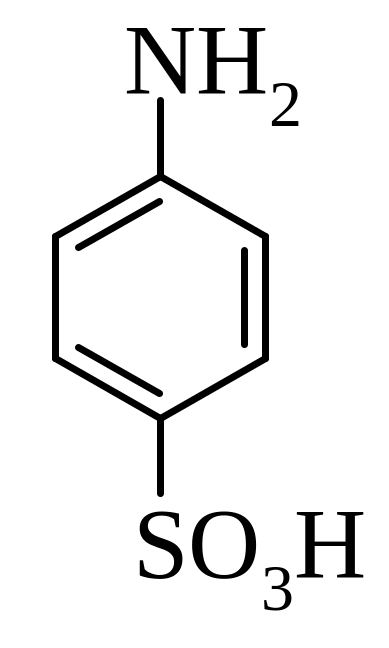
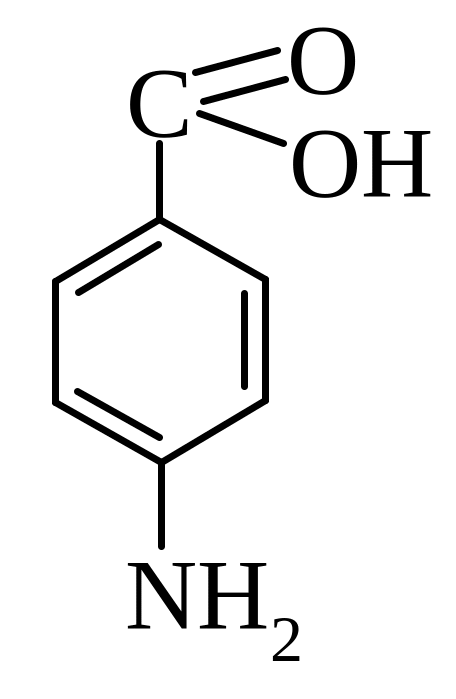
10. Ароматичні аміни (C6H5NH2), діазо- та азосполуки. Хімічні властивості. Реакції азасполучення та їх використання для отримання азабарвників (приклади). Дати назви вказаних сполук та на їх прикладах пояснити запитання:
А)
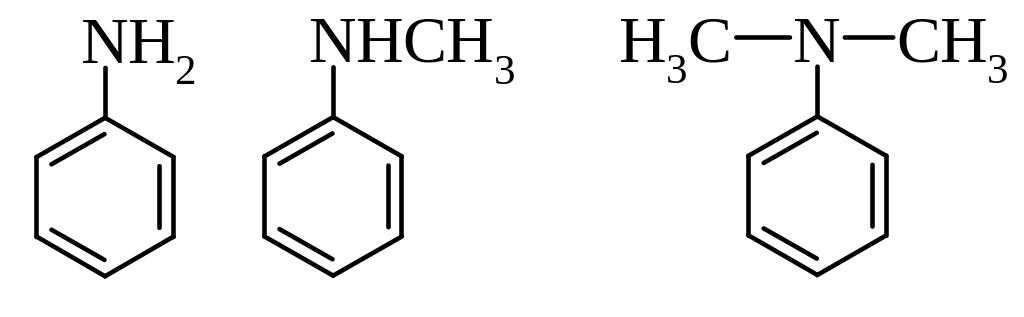
Б)
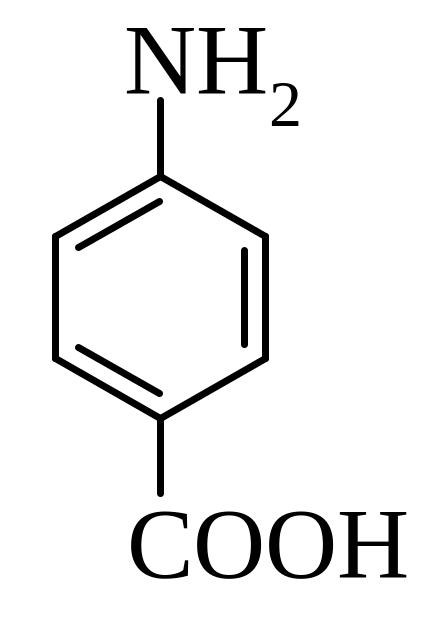
11. Ароматичні вуглеводні з конденсованими бензеновими ядрами. Добування та використання. Написати хімічні властивості для наступних сполук:
А) нафтален; антрацен
Б) фенантрен; нафтален
12. Написати хімічні реакції, назвати всі речовини, тип та механізм реакцій:
А)
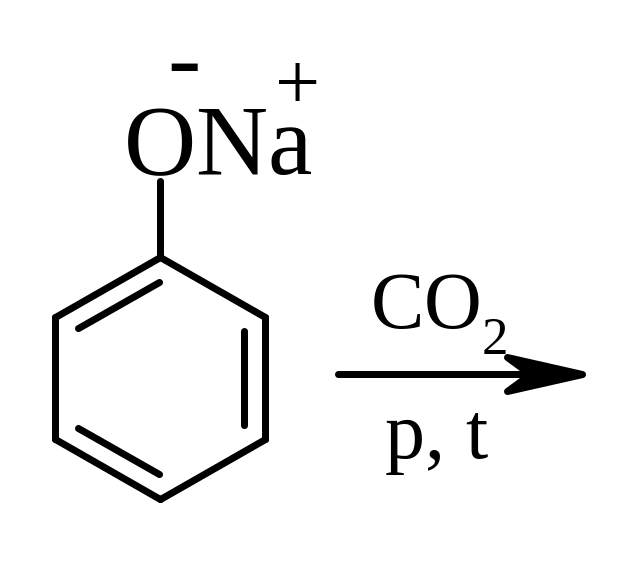 ?
?
 ?
?
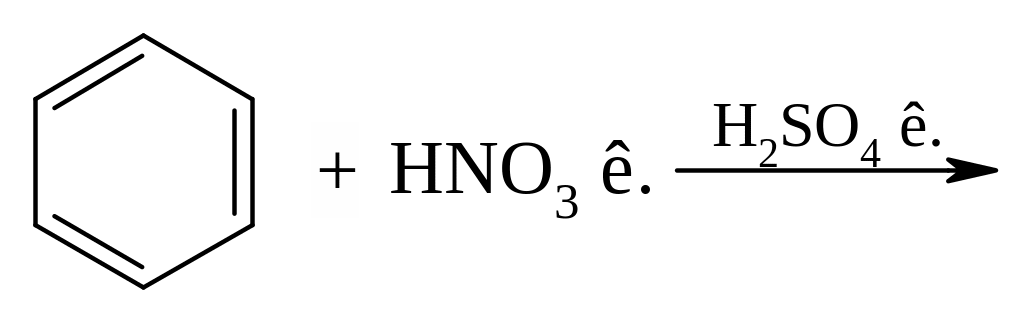 ?
?
Б)
 ?
?
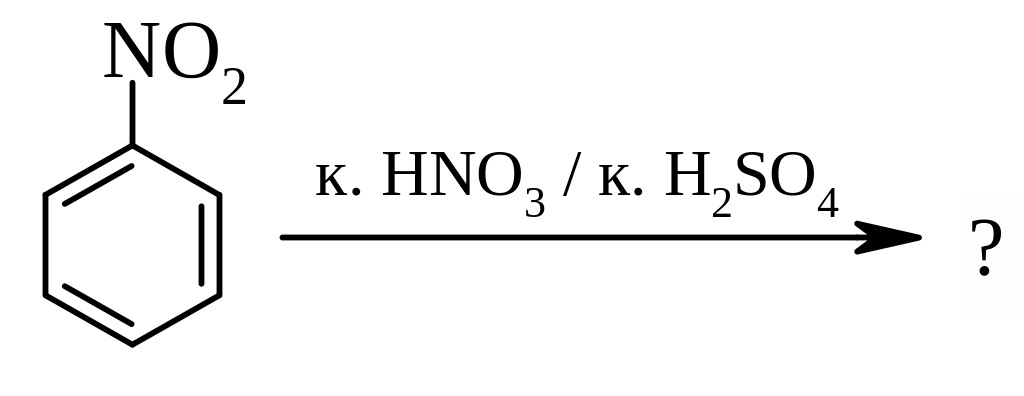
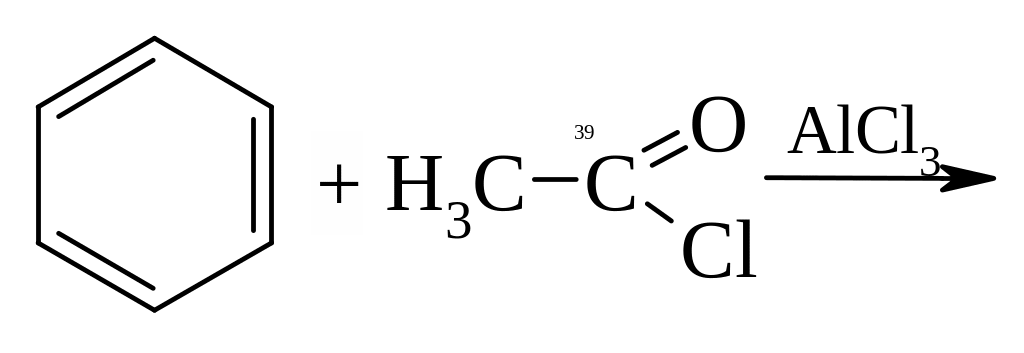 ?
?
13. Напишіть реакції та зробіть необхідні розрахунки:
А) Ароматичний вуглеводень, який є гомологом бензену, масою 5,3г спалили. Добули СО2 об’ємом 8,96 л (н.у.) . Визначте формулу вуглеводню . Скільки ізомерів може мати цей вуглеводень? Напишіть структурні формули цих ізомерів.
Б) Яка маса тринітротолуену утворюється з толуену масою 57,5 г, якщо вихід продукту реакції становить 80% від теоретично можливого? Напишіть структурні формули можливих ізомерів.
14. Запропонуйте методи синтезу та поясніть застосування ароматичних сполук в будівництві, в промисловості оздоблювальних матеріалів, полімерів, барвників, поверхнево-активних речовин т.щ.
А) фенол, алкіларилсульфонати, ксилен, діазосполуки ароматичного ряду
Б) стирен, кумен (ізопропілбензен), бензен, бензенсульфокислота, анілін
15. Напишіть структурні формули речовин, їх назви, методи отримання та застосування наступних ароматичних сполук:
А) ароматичні аміни, алкільні похідні ароматичних вуглеводнів, ароматичні карбонові кислоти
Б) феноли, багатоядерні ароматичні сполуки, діазосполуки
