
- •Iші дәріс тақырыбы
- •1.1 Сапалық анализдің әдістері
- •IIші дәріс тақырыбы
- •IiIші дәріс тақырыбы
- •IVші дәріс тақырыбы
- •Күшті қышқылдан және күшті негізден түзілген тұз -
- •4. Әлсіз қышқылдан және әлсіз негізден түзілген тұз.
- •Vші дәріс тақырыбы
- •VI ші дәріс тақырыбы
- •6.1 Тотығу-тотықсыздандыру (редокс) потенциал
- •6.2 Тотығу-тотықсыздандыру реакцияның тепе-теңдік константасы
- •ViIші дәріс тақырыбы
- •Комплексті қосылыстардағы химиялық байланыстың табиғатың түсіндіретін теориялар
- •Комплексті қосылыстар ерітіндісіндегі тепе-теңдік
- •ViiIші дәріс тақырыбы
- •8.1 Титриметриялық анализдің есептеуі
- •8.2 Қышқылды-негіздік әдісінің титрлеу қисықтары
- •IXші дәріс тақырыбы
- •Хромофорлық теория
- •Xші дәріс тақырыбы
- •Индикаторлар
- •Редокс-индикаторлар
- •XIші дәріс тақырыбы
- •XiIші Дәріс тақырыбы
- •Индикатормен титрлеу әдістері
- •XiiIші Дәріс тақырыбы
- •1. Комплексометрия
- •Цианидометрия
- •Хелатометрия
- •XivДәріс тақырыбы
- •1. Гравиметрия әдіс
- •XV ші дәріс тақырыбы
- •Молекулалы – абсорбциялық анализ
Iші дәріс тақырыбы
Кіріспе. Сапалық анализдің әдістері
Аналитикалық химия анализ әдістерін зерттейді, оларды тәжірибеге еңгізеді және ғылыми негізін қалайды. Заттың құрылысы түралы хабар алудың негізі деп химиялық реакция саналады. Заттардың химиялық құрамын зерттейтін ғылым ретінде аналитикалық химия келесі сұрақтарды шешеді:
1) заттардың химиялық құрамын: изотопты, элементті, ионды, топтық, молекулалық, фазалық анықтайды – сапалық анализ ;
2) заттардың құрамы компоненттерінің мөлшерін анықтайды – сандық анализ;
3) заттардың құрылысын анықтайды – молекула бөлшектерінің орналасуын және олардың арасындағы байланыстарды зерттейді.
1.1 Сапалық анализдің әдістері
Заттың сапасын химиялық, физикалық және физика-химиялық әдістермен зерттеуге болады. Химиялық әдістер үшке бөлінеді: 1) экстракция; 2) хроматография; 3) тұнбалау әдісі.
Заттың химиялық талдауын екі тәсілмен жүргізеді: «құрғақ» немесе «сулы» жолмен.
Алынған зат массасына немесе көлеміне байланысты анализ үш әдіске бөлінеді:
1) макро-
2) жартылаймикро-
3) микро
Химиялық әдістердің негізіне хабар алудың көзі есебінде химиялық реакция саналады. Элементтерді, иондарды, молекулаларды бөлуге, анықтауға және сандық мөлшерін есептеуге арналған химиялық реакцияларды аналитикалық реакциялар дейді.
Аналитикалық реакциялар қолданылуына байланысты топты және жекелі болып екіге бөлінеді.
Топты реакциялар күрделі заттар қосындысынан белгілі бір топты, яғни аналитикалық топты ажыратуға арналған.
Жекелі, арнайы реакциялар деп тек белгілі бір ионға ғана тән реакцияларды
Негізгі әдебиет: 1[45-64], 2[78-127].
IIші дәріс тақырыбы
Гомогенді жүйедегі тепе-теңдік
Гомогенді жүйелерде реакция жүйенің барлық көлемінде жүреді. Электролиттер суда немесе басқа полярлы еріткіштерде ерігенде оң және теріс зарядталған бөлшектерге – иондарға ыдырайды. Бұл процесті диссоциациялану немесе ионизациялану дейді. Диссоциациялану процесініне ұшыраған молекулалар үлесін диссоциациялану дәреже дейді, α деп белгілейді.
Жалпы түрде жазылған реакция үшін:

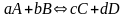 (2.1)
(2.1)
Тікелей
реакцияның жылдамдығы былай өрнектеледі:
 (2.2)
(2.2)
Тікелей
реакциямен қатар кері реакция жүреді.
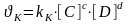 (2.3)
(2.3)
мұнда: [А], [В], [С], [D] – бастапқы заттардың және реакция өнімдерінің молярлық концентрациялары, моль/л;
kT,
kK
– тікелей және кері реакциялардың
жылдамдық константалары. Тепе-теңдік
орныққан кезде тікелей
және
кері
реакция жылдамдықтары өзара тенеседі
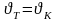 ,
яғни
,
яғни
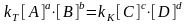 (2.4)
(2.4)
Кс – реакция тепе-теңдік концентрациялық константасы.
P = const, T = const, I = const жағдайларда, Kc – тұрақты шама.
Молярлық концентрациялар арқылы көрсетілген тепе-теңдік константа тек идеалды және сұйылтылған ерітінділер үшін қолданылады.
Иондардың активтіліктері арқылы есептелген тепе-теңдік константа термодинамикалық диссоциациялану константа деп аталады
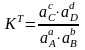 (2.5)
(2.5)
Концентрациялық константадан оның айырмашылығы, ол ерітіндінің иондық күшіне тәуелсіз.
Негізгі әдебиет: 1[5-35], 2[20-25].
