
- •3.3 Молекулярный анализ органических веществ
- •3.3.1 Общие представления
- •3.3.1 Спектрофотометрия и фотоколориметрия
- •Спектрофотометр
- •Внутренние влияющие факторы
- •Оранжевый желтый
- •Модификации способа определения концентрации одного светопоглощающего компонента в области длин волн λ1 – λ2
- •1. Способ сравнения оптических плотностей, измеренных для определяемого компонента в веществе сравнения и в пробе анализируемого вещества.
- •2. Способ с использованием значения молярного коэффициента поглощения ε.
- •Дифференциальная фотометрия
- •Определение концентрации нескольких светопоглощающих компонентов в области длин волн λ1 – λ2. Закон аддитивности
- •Модели спектрофотометров и фотоколориметров
- •Возможности методов спектрофотометрии и фотоколориметрии в анализе вещества объектов окружающей среды
- •Примеры утверждённых в России методик определения загрязняющих компонентов в веществе объектов окружающей среды методом фотоколориметрии
- •Пнд ф 13.1.61-2007 (издание 2012 г.)
- •Методика измерений массовой концентрации сероуглерода в промышленных выбросах в атмосферу фотометрическим методом. Пнд ф 13.1.60-2007 (издание 2012 г.)
- •3.3.2 Методы нефелометрии и турбидиметрии
- •Применение методов нефелориметрии и турбидиметрии в анализе вещества в охране окружающей среды
- •Примеры утверждённых в России методик определения загрязняющих компонентов в веществе объектов окружающей среды методом фотоколориметрии Турбидиметрия
- •Нефелометрия
- •Средства измерения
- •Модели спектрофлюориметров и флюориметрических анализаторов
- •Примеры утверждённых в России методик определения загрязняющих компонентов в веществе объектов окружающей среды методом флюориметрии
3.3 Молекулярный анализ органических веществ
3.3.1 Общие представления
Молекулярный анализ пробы органического вещества заключается в определении органических соединений, характеризующихся одинаковыми физико-химическими или физическими свойствами, часто это соединения одного класса (предельные и непредельные углеводороды, альдегиды, кетоны, спирты, карбоновые кислоты и т.д.).
На сегодняшний день идентифицировано несколько миллионов органических соединений природного и искусственного происхождения. Не существует методов анализа, которые позволили бы определить в одной навеске пробы органического вещества все присутствующие в нём химические соединения. Поэтому, либо на стадии подготовки пробы к измерениям выделяют по определённым свойствам узкие фракции органических соединений и далее их анализируют; либо в пробе анализируемого вещества определяют химические соединения, входящие в узкую фракцию по каким-либо свойствам.
Молекулярный анализ пробы органического или смешанного металлоорганического вещества может быть выполнен хроматографическими методами, методом масс-спектрометрии органических веществ, методом ядерного магнитного резонанса, методом ИК-спектрометрии, методом спектрофотометрии, методом флюориметрии, методом вольтамперометрии.
Для выполнения молекулярного анализа проб органического или металлоорганического вещества объектов окружающей среды используются хроматографические методы, фотоколориметрический метод и метод флюориметрии. Хроматографические методы пригодны для выполнения как качественного, так и количественного молекулярного анализа вещества природных вод на обнаружение в нём органических и металлоорганических соединений, вытяжки из почв, атмосферного воздуха, воздуха промышленных выбросов. Флюориметрия применяется для проведения количественного анализа пробы вещества природной воды, вытяжки из почвы, талой воды, полученной из пробы вещества снежного покрова и др. на содержание в них органических, органно-минеральных и металлоорганических соединений сложного строения.
Остальные вышеперечисленные методы применяют в охране окружающей среды при детальных исследованиях выделенных по физико-химическим, физическим или химическим свойствам узких фракций органического или металлоорганического вещества, например, в детальном изучении состава выделенных фракций из пробы вещества природного объекта при идентификации в ней неизвестных загрязняющих компонентов.
3.3.1 Спектрофотометрия и фотоколориметрия
Молекулярный абсорбционный анализ можно классифицировать в соответствии с участком электромагнитного спектра, используемого для облучения анализируемого вещества. В этом случае название метода соответствует названию области спектра.
Ультрафиолетовая (УФ)-спектрометрия. Для облучения используется ультрафиолетовое излучение в диапазоне длин волн180 … 400 нм.
Спектрометрия в видимой области. Для облучения используется видимое излучение в диапазоне длин волн 400 …760 нм.
Ближняя инфракрасная (БИК)-спектрометрия. Для облучения используется ИК-излучение в диапазоне длин волн 760 нм…1000 нм.
Метод молекулярной абсорбционной спектрометрии в УФ- и видимой областях спектра обычно называют спектрофотометрией. В зависимости от типа абсорбционных спектральных приборов различают фотометрический и спектрофотометрический методы. Их сравнительная характеристика приведена в табл. 9.1.
Таблица 9.1. Фотометрические методы анализа
Метод |
Тип прибора |
Рабочая область спектра, нм |
Способ монохроматизации |
Регистрируемые сигналы |
Фотометрия |
Фотометр (фотоколори-метр) |
Видимая 400–750 |
Светофильтр |
Оптическая плотность (А) и пропускание (Т) в диапазоне длин волн, отвечающем полосе пропускания светофильтра |
Спектрофото-метрия |
Спектрофото-метр |
УФ, видимая и ближняя ИК 180–1000 |
Монохроматор или полихроматор |
Оптическая плотность (А) и пропускание (Т) при фиксированной длине волны; электронные спектры поглощения в виде кривых А = f(), A = f(), T = f(), T = f() |
Оба метода объединяют в одну группу фотометрических методов анализа. Когда определение проводят в видимой части спектра, часто используют термин фотоколориметрия (от лат. color – цвет), поскольку имеют дело с окрашенными растворами.
Спектры поглощения
Спектрофотометрия основана на явлении избирательного поглощения монохроматического УФ- и видимого света молекулами вещества. В результате поглощения определённых квантов излучения электроны, участвующие в образовании химической связи между атомами в молекуле переходят из основного состояния с минимальной энергией в более высокое энергетическое возбужденное состояние. В этом состоянии электроны находятся 10-9 с и релаксируют в основное состояние, излучая поглощенный избыток энергии в виде тепла. Такое явление может быть измерено с помощью спектрофотометра и фотоколориметра.
Электромагнитное излучение поглощается анализируемым веществом избирательно: при некоторых длинах волн светопоглощение происходит интенсивно, а при некоторых свет не поглощается. Интенсивно поглощаются кванты света, энергия которых (h) равна энергии возбуждения электрона в молекуле.
Графическое изображение распределения поглощаемой энергии по длинам волн называется спектром поглощения, представляющего собой непрерывную кривую с максимумами. Количество поглощенной световой энергии выражают величинами Т, А, . В видимой и УФ - областях спектра обычно используют координаты A = f ( ) или = f ( ).
Основные характеристики спектра. Участок спектра, на котором наблюдается интенсивное поглощение излучения называют полосой поглощения. Спектр в определенном диапазоне длин волн может содержать от нуля до нескольких полос поглощения, рис. 9.1.
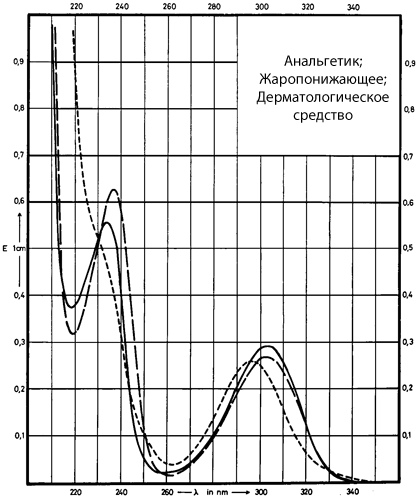
Рис. 9.1 УФ-спектр салициловой кислоты в различных растворителях
― метанол; ∙∙∙∙ 0.1 M NaOH --- 0.1 M HCL
Наибольший интерес
для химического анализа представляют
следующие характеристики спектра: число
максимумов (полос поглощения), их
положение по шкале длин волн, высота
максимума, рис. 9.1, значение молярного
коэффициента
в максимуме поглощения, интенсивность
полосы поглощения, ширина и форма полосы
(рис.9.2). Как видно из рис. 9.1, в УФ-спектре
салициловой кислоты четко регистрируются
две полосы поглощения в области 210 - 350
нм. Ширину полосы поглощения принято
характеризовать величиной
![]() -
полуширина полосы поглощения; ее измеряют
при = 1/2 max.
-
полуширина полосы поглощения; ее измеряют
при = 1/2 max.
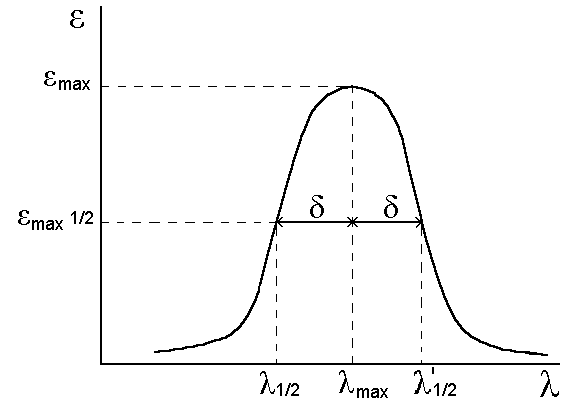
Рис. 9.2. Полоса поглощения
Интенсивность поглощения зависит от пространственной структуры молекулы, определяющей возможность поглощения того или другого количества энергии излучения конкретной длины волны. Для аналитической практики имеет значение поглощение при определенной длине волны, поэтому при характеристике полос используют значение молярного коэффициента в максимуме поглощения - max. Очевидно, чем выше max и меньше ширина полосы, тем лучше метрологические характеристики определения данного компонента.
Данные о длине волны и интенсивности поглощения в максимуме могут служить лишь приблизительным критерием при идентификации вещества, причем на положение максимума влияют введение в молекулу заместителя, структурные особенности соединения, изменение внешних условий, например, замена растворителя. Если полоса смещается в сторону более длинных волн, говорят о батохромном сдвиге или углублении окраски; если полоса смещается в сторону коротких волн, эффект называют гипсохромным сдвигом.
Наличие полос поглощения связано с соответствующими энергетическими переходами внешних (обобщенных, оптических) электронов в молекуле. Спектры в УФ- и видимой области называются электронными.
Электронные спектры соединений
Поглощение энергии излучения в видимом и ультрафиолетовом диапазоне длин волн приводит к возбуждению обобщенных электронов в молекуле и появлению в спектре полос, соответствующих электронным переходам между различными энергетическими уровнями в молекуле, которые называют орбиталями.
Электроны в молекуле могут занимать различные орбитали. Различают следующие молекулярные орбитали (МО): -связывающая, *-разрыхляющая, n-несвязывающая, -связывающая, *- разрыхляющая. Аналогично называют электроны в органических молекулах. Так электроны, участвующие в образовании одинарных С-С связей называют -электронами, участвующие в образовании С=С и С≡Ссвязей – -электронами, участвующие в образовании углерода с гетероатомами – N, O, S, галогенами, n-электронами.
Схема относительного расположения энергетических уровней, соответствующих разным МО, показана на рис.9.3.
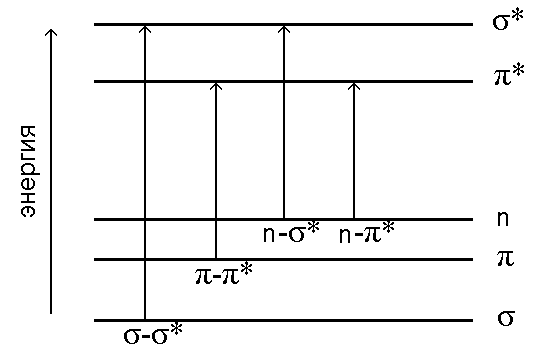
Рис.9.3 Схема электронных уровней и энергия возможных электронных переходов
Различные электронные переходы требуют неодинаковой энергии, поэтому полосы поглощения располагаются при разных длинах волн.
Наибольшей энергии
требует -*
– переход, связанный с возбуждением
внутренних электронов. Он соответствует
поглощению в далекой ультрафиолетовой
области (
200 нм, Е 600
кДж/моль).![]() Такие
переходы характерны, например, для
насыщенных углеводородов. Получить
спектр в этой области непросто, поскольку
здесь поглощают компоненты атмосферы;
по этой причине поглощение одинарной
связью не имеет большого значения в
аналитической практике.
Такие
переходы характерны, например, для
насыщенных углеводородов. Получить
спектр в этой области непросто, поскольку
здесь поглощают компоненты атмосферы;
по этой причине поглощение одинарной
связью не имеет большого значения в
аналитической практике.
Переход n-* связан уже с меньшими затратами энергии; полосы, связанные с этим переходом, расположены в обычном ультрафиолете ( ~ 200 ÷ 300 нм). Еще меньшая энергия требуется для перехода на разрыхляющие *-орбитали. Переходы n-* и -* встречаются в молекулах соединений с сопряженными связями и молекулах ароматических соединений. Такие функциональные группы, как С=О, С=С , –N=N–, –N=O, С=S, –CN, –CC– и многие другие, всегда являются причиной поглощения в видимой и ультрафиолетовой областях. Их называют хромофорными группами.
Этим же переходом n-* можно объяснить, например, интенсивную окраску ионов MnO4- и CrO42- (переход с несвязывающей орбитали кислорода). Поскольку каждое вещество характеризуется своей системой энергетических уровней, то и спектры веществ различаются как по числу полос, так и по их положению на шкале длин волн.
Полосы поглощения в спектре в УФ- и видимой областях можно зафиксировать только у тех молекул, которые имеют систему сопряженных связей. Чем больше сопряженных связей в молекуле, тем в более длинноволновой области можно зафиксировать полосы поглощения.
Очень мало неорганических молекул имеют спектры поглощения с выраженными полосами поглощения в УФ-области. К ним относятся КМnО4 и К2Cr2O7, имеющие систему подвижных электронов в атомах Мn и Cr. В видимой области полосы поглощения есть у всех окрашенных соединений, например у молекул с очень большой системой обобщенных электронов – красителей, у многих комплексных соединений, сольватов, ассоциатов.
Тонкая структура электронных спектров. Энергия, необходимая для возбуждения электронов, велика по сравнению с энергией возбуждения колебательного (и вращательного) движения атомов. Поэтому каждый электронный переход сопровождается колебательным переходом (в газовой фазе могут стать заметными и вращательные переходы). Наложение колебательных, а иногда и вращательных переходов приводит к существенному уширению полос в электронных спектрах, т.к. колебательная структура не всегда разрешается (рис. 9.4).
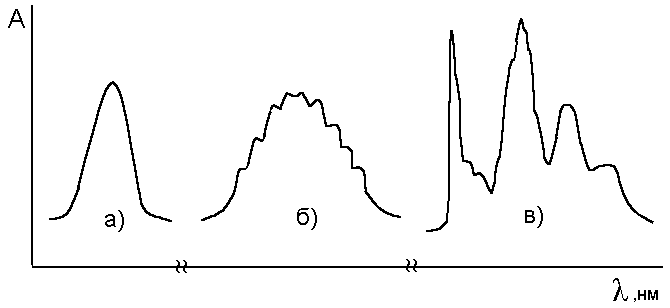
Рис. 9.4. Электронные спектры веществ: а) гладкий контур, колебательная структура не проявляется;
б) на контуре полосы видны следы колебательной структуры;
в) спектр поглощения паров антрацена с четкой колебательной структурой
В зависимости от состава молекул и условий измерения спектров (газовая или конденсированная фаза, тип растворителя, температура) полосы в электронных спектрах могут быть гладкими или характеризоваться лучше или хуже выраженной колебательной и вращательной структурами (рис.0.4); например, с увеличением полярности растворителя колебательная структура полос размывается.
Ширина полос резко увеличивается при переходе к конденсированному состоянию вещества вследствие сильного влияния соседних молекул.
Средства измерения
Основные узлы во всех приборах – абсорбционных спектрометрах в видимой и УФ-области одинаковы независимо от многообразия схем и конструктивных особенностей измерительного прибора, рис. 9.5.
