
- •Isbn 985-06-0828-5.
- •Введение
- •Глава 1. Растворы. Основы теории электролитической диссоциации.
- •1.1. Понятие о растворах. Процесс растворения. Растворимость веществ
- •1.2. Массовая доля растворенного вещества
- •1.3. Электролитическая диссоциация
- •1.5. Диссоциация оснований, кислот, амфотерных гидроксидов, солей в водных растворах
- •1.6. Факторы, влияющие на степень электролитической диссоциации
- •1.7. Константа электролитической диссоциации
- •1.8. Сильные электролиты и их активность
- •Глава 2. Кислотно-основное равновесие в водных растворах
- •2.1. Диссоциация воды.
- •2.2. Буферные растворы
- •2.3. Сущность гидролиза и типы гидролиза солей
- •2.4. Соли, образованные сильным основанием и слабой кислотой
- •2.5. Соли, образованные слабым основанием и сильной кислотой
- •2.6. Соли, образованные слабым основанием и слабой кислотой
- •2.7. Соли, образованные сильным основанием и сильной кислотой
- •2.8. Ступенчатый гидролиз
- •2.9. Степень гидролиза. Смещение равновесия гидролиза
- •2.10. Необратимый, или полный, гидролиз
- •Глава 3. Реакции окисления-восстановления
- •3.1. Основные положения электронной теории окислительно-восстановительных реакций
- •3.2. Окислительно-восстановительные потенциалы и направление окислительно-восстановительных реакций
- •3.3. Составление уравнений окислительно-восстановительных реакций электронно-ионным методом, или методом полуреакций
- •3.4. Применение реакций окисления-восстановления в химическом анализе
- •Глава 4. Комплексные соединения
- •4.2. Природа химической связи в комплексных ионах
- •4.3. Классификация и номенклатура комплексных соединений
- •4.4. Диссоциация комплексных соединений. Константы нестойкости и устойчивости
- •4.5. Внутрикомплексные соединения
- •4.6 Применение комплексных соединений в медицине и химическом анализе
- •Глава 5. Гетерогенные равновесия и процессы
- •5.1. Константа растворимости
- •5.2. Взаимосвязь между растворимостью и константой растворимости
- •5.3. Условия образования осадков
- •5.4. Условия растворения осадков
- •5.5. Понятие о коллоидных растворах
- •Часть II
- •Глава 6. Основы качественного анализа
- •6.1. Методы качественного анализа
- •6.2. Чувствительность и специфичность реакций. Дробный и систематический анализ
- •6.3. Понятие о химических реактивах
- •6.4. Аналитическая классификация катионов
- •Глава 7. Устройство и оборудование лаборатории
- •7.1. Требования к помещению лаборатории
- •7.2. Оборудование и посуда для полумикроанализа
- •7.3. Мытье химической посуды
- •Глава 8. Первая аналитическая группа катионов
- •8.1. Общая характеристика группы
- •8.2. Биологическая роль катионов первой аналитической группы. Применение соединений катионов первой аналитической группы в медицине
- •8.3. Частные реакции катионов первой аналитической группы
- •8.4. Анализ смеси катионов первой аналитической группы
- •Глава 9. Вторая аналитическая группа катионов
- •9.1.Общая характеристика группы. Действие группового реагента
- •9.2. Биологическая роль катионов второй аналитической группы. Применение соединений катионов второй аналитической группы в медицине
- •9.3. Частные реакции катионов второй аналитической группы
- •9.4. Анализ смеси катионов второй аналитической группы
- •2. Исследование осадка:
- •Глава 10. Третья аналитическая группа катионов
- •10.1.Общая характеристика группы. Действие группового реагента
- •10.2. Биологическая роль катионов третьей аналитической группы. Применение соединений катионов третьей аналитической группы в медицине
- •10.3. Частные реакции катионов третьей аналитической группы
- •10.4. Анализ смеси катионов третьей аналитической группы
- •10.5. Систематический анализ смеси катионов первой, второй и третьей аналитических групп
- •Вопросы
- •Глава 11. Четвертая аналитическая
- •11.1. Общая характеристика группы. Действие группового реагента
- •11.2. Биологическая роль катионов четвертой аналитической группы. Применение соединений катионов четвертой аналитической группы в медицине
- •11.3. Частные реакции катионов четвертой аналитической группы
- •11.4. Анализ смеси катионов четвертой аналитической группы
- •Глава 12. Пятая аналитическая группа катионов
- •12.1. Общая характеристика группы. Действие группового реагента
- •12.2. Биологическая роль катионов пятой аналитической группы. Применение соединений катионов пятой группы в медицине
- •12.3. Частные реакции катионов пятой аналитической группы
- •12.4. Ход анализа смеси катионов пятой аналитической группы
- •Глава 13. Шестая аналитическая группа катионов
- •13.1. Общая характеристика группы. Действие группового реагента
- •13.2. Биологическая роль катионов шестой аналитической группы. Применение соединений катионов шестой аналитической группы в медицине
- •13.3. Частные реакции катионов шестой аналитической группы
- •13.4. Анализ смеси катионов шестой аналитической группы
- •13.5. Систематический анализ смеси катионов всех аналитических групп
- •13.6. Ситуационные задачи по обнаружению катионов в исследуемом растворе
- •Глава 14. Общая характеристика
- •14.1. Биологическая роль элементов, входящих в состав анионов
- •14.2. Частные реакции анионов первой аналитической группы. Действие группового реагента
- •14.3. Частные реакции анионов второй аналитической группы. Действие группового реагента
- •14.4. Частные реакции анионов третьей аналитической группы
- •Глава 15. Систематический ход
- •15.1. Предварительные испытания
- •15.2. Обнаружение анионов первой аналитической группы
- •15.3. Обнаружение анионов второй аналитической группы
- •15.4. Обнаружение анионов третьей аналитической группы
- •15.5. Ситуационные задачи по обнаружению анионов в исследуемом растворе
- •Глава 16. Анализ неорганического
- •16.1. Установление аналитической группы катиона. Обнаружение катиона
- •16.2. Установление аналитической группы аниона. Обнаружение аниона
- •16.3. Анализ смеси нескольких солей
- •Часть III
- •Глава 17. Основные принципы количественного анализа
- •17.1. Задачи и методы количественного анализа
- •17.2. Подготовка вещества к анализу. Отбор проб для анализа
- •17.3. Лабораторные технические и аналитические весы
- •Глава 18. Гравиметрический (весовой) анализ
- •18.1. Сущность гравиметрического анализа
- •18.2. Посуда и оборудование в гравиметрическом анализе
- •18.3. Осаждение. Влияние различных факторов на образование осадков
- •18.4. Техника выполнения операций при проведении гравиметрического анализа
- •18.5. Примеры гравиметрических определений
- •Глава 19. Титриметрическии (объемный) анализ
- •19.1. Моль. Молярная масса. Химический эквивалент. Молярная масса эквивалента. Фактор эквивалентности
- •19.2. Способы выражения состава раствора
- •19.3. Основные понятия в титриметрическом анализе и условия его проведения
- •19.4. Измерение объемов растворов и посуда в титриметрическом анализе
- •19.5. Рабочие растворы, их приготовление. Установочные (исходные) вещества. Поправочный коэффициент
- •19.6. Способы титрования
- •19.7. Классификация методов титриметрического анализа
- •Глава 20. Кислотно-основное
- •20.1. Сущность и методы кислотно-основного титрования
- •20.2. Точка эквивалентности при кислотно-основном титровании
- •20.3. Кислотно-основные индикаторы
- •20.4. Кривые кислотно-основного титрования. Выбор индикатора
- •20.5. Стандартизация титрантов в методе кислотно-основного титрования
- •Тестовый самоконтроль по теме: «Кислотно-основное титрование»
- •20.6. Примеры определений в методе кислотно-основного титрования
- •V(hClконц) V(hClразб) • с(hClразб)
- •Глава 21. Методы окислительно-восстановительного
- •21.1. Общая характеристика и классификация методов окислительно-восстановительного титрования
- •21.2. Перманганатометрия. Характеристика метода
- •21.3. Приготовление рабочего раствора кМnО4 и его стандартизация
- •21.4. Примеры перманганатометрических определений
- •21.5. Йодометрия. Характеристика метода
- •21.6. Стандартизация рабочих растворов в йодометрии
- •21.7. Примеры йодометрических определений
- •21.8. Броматометрия и бромометрия
- •21.9. Нитритометрия
- •Глава 22. Методы осаждения
- •22.1. Общая характеристика методов и их классификация
- •22.2. Метод Мора
- •22.3. Метод Фаянса
- •22.4. Метод Фольгарда (роданометрия или тиоцианатометрия)
- •Глава 23. Комплексонометрия
- •23.1. Сущность и возможности метода
- •23.2. Основные титранты и первичные стандарты метода
- •23.3. Индикаторы комплексонометрических определений
- •23.4. Примеры комплексонометрических определений
- •Глава 24. Физико-химические
- •24.1. Сущность физико-химических методов анализа. Их классификация
- •24.2. Фотометрические методы анализа
- •24.3. Нефелометрия и турбидиметрия
- •24.4. Рефрактометрический метод анализа (рефрактометрия)
- •24.5. Потенциометрия. Потенциометрическое определение рН растворов
- •24.6. Хроматография. Сущность
3.3. Составление уравнений окислительно-восстановительных реакций электронно-ионным методом, или методом полуреакций
Для составления ОВ-реакций используются два метода: метод электронного баланса и электронно-ионный метод. Метод электронного баланса рекомендуется для уравнивания ОВ-реакций, протекающих в газовой или твердой фазах. Для составления ОВ-реакций, протекающих в водных растворах, применяется электронно-ионный метод. В данном учебном пособии он и рассматривается.
При электронно-ионном методе составляют две полуреакции. Одна из них - это окисление восстановителя, другая — восстановление окислителя. Эти две полуреакции суммируют в общее уравнение. В этом методе степени окисления элементов в составе соединений не определяют. Электронно-ионный метод характеризует процессы, которые происходят в условиях протекания реакции. В растворе нет ионов S+4, S6+, Mn7+, но есть ионы SO2-3, SO2-4, МnО-4 . Слабые электролиты, газы и практически нерастворимые вещества записывают в молекулярном виде.
При составлении ионного уравнения для каждой полуреакции надо учитывать количество атомов кислорода и водорода в исходных веществах и продуктах реакции. Баланс атомов О и Н в ОВ-реакциях, протекающих в различных средах, показан в табл. 3.2.
При протекании реакции в кислой среде в полуреакции могут быть только молекулы воды и Н+ - ионы; в щелочной среде — только молекулы воды и ОН- - ионы; в нейтральной — только молекулы воды.
Таблица 3.2. Баланс атомов кислорода и водорода в окислительно-восстановительных реакциях
Левая часть полуреакции |
Среда |
В левую часть добавить на 1 атом 0 |
В правую часть добавить |
Недостаток O
Избыток O |
pH ≤ 7 рН > 7
рН < 7 рН ≥ 7 |
Н2О 2ОН-
2Н+ Н2О |
2Н+ Н2O
Н2O 2ОН- |
Рассмотрим несколько примеров составления уравнений ОВ-реакций с помощью электронно-ионного метода.
Пример 1 (кислая среда):
Na2SO3 + КМnО4 + H2SO4 → Na2SO4 + MnSO4 + K2SO4 + H2O.
В ионной форме:
2Na+ + SO2-3 +К+ + MnO-4 + 2H+ + SO2-4 → 2Na+ + SO2-4+ 2К++ SO2-4 +H2O.
Из схемы реакции видно, что в окислении-восстановлении участвуют ионы:
SO2-3 + МnО-4 + 2Н+ → SO2-4 + Mn2+ + Н2О;
SO2-3 → SO2-4 - процесс окисления;
MnO-4 → Mn2+ - процесс восстановления.
Составим ионные уравнения для каждой полуреакции, учитывая число атомов кислорода и водорода (см. табл. 3.2). Число атомов элементов в левой и правой частях уравнения должно быть одинаково:
SO2-3 + Н2O → SO2-4 + 2H+;
МnО-4 + 8Н+ → Мn2+ + 4Н2О.
Составим электронные уравнения для каждой полуреакции, учитывая, что суммарный заряд в левой части уравнения должен быть равен суммарному заряду в правой части уравнения:
SO2-3 + Н2О - 2 ē = SO2-4 + 2H+;
МnО-4 + 8Н+ + 5 ē = Мn2+ + 4Н2О.
Общее число электронов, отдаваемых восстановителем, должно быть равно числу электронов, присоединяемых окислителем. Находим наименьшее общее кратное, на которое делятся 2 и 5. Оно равно 10. Находим коэффициенты для восстановителя и окислителя:
SO2-3 + Н2О - 2 ē = SO2-4 + 2Н+ 5
10
МnО-4 + 8Н+ + 5 ē = Мn2+ + 4Н2О 2
Суммируем электронно-ионные уравнения, предварительно умноженные на коэффициенты:
5 SO2-3 + 5Н2О + 2MnO-4 + 16H+ = 5 SO2-4 + 10Н+ + 2Мn2+ + 8Н2О.
Сократив подобные члены, получим ионное уравнение
5 SO2-3 + 2МnО-4 + 6Н+ = 5 SO2-4 + 2 Мn2+ + ЗН2О,
по которому составляют молекулярное уравнение реакции. Для этого к каждому аниону приписывают соответствующий катион, а к каждому катиону - соответствующий анион:
5Na2SO3 + 2KMnO4 + 3H2SO4 = 5Na2SO4 + 2MnSO4 + K2SO4 + 3H2O.
Пример 2 (щелочная среда):
Na2SO3 + KMnO4 + КОН → Na2SO4 + K2MnO4 + Н2О;
2Na+ + SO2-3 + К+ + МnО-4 + К+ + ОН- → 2Na+ + →+
+ 2К+ + MnO2-4 + Н2О
или SO2-3 + MnO-4 + ОН- → SO2-4 + MnO2-4+ Н2О;
SO2-3 → SO2-4 - процесс окисления;
MnO-4 → MnO2-4 - процесс восстановления.
Полуреакции:
SO2-3 + 2ОН- - 2ē = SO2-4 + Н2О 1
2
MnO-4 + ē = MnO2-4 2
SO2-3 + 2 OH- + 2 MnO-4 = SO2-4 + Н2О + 2 MnO-4.
Молекулярное уравнение реакции:
Na2SO3 + 2KMnO4 + 2KOH = Na2SO4 + 2K2MnO4 + H2O.
Пример З (нейтральная среда):
Na2SO3 + KMnO4 → Na2SO4 + MnO2↓ + ... .
SO2-3 → SO2-4 - процесс окисления;
MnO-4 → MnO2 - процесс восстановления.
Полуреакции:
SO2-3 + Н2О - 2 ē = SO2-4 + 2Н+ 3
6
MnO-4 + 2Н2О + 3 ē = MnO2 + 4ОН- 2
3 SO2-3 MnO-4 + 7 Н2О = 3 SO2-4 + 2 MnO2 + 6H+ + 8 OH-.
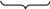
6 H2O + 2 OH-
Сокращенное ионное уравнение:
3 SO2-3 + 2MnO-4 + H2O = 3 SO2-4 + 2MnO2↓ + 2OH-.
Молекулярное уравнение реакции:
3Na2SO3 + 2KMnO4 + H2O = 3Na2SO4 + 2MnO2↓ + 2KOH.
