
- •Isbn 985-06-0828-5.
- •Введение
- •Глава 1. Растворы. Основы теории электролитической диссоциации.
- •1.1. Понятие о растворах. Процесс растворения. Растворимость веществ
- •1.2. Массовая доля растворенного вещества
- •1.3. Электролитическая диссоциация
- •1.5. Диссоциация оснований, кислот, амфотерных гидроксидов, солей в водных растворах
- •1.6. Факторы, влияющие на степень электролитической диссоциации
- •1.7. Константа электролитической диссоциации
- •1.8. Сильные электролиты и их активность
- •Глава 2. Кислотно-основное равновесие в водных растворах
- •2.1. Диссоциация воды.
- •2.2. Буферные растворы
- •2.3. Сущность гидролиза и типы гидролиза солей
- •2.4. Соли, образованные сильным основанием и слабой кислотой
- •2.5. Соли, образованные слабым основанием и сильной кислотой
- •2.6. Соли, образованные слабым основанием и слабой кислотой
- •2.7. Соли, образованные сильным основанием и сильной кислотой
- •2.8. Ступенчатый гидролиз
- •2.9. Степень гидролиза. Смещение равновесия гидролиза
- •2.10. Необратимый, или полный, гидролиз
- •Глава 3. Реакции окисления-восстановления
- •3.1. Основные положения электронной теории окислительно-восстановительных реакций
- •3.2. Окислительно-восстановительные потенциалы и направление окислительно-восстановительных реакций
- •3.3. Составление уравнений окислительно-восстановительных реакций электронно-ионным методом, или методом полуреакций
- •3.4. Применение реакций окисления-восстановления в химическом анализе
- •Глава 4. Комплексные соединения
- •4.2. Природа химической связи в комплексных ионах
- •4.3. Классификация и номенклатура комплексных соединений
- •4.4. Диссоциация комплексных соединений. Константы нестойкости и устойчивости
- •4.5. Внутрикомплексные соединения
- •4.6 Применение комплексных соединений в медицине и химическом анализе
- •Глава 5. Гетерогенные равновесия и процессы
- •5.1. Константа растворимости
- •5.2. Взаимосвязь между растворимостью и константой растворимости
- •5.3. Условия образования осадков
- •5.4. Условия растворения осадков
- •5.5. Понятие о коллоидных растворах
- •Часть II
- •Глава 6. Основы качественного анализа
- •6.1. Методы качественного анализа
- •6.2. Чувствительность и специфичность реакций. Дробный и систематический анализ
- •6.3. Понятие о химических реактивах
- •6.4. Аналитическая классификация катионов
- •Глава 7. Устройство и оборудование лаборатории
- •7.1. Требования к помещению лаборатории
- •7.2. Оборудование и посуда для полумикроанализа
- •7.3. Мытье химической посуды
- •Глава 8. Первая аналитическая группа катионов
- •8.1. Общая характеристика группы
- •8.2. Биологическая роль катионов первой аналитической группы. Применение соединений катионов первой аналитической группы в медицине
- •8.3. Частные реакции катионов первой аналитической группы
- •8.4. Анализ смеси катионов первой аналитической группы
- •Глава 9. Вторая аналитическая группа катионов
- •9.1.Общая характеристика группы. Действие группового реагента
- •9.2. Биологическая роль катионов второй аналитической группы. Применение соединений катионов второй аналитической группы в медицине
- •9.3. Частные реакции катионов второй аналитической группы
- •9.4. Анализ смеси катионов второй аналитической группы
- •2. Исследование осадка:
- •Глава 10. Третья аналитическая группа катионов
- •10.1.Общая характеристика группы. Действие группового реагента
- •10.2. Биологическая роль катионов третьей аналитической группы. Применение соединений катионов третьей аналитической группы в медицине
- •10.3. Частные реакции катионов третьей аналитической группы
- •10.4. Анализ смеси катионов третьей аналитической группы
- •10.5. Систематический анализ смеси катионов первой, второй и третьей аналитических групп
- •Вопросы
- •Глава 11. Четвертая аналитическая
- •11.1. Общая характеристика группы. Действие группового реагента
- •11.2. Биологическая роль катионов четвертой аналитической группы. Применение соединений катионов четвертой аналитической группы в медицине
- •11.3. Частные реакции катионов четвертой аналитической группы
- •11.4. Анализ смеси катионов четвертой аналитической группы
- •Глава 12. Пятая аналитическая группа катионов
- •12.1. Общая характеристика группы. Действие группового реагента
- •12.2. Биологическая роль катионов пятой аналитической группы. Применение соединений катионов пятой группы в медицине
- •12.3. Частные реакции катионов пятой аналитической группы
- •12.4. Ход анализа смеси катионов пятой аналитической группы
- •Глава 13. Шестая аналитическая группа катионов
- •13.1. Общая характеристика группы. Действие группового реагента
- •13.2. Биологическая роль катионов шестой аналитической группы. Применение соединений катионов шестой аналитической группы в медицине
- •13.3. Частные реакции катионов шестой аналитической группы
- •13.4. Анализ смеси катионов шестой аналитической группы
- •13.5. Систематический анализ смеси катионов всех аналитических групп
- •13.6. Ситуационные задачи по обнаружению катионов в исследуемом растворе
- •Глава 14. Общая характеристика
- •14.1. Биологическая роль элементов, входящих в состав анионов
- •14.2. Частные реакции анионов первой аналитической группы. Действие группового реагента
- •14.3. Частные реакции анионов второй аналитической группы. Действие группового реагента
- •14.4. Частные реакции анионов третьей аналитической группы
- •Глава 15. Систематический ход
- •15.1. Предварительные испытания
- •15.2. Обнаружение анионов первой аналитической группы
- •15.3. Обнаружение анионов второй аналитической группы
- •15.4. Обнаружение анионов третьей аналитической группы
- •15.5. Ситуационные задачи по обнаружению анионов в исследуемом растворе
- •Глава 16. Анализ неорганического
- •16.1. Установление аналитической группы катиона. Обнаружение катиона
- •16.2. Установление аналитической группы аниона. Обнаружение аниона
- •16.3. Анализ смеси нескольких солей
- •Часть III
- •Глава 17. Основные принципы количественного анализа
- •17.1. Задачи и методы количественного анализа
- •17.2. Подготовка вещества к анализу. Отбор проб для анализа
- •17.3. Лабораторные технические и аналитические весы
- •Глава 18. Гравиметрический (весовой) анализ
- •18.1. Сущность гравиметрического анализа
- •18.2. Посуда и оборудование в гравиметрическом анализе
- •18.3. Осаждение. Влияние различных факторов на образование осадков
- •18.4. Техника выполнения операций при проведении гравиметрического анализа
- •18.5. Примеры гравиметрических определений
- •Глава 19. Титриметрическии (объемный) анализ
- •19.1. Моль. Молярная масса. Химический эквивалент. Молярная масса эквивалента. Фактор эквивалентности
- •19.2. Способы выражения состава раствора
- •19.3. Основные понятия в титриметрическом анализе и условия его проведения
- •19.4. Измерение объемов растворов и посуда в титриметрическом анализе
- •19.5. Рабочие растворы, их приготовление. Установочные (исходные) вещества. Поправочный коэффициент
- •19.6. Способы титрования
- •19.7. Классификация методов титриметрического анализа
- •Глава 20. Кислотно-основное
- •20.1. Сущность и методы кислотно-основного титрования
- •20.2. Точка эквивалентности при кислотно-основном титровании
- •20.3. Кислотно-основные индикаторы
- •20.4. Кривые кислотно-основного титрования. Выбор индикатора
- •20.5. Стандартизация титрантов в методе кислотно-основного титрования
- •Тестовый самоконтроль по теме: «Кислотно-основное титрование»
- •20.6. Примеры определений в методе кислотно-основного титрования
- •V(hClконц) V(hClразб) • с(hClразб)
- •Глава 21. Методы окислительно-восстановительного
- •21.1. Общая характеристика и классификация методов окислительно-восстановительного титрования
- •21.2. Перманганатометрия. Характеристика метода
- •21.3. Приготовление рабочего раствора кМnО4 и его стандартизация
- •21.4. Примеры перманганатометрических определений
- •21.5. Йодометрия. Характеристика метода
- •21.6. Стандартизация рабочих растворов в йодометрии
- •21.7. Примеры йодометрических определений
- •21.8. Броматометрия и бромометрия
- •21.9. Нитритометрия
- •Глава 22. Методы осаждения
- •22.1. Общая характеристика методов и их классификация
- •22.2. Метод Мора
- •22.3. Метод Фаянса
- •22.4. Метод Фольгарда (роданометрия или тиоцианатометрия)
- •Глава 23. Комплексонометрия
- •23.1. Сущность и возможности метода
- •23.2. Основные титранты и первичные стандарты метода
- •23.3. Индикаторы комплексонометрических определений
- •23.4. Примеры комплексонометрических определений
- •Глава 24. Физико-химические
- •24.1. Сущность физико-химических методов анализа. Их классификация
- •24.2. Фотометрические методы анализа
- •24.3. Нефелометрия и турбидиметрия
- •24.4. Рефрактометрический метод анализа (рефрактометрия)
- •24.5. Потенциометрия. Потенциометрическое определение рН растворов
- •24.6. Хроматография. Сущность
2.3. Сущность гидролиза и типы гидролиза солей
В общем случае под гидролизом понимают реакцию разложения вещества водой (от греч. «гидро» - вода, «лизис» - разложение). Гидролизу могут подвергаться белки, жиры, углеводы, эфиры и другие вещества. В неорганической химии чаще всего встречаются с гидролизом солей.
Гидролизом соли называется взаимодействие ионов соли с ионами воды, которое приводит к образованию слабых электролитов.В результате гидролиза солей их водные растворы показывают кислую, щелочную или нейтральную реакцию среды. Как известно, реакция среды зависит от концентрации ионов водорода Н+ или гидроксид-ионов ОН-.
Вода является слабым электролитом и диссоциирует по уравнению
Н2О ↔ Н+ + ОН-.
Появление избытка ионов Н+ или ОН- в растворе объясняется тем, что ионы соли реагируют с ионами воды. Равновесие диссоциации воды смещается вправо, так как при гидролизе солей образуются слабые электролиты:

В зависимости от природы соли в растворе накапливаются либо ионы Н+, либо ОН-, которые и определяют реакцию среды.
Гидролиз соли - это реакция, обратная реакции нейтрализации. Поэтому каждую соль можно представить себе как соединение, образованное основанием и кислотой. Кислоты и основания бывают сильными или слабыми электролитами. В зависимости от силы исходной кислоты и исходного основания различают четыре типа солей:
• образованные сильным основанием и слабой кислотой;
• образованные слабым основанием и сильной кислотой;
• образованные слабым основанием и слабой кислотой;
• образованные сильным основанием и сильной кислотой.
2.4. Соли, образованные сильным основанием и слабой кислотой
В водном растворе цианида калия соль полностью распадается на ионы калия К+ и цианид-ионы CN-. Ионы калия К+ и гидроксид-ионы ОН- могут находиться в растворе одновременно в значительных количествах. Ионы водорода Н+ и цианид-ионы CN- взаимодействуют между собой с образованием циановодородной кислоты (Кд = 6,02 • 10-10). Этот процесс схематически может быть представлен следующим образом:
KCN → К+ + CN-
Н2О ↔ ОН- + Н+
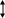
HCN
В результате гидролиза такой соли в растворе находятся полностью продиссоциированная щелочь и слабо диссоциированная кислота. Эта кислота частично диссоциирует на ионы и возвращает в раствор часть ионов Н+ и CN-. Возникает обратная реакция и устанавливается динамическое химическое равновесие:
К+ + CN- + Н2О ↔ К+ + ОН- + HCN.
Следовательно, реакция между цианидом калия и водой является обратимой и проходит не полностью. Такое явление называется обратимым гидролизом.
В результате того, что в растворе образуется сильный электролит гидроксид калия, концентрация гидроксид-ионов ОН- будет значительно больше концентрации ионов водорода Н+. В растворе соли возникает щелочная среда, т.е. рН > 7. Действительно, эксперимент показывает, что 0,1М раствор этой соли имеет рН 11,1. Гидролиз цианида калия в сокращенной ионной форме можно представить уравнением
К+ + CN- + Н2О ↔ К+ + ОН- + HCN.
Подобно раствору KCN, раствор ацетата натрия также имеет щелочную среду, что видно из молекулярного и сокращенного ионного уравнений гидролиза:
CH3COONa + Н2О ↔ СН3СООН + NaOH;
СН3СОО- + Н2О ↔ СН3СООН + ОН-.
Сокращенное ионное уравнение показывает, что гидролиз соли, образованной сильным основанием и слабой кислотой, идет цо аниону слабой кислоты и реакция среды становится щелочной.
