
- •Оглавление
- •Часть I. Механика 4
- •Часть II. Молекулярная физика и термодинамика 81
- •Часть I. Механика
- •Кинематика
- •Основные понятия кинематики
- •З.2. Скорость
- •Среднее ускорение
- •Мгновенное ускорение
- •Ускорение точки при прямолинейном движении
- •Кинематика вращательного движения
- •4. Динамика
- •Закон всемирного тяготения
- •2). Сила тяжести
- •3). Сила реакции опоры
- •4). Сила трения
- •Виды трения
- •5). Сила упругости
- •4.4. Импульс. Закон сохранения импульса
- •История появления термина
- •4.5. Законы Ньютона
- •Замечания:
- •4.6. Энергия
- •Потенциальная энергия тела, поднятого над поверхностью Земли
- •Закон сохранения энергии в механике
- •4.7. Динамика вращательного движения
- •2). Пара сил
- •Момент импульса
- •Механический (классический) принцип относительности (принцип относительности Галилея)
- •Основы механики жидкостей и газов
- •Архимед из СиракузArchimedes of Siracuse, ок. 287–212 г. До н. Э.
- •Условие плавания тел
- •Вязкость газов
- •Часть II. Молекулярная физика и термодинамика
- •I. Молекулярная физика
- •1.1. Предмет молекулярной физики
- •1.2. Внесистемные единицы измерения величин в микрофизике физике
- •1.3. Основные положения молекулярно-кинетической теории строения вещества
- •1.4. Число степеней свободы молекул
- •1.5. Термодинамическая система. Термодинамические состояние и процесс
- •1.6. Статистический метод в молекулярной физике
- •1.7. Количество вещества. Масса молекул
- •1.8. Идеальный газ
- •1.9. Закон равномерного распределения энергии по степеням свободы молекул
- •1.10. Закон Максвелла25 о распределении молекул идеального газа по скоростям
- •Вывод распределения по Максвеллу
- •Границы применимости
- •Зависимость функции распределения Максвелла от температуры.
- •Характерные скорости Наиболее вероятная скорость
- •Средняя скорость
- •1.11. Основное уравнение молекулярно – кинетической теории (уравнение Клаузиуса26)
- •1.12. Уравнение Менделеева27 - Клапейрона28
- •1.13. Барометрическая формула. Распределение Больцмана
- •1.14. Средняя длина свободного пробега молекул
- •II. Термодинамика
- •2 .1. Термодинамический метод
- •2.2. Внутренняя энергия
- •Два способа изменения внутренней энергии. Теплота и работа
- •Первое начало термодинамики
- •Нулевое начало термодинамики
- •Теплоёмкость
- •1). Молярная теплоёмкость идеального газа при постоянном объёме
- •2). Молярная теплоёмкость идеального газа при постоянном давлении Уравнение Майера
- •Термический кпд для кругового процесса
- •Из истории тепловых двигателей
- •Цикл Карно38
- •Второе начало термодинамики
- •Энтропия
- •2.16. Статистическая интерпретация второго начала термодинамики
- •Реальные газы
- •Жидкости
- •Твёрдые тела
- •Изоморфизм и полиморфизм кристаллов
- •Кристаллические вещества Типы кристаллических решеток
- •Общая характеристика
- •Классификация решёток по симметрии
- •Объём ячейки
Жидкости
Жи́дкость — вещество, находящееся в жидком агрегатном состоянии, занимающем промежуточное положение между твёрдым и газообразным состояниями. Основным свойством жидкости, отличающим её от веществ, находящихся в других агрегатных состояниях, является способность неограниченно менять форму под действием касательных механических напряжений, даже сколь угодно малых, практически сохраняя при этом объём.
Общая информация о жидком солстоянии
Жидкое состояние обычно считают промежуточным между твёрдым телом и газом: газ не сохраняет ни объём, ни форму, а твёрдое тело сохраняет и то, и другое.
Форма жидких тел может полностью или отчасти определяться тем, что их поверхность ведёт себя как упругая мембрана. Так, вода может собираться в капли. Но жидкость способна течь даже под своей неподвижной поверхностью, и это тоже означает несохранение формы (внутренних частей жидкого тела).
Молекулы жидкости не имеют определённого положения, но в то же время им недоступна полная свобода перемещений. Между ними существует притяжение, достаточно сильное, чтобы удержать их на близком расстоянии.
Вещество в жидком состоянии существует в определённом интервале температур, ниже которого переходит в твердое состояние (происходит кристаллизация либо превращение в твердотельное аморфное состояние — стекло), выше — в газообразное (происходит испарение). Границы этого интервала зависят от давления.
Как правило, вещество в жидком состоянии имеет только одну модификацию. (Наиболее важные исключения — это квантовые жидкости и жидкие кристаллы.) Поэтому в большинстве случаев жидкость является не только агрегатным состоянием, но и термодинамической фазой (жидкая фаза).
Все жидкости принято делить на чистые жидкости и смеси. Некоторые смеси жидкостей имеют большое значение для жизни: кровь, морская вода и др. Жидкости могут выполнять функцию растворителей.
Физические свойства жидкостей
1).Текучесть
Основным свойством жидкостей является текучесть. Если к участку жидкости, находящейся в равновесии, приложить внешнюю силу, то возникает поток частиц жидкости в том направлении, в котором эта сила приложена: жидкость течёт. Таким образом, под действием неуравновешенных внешних сил жидкость не сохраняет форму и относительное расположение частей, и поэтому принимает форму сосуда, в котором находится.
В отличие от пластичных твёрдых тел, жидкость не имеет предела текучести: достаточно приложить сколь угодно малую внешнюю силу, чтобы жидкость потекла.
2).Сохранение объёма
Одним из характерных свойств жидкости является то, что она имеет определённый объём (при неизменных внешних условиях). Жидкость чрезвычайно трудно сжать механически, поскольку, в отличие от газа, между молекулами очень мало свободного пространства. Давление, производимое на жидкость, заключенную в сосуд, передаётся без изменения в каждую точку объёма этой жидкости (закон Паскаля, справедлив также и для газов). Эта особенность, наряду с очень малой сжимаемостью, используется в гидравлических машинах.
Жидкости обычно увеличивают объём (расширяются) при нагревании и уменьшают объём (сжимаются) при охлаждении. Впрочем, встречаются и исключения, например, вода сжимается при нагревании, при нормальном давлении и температуре от 0 °C до приблизительно 4 °C.
3). Вязкость
Кроме того, жидкости (как и газы) характеризуются вязкостью. Она определяется как способность оказывать сопротивление перемещению одной из частей относительно другой — то есть как внутреннее трение.
Когда соседние слои жидкости движутся относительно друг друга, неизбежно происходит столкновение молекул дополнительно к тому, которое обусловлено тепловым движением. Возникают силы, затормаживающие упорядоченное движение. При этом кинетическая энергия упорядоченного движения переходит в тепловую — энергию хаотического движения молекул.
Жидкость в сосуде, приведённая в движение и предоставленная самой себе, постепенно остановится, но её температура повысится.
4).Смешиваемость
Смешиваемость — способность жидкостей растворяться друг в друге. Пример смешиваемых жидкостей: вода и этиловый спирт, пример несмешиваемых: вода и жидкое масло.
5). Образование свободной поверхности и поверхностное натяжение
Из-за сохранения объёма жидкость способна образовывать свободную поверхность. Такая поверхность является поверхностью раздела фаз данного вещества: по одну сторону находится жидкая фаза, по другую — газообразная (пар), и, возможно, другие газы, например, воздух.
Если жидкая и газообразная фазы одного и того же вещества соприкасаются, возникают силы, которые стремятся уменьшить площадь поверхности раздела — силы поверхностного натяжения. Поверхность раздела ведёт себя как упругая мембрана, которая стремится стянуться.
6).Волны плотности
Хотя жидкость чрезвычайно трудно сжать, тем не менее, при изменении давления её объем и плотность всё же меняются. Это происходит не мгновенно; так, если сжимается один участок, то на другие участки такое сжатие передаётся с запаздыванием. Это означает, что внутри жидкости способны распространяться упругие волны, более конкретно, волны плотности. Вместе с плотностью меняются и другие физические величины, например, температура.
Если при распространении волны́ плотность меняется достаточно слабо, такая волна называется звуковой волной, или звуком.
Если плотность меняется достаточно сильно, то такая волна называется ударной волной. Ударная волна описывается другими уравнениями.
Волны плотности в жидкости являются продольными, то есть плотность меняется вдоль направления распространения волны. Поперечные упругие волны в жидкости отсутствуют из-за несохранения формы.
Упругие волны в жидкости со временем затухают, их энергия постепенно переходит в тепловую энергию. Причины затухания — вязкость, «классическое поглощение», молекулярная релаксация и другие. При этом работает так называемая вторая, или объёмная вязкость — внутреннее трение при изменении плотности. Ударная волна в результате затухания через какое-то время переходит в звуковую.
Упругие волны в жидкости подвержены также рассеянию на неоднородностях, возникающих в результате хаотического теплового движения молекул.
Строение жидкостей
Экспериментальные исследования жидкого состояния вещества, основанные на наблюдении дифракции рентгеновских лучей и потоков нейтронов при прохождении их через жидкие среды, обнаружили наличие в жидкости ближнего порядка49, т.е. наличие некоторой упорядоченности в расположении частиц лишь на малом расстоянии от какой-либо выделенной позиции (рис. 140).

Рис. 140. Дальний и ближний порядок : а – двумерная модель твердого тела, иллюстрирующая наличие дальнего порядка; б – двумерная модель жидкости, иллюстрирующая наличие только ближнего порядка.
Взаимное расположение соседних частиц в жидкостях сходно с упорядоченным расположением соседних частиц в кристаллах. Однако, эта упорядоченность в жидкостях наблюдается лишь внутри малых объёмов. При расстояниях r > (3 4) d от некоторой выбранной «центральной» молекулы упорядоченность нарушается (d- эффективный диаметр молекулы). Подобная упорядоченность в расположении частиц в жидкостях и называется ближним порядком.
Из – за отсутствия дальнего порядка жидкости, за немногим исключением, не обнаруживают анизотропии, характерной для кристаллов. По этой причине структуру жидкости иногда называют квазикристаллической или кристаллоподобной.
Впервые идея о близости некоторых свойств жидкостей (особенно расплавов металлов) и кристаллических твердых тел была высказана и затем развивалась в работах советского физика Я.И.Френкеля еще 1930–1940-х. Согласно взглядам Френкеля, получившим теперь всеобщее признание, тепловое движение атомов и молекул в жидкости состоит из нерегулярных колебаний со средней частотой, близкой к частоте колебаний атомов в кристаллических телах. Центр колебаний определяется при этом полем сил соседних частиц и смещается вместе со смещениями этих частиц.
Упрощенно можно представить такое тепловое движение как наложение друг на друга сравнительно редких перескоков частиц из одних временных положений равновесия в другие и тепловых колебаний в промежутках между скачками. Среднее время < > «оседлого» пребывания молекулы жидкости вблизи некотрого положения равновесия называется временем релаксации. По истечеии времени < > молекула меняет место равновесия, скачком перемещаясь в новое положение, отстоящее от предыдущего на расстояние порядка размеров самих молекул. Таким образом, молекула медленно перемещается внутри жидкости. С ростом температуры время < > уменьшается, подвиждность молекул возрасчтает, что влечёт за собой уменьшенине вязкости жидкостей (возрастает текучесть). По образному выражению Я.И.Френкеля, молекулы странствуют по всему объему жидкости, ведя кочевой образ жизни, при котором кратковременные переезды сменяются относительно длинными периодами оседлой жизни.
Аморфные твёрдые тела (стекло, смолы, битум и т.д.) можно рассматривать как переохлаждённые жидкости, частицы которых из-за сильно возросшей вязкости имеют ограниченную подвижность.
Из-за малой упорядоченности жидкого состояния теория жидкости оказывается менее развитой, чем теория газов и кристаллических твердых тел. Пока нет полной теории жидкости.
Особый тип жидкостей – это некоторые органические соединения, состоящие из молекул удлиненной или дискообразной формы, или так называемые жидкие кристаллы. Взаимодействие между молекулами в таких жидкостях стремится выстроить длинные оси молекул в определенном порядке. При высоких температурах тепловое движение препятствует этому, и вещество представляет собой обычную жидкость. При температурах ниже критической в жидкости появляется выделенное направление, возникает дальний ориентационный порядок. Сохраняя основные черты жидкости, например, текучесть, жидкие кристаллы обладают характерными свойствами твердых кристаллов – анизотропией магнитных, электрических и оптических свойств. Эти их свойства (наряду с текучестью) находят многочисленные технические применения, например в электронных часах, калькуляторах, мобильных телефонах, а также в мониторах персональных компьютеров, телевизорах, в качестве индикаторов, табло и экранов для отображения цифровой, буквенной и аналоговой информации.
Поверхностное натяжение
Наиболее
интересной особенностью жидкостей
является наличие свободной поверхности.
С поверхностью жидкости связана свободная
энергия, пропорциональная
площади S свободной
поверхности жидкости: Есв..= S.
Так как свободная энергия изолированной
системы стремится к минимуму, то жидкость
(в отсутствие внешних полей) стремится
принять форму, имеющую минимальную
площадь поверхности. Таким образом,
задача о форме жидкости сводится к
изопериметрической
задаче при заданных
дополнительных условиях (начальное
распределение, объём и т. п.).
Свободная капля принимает форму шара,
однако при более сложных условиях задача
о форме поверхности жидкости становится
исключительно сложной.
S.
Так как свободная энергия изолированной
системы стремится к минимуму, то жидкость
(в отсутствие внешних полей) стремится
принять форму, имеющую минимальную
площадь поверхности. Таким образом,
задача о форме жидкости сводится к
изопериметрической
задаче при заданных
дополнительных условиях (начальное
распределение, объём и т. п.).
Свободная капля принимает форму шара,
однако при более сложных условиях задача
о форме поверхности жидкости становится
исключительно сложной.
Жидкость, в отличие от газов, не заполняет весь объем сосуда, в который она налита. Между жидкостью и газом (или паром) образуется граница раздела, которая находится в особых условиях по сравнению с остальной массой жидкости. Молекулы в пограничном слое жидкости, в отличие от молекул в ее глубине, окружены другими молекулами той же жидкости не со всех сторон. Силы межмолекулярного взаимодействия, действующие на одну из молекул внутри жидкости со стороны соседних молекул, в среднем взаимно скомпенсированы (рис. 141).

Рис. 141.
Любая молекула в пограничном слое притягивается молекулами, находящимися внутри жидкости (силами, действующими на данную молекулу жидкости со стороны молекул газа (или пара) можно пренебречь. В результате появляется некоторая равнодействующая сила, направленная вглубь жидкости. Поверхностные молекулы силами межмолекулярного притяжения втягиваются внутрь жидкости (рис. 142).

Рис. 142.
Но все молекулы, в том числе и молекулы пограничного слоя, должны находиться в состоянии равновесия. Это равновесие достигается за счет некоторого уменьшения расстояния между молекулами поверхностного слоя и их ближайшими соседями внутри жидкости. При уменьшении расстояния между молекулами возникают силы отталкивания. Молекулы поверхностного слоя упакованы несколько более плотно, а поэтому они обладают дополнительным запасом потенциальной энергии по сравнению с внутренними молекулами. Следовательно, молекулы поверхностного слоя жидкости обладают избыточной по сравнению с молекулами внутри жидкости потенциальной энергией П, равной свободной энергии Есв.. Таким образом, потенциальная энергия поверхности жидкости пропорциональна ее площади: П = S.
Из механики известно, что равновесным состояниям системы соответствует минимальное значение ее потенциальной энергии, т.е. свободная поверхность жидкости стремится сократить свою площадь. Жидкость ведет себя так, как будто по касательной к ее поверхности действуют силы, сокращающие (стягивающие) эту поверхность. Эти силы i называются силами поверхностного натяжения.
Выберем на поверхности жидкости некоторый замкнутый контур L. Для всех молекул, лежащих внутри этого контура, все силы i, взаимно уравновешиваются. Однако для молекул, расположенных вдоль контура L, силы i направлены наружу, являются внешними силами; они перпендикулярны периметру и касательные к поверхности жидкости. Эти силы, растягивающие плёнку, и являются силами поверхностного натяжения (рис. 143).

Рис. 143.
Сила поверхностного натяжения направлена по касательной к поверхности жидкости, перпендикулярно к участку контура, на который она действует и пропорциональна длине этого участка: i = l.
Наличие сил поверхностного натяжения делает поверхность жидкости похожей на упругую растянутую пленку, с той только разницей, что упругие силы в пленке зависят от площади ее поверхности (т. е. от того, как пленка деформирована), а силы поверхностного натяжения не зависят от площади поверхности жидкости.
Поверхностное натяжение - стремление жидкости уменьшить избыток своей потенциальной энергии на границе раздела с другой фазой (поверхностную энергию).
Таким образом, поверхностное натяжение имеет двойной физический смысл — энергетический (термодинамический) и силовой (механический). Энергетическое (термодинамическое) определение: поверхностное натяжение — это удельная работа увеличения поверхности при её растяжении при условии постоянства температуры. Силовое (механическое) определение: поверхностное натяжение — это сила, действующая на единицу длины линии, которая ограничивает поверхность жидкости.
Следует иметь в виду, что вследствие крайне низкой сжимаемости наличие более плотно упакованного поверхностного слоя не приводит к сколь-нибудь заметному изменению объема жидкости. Если молекула переместится с поверхности внутрь жидкости, силы межмолекулярного взаимодействия совершат положительную работу. Наоборот, чтобы вытащить некоторое количество молекул из глубины жидкости на поверхность (т. е. увеличить площадь поверхности жидкости), внешние силы должны совершить положительную работу ΔAвнеш. = П, пропорциональную изменению ΔS площади поверхности: ∆Авнешн.= ∆S, где называется коэффициентом поверхностного натяжения (σ > 0).
Таким
образом, с точки зрения энергетической:
коэффициент
поверхностного натяжения равен
работе, необходимой для увеличения
площади поверхности жидкости при
постоянной температуре на единицу:
=
Коэффициент поверхностного натяжения зависит от химического состава жидкости и её температуры. С увеличением температуры уменьшается и обращается в нуль при критической температуре. При введении в жидкости примесей, поверхносто-активных веществ коэффициент поверхностного натяжения уменьшается. Так как появление поверхности жидкости требует совершения работы, каждая среда «стремится» уменьшить площадь своей поверхности:
Обычно мы наблюдаем жидкости, подверженные действию сил земного тяготения. При этом жидкость принимает форму, соответствующую минимуму суммарной энергии – энергии в поле силы тяготения и поверхностной энергии. Было доказано теоретически, что понятие поверхностного натяжения жидкости однозначно является частью понятия внутренней энергии. Поверхностное натяжение может быть на границе газообразных, жидких и твёрдых тел. Обычно имеется в виду поверхностное натяжение жидких тел на границе «жидкость — газ». В случае жидкой поверхности раздела поверхностное натяжение правомерно также рассматривать как силу, действующую на единицу длины контура поверхности и стремящуюся сократить поверхность до минимума при заданных объёмах фаз. Прибор для измерения поверхностного натяжения называется тензиометром. Пример. Некоторые жидкости, как, например, мыльная вода, обладают способностью образовывать тонкие пленки. Всем хорошо известные мыльные пузыри имеют правильную сферическую форму – в этом тоже проявляется действие сил поверхностного натяжения. Если в мыльный раствор опустить проволочную рамку, одна из сторон которой подвижна, то вся она затянется пленкой жидкости (рис. 144).
Силы поверхностного натяжения стремятся сократить поверхность пленки. Для равновесия подвижной стороны рамки к ней нужно приложить внешнюю силу:
вн.
=
Если
под действием силы
вн
перекладина переместится на Δx,
то будет произведена работа
ΔAвн = FвнΔx = ΔEp = σΔS,
где ΔS = 2LΔx
– приращение площади поверхности
обеих сторон мыльной пленки. Так как
модули сил
вн
и
н.одинаковы,
можно записать:
Давление под изогнутой поверхностью жидкости. Формула Лапласа Известно, что поверхность жидкости около стенок сосуда искривляется. Свободная поверхность жидкости, искривлённая около стенок сосуда, называется мениском (рис. 145).
Рис. 145. Краевые углы смачивающей (1) и несмачивающей (2) жидкостей. Рассмотрим тонкую жидкую плёнку, толщиной которой можно пренебречь. Стремясь минимизировать свою свободную энергию, плёнка создаёт разность давления с разных сторон. Из-за действия сил поверхностного натяжения в каплях жидкости и внутри мыльных пузырей возникает добавочное давление ΔР (плёнка сжимается до тех пор, пока давление внутри пузыря не будет превышать атмосферное на величину добавочного давления плёнки ΔР). Рассмотрим поверхность жидкости, опирающуюся на некоторый плоский контур (рис.146, а). Если поверхность жидкости не плоская, то стремление ее к сокращению и приведет к возникновению давления ∆Р, дополнительного к тому, которое испытывает жидкость с плоской поверхностью. В случае выпуклой поверхности это дополнительное давление положительно (рис. 146, б), в случае вогнутой поверхности — отрицательно (рис. 146, в). В последнем случае поверхностный слой, стремясь сократиться, растягивает жидкость.
Рис. 146. Величина добавочного давления, очевидно, должна возрастать с увеличением коэффициента поверхностного натяжения и кривизны поверхности R. Вычислим добавочное давление для сферической поверхности жидкости. Для этого рассечем мысленно сферическую каплю жидкости диаметральной плоскостью на два полушария (рис. 147). Из-за поверхностного натяжения оба полушария притягиваются друг к другу с силой, равной: F = l = 2 R .
Эта
сила прижимает друг к другу оба
полушария по поверхности и, следовательно,
обусловливает дополнительное давление:
∆P
=
=
Кривизна сферической поверхности всюду одинакова и определяется радиусом сферы R. Очевидно, что чем меньше R, тем больше кривизна сферической поверхности.
Рис. 147.
Избыточное
давление внутри мыльного пузыря в
два раза больше, так как пленка имеет
две поверхности: ∆P
=
Добавочное давление обусловливает изменение уровня жидкости в узких трубках (капиллярах), вследствие чего называется иногда капиллярным давлением. Кривизну произвольной поверхности принято характеризовать так называемой средней кривизной <K>, которая может оказаться различной для разных точек поверхности50.
Величина
R
дает кривизну сферы. В геометрии
доказывается, что полусумма обратных
радиусов кривизны для любой пары
взаимно перпендикулярных нормальных
сечений имеет одно и то же значение:
<K>= Эта величина и есть средняя кривизна поверхности в данной точке. В этой формуле радиусы R1,2 — алгебраические величины. Если центр кривизны нормального сечения находится под данной поверхностью, соответствующий радиус кривизны положителен; если центр кривизны лежит над поверхностью, радиус кривизны отрицателен (рис.148). Таким образом, неплоская поверхность может иметь среднюю кривизну, равную нулю. Для этого нужно, чтобы радиусы кривизны были одинаковы по величине и противоположны по знаку.
Например,
для сферы центры кривизны в любой
точке поверхности совпадают с центром
сферы, поэтому R1
= R2
= R
и ∆P
=
.Для
случая поверхности кругового цилиндра
радиуса R
имеем: R1
= R;
R2
=
и ∆P
=
Можно доказать, что для поверхности любой формы справедливо соотношение: ∆P=2<K>. (2) Подставив в формулу (2) выражение (1), получим формулу добавочного давления под произвольной поверхностью, называемую формулой Лапласа (рис. 148):
∆P
=
(
Рис. 148. Радиусы R1 и R2 в формуле (3) — алгебраические величины. Если центр кривизны нормального сечения находится под данной поверхностью, соответствующий радиус кривизны положителен; если центр кривизны лежит над поверхностью, радиус кривизны отрицателен.
Пример.
Если
в жидкости имеется пузырек газа, то
поверхность пузырька, стремясь
сократиться, будет оказывать на газ
дополнительное давление ∆P
=
.
Найдем радиус пузырька в воде, при
котором добавочное давление ∆P равно
1
aтм.
(105
Па).
Коэффициент поверхностного натяжения
воды при 20°С
равен
Явления на границе жидкости и твёрдого тела На краю поверхности жидкости, находящейся в сосуде, мы имеем дело с соприкосновением трёх сред: твёрдой, жидкой и газообразной. В этом случае вся система принимает конфигурацию, соответствующую минимуму суммарной энергии (поверхностной, в поле силы тяжести и т.п.).
Вблизи границы между жидкостью, твердым телом и газом форма свободной поверхности жидкости зависит от сил взаимодействия молекул жидкости с молекулами твердого тела (взаимодействием с молекулами газа (или пара) можно пренебречь) и принимает форму мениска. Для характеристики мениска вводится краевой угол между смоченной поверхностью стенки и мениском в точках их пересечения (рис. 145). Если эти силы взаимодействия между жидкостью и твердым телом больше сил взаимодействия между молекулами самой жидкости, то жидкость смачивает поверхность твердого тела. В этом случае жидкость подходит к поверхности твердого тела под острым углом θ, характерным для данной пары жидкость – твердое тело (рис. 146 б). Если силы взаимодействия между молекулами жидкости превосходят силы их взаимодействия с молекулами твердого тела, то краевой угол θ оказывается тупым (рис. 146 а). В этом случае говорят, что жидкость не смачивает поверхность твердого тела. Для количественного описания смачивания жидкостью твердого тела рассмотрим равновесие сил, действующих на элемент l контура, образованного пересечением трех границ раздела фаз: газа 1, жидкости 2 и твердого тела 3 (см. рис. 146).
На
рис. 146
12
=
В
проекции на горизонтальную ось можно
записать условие равновесия (рис
146):
где проведено сокращение на величину длины элемента контура l.
Из
формулы (1)
имеем:
=
Как следует из этой формулы, равновесию жидкости на поверхности твердого тела соответствует вполне определенный угол . Этот угол может принимать значения от 0 до .
Так
как |
Если
это условие не выполняется, капля
либо, при
<1
начинает
неограниченно (до толщины нескольких
мономолекулярных слоев) растекаться
по поверхности, либо, при
<
1,
стягиваться
до тех пор, пока её общая граница с
поверхностью не превратится в точку.
В первом случае наблюдается явление
полного
смачивания
твердого тела жидкостью (например,
капля керосина на поверхности стекла),
а во втором - полное
несмачиваение
(например, капля воды на поверхности
парафина). Если краевой угол 0<
Таким образом, угол зависит только от природы трёх соприкасающихся сред. Рассмотрим частные случаи, следующие из формулы (1): 1). > > 0 < – смачивание (рис. 149).
Рис. 149. Капля жидкости растекается по поверхности. 2). < < 0 > – несмачивание, (рис. 150).
Рис. 150. 3). = 0 – полное (идеальное) смачивание. 4). = - полное (идеальное) несмачивание. 5). = – отсутствуют смачивание и несмачивание, жидкость имеет плоскую поверхность. Из
формулы (2) видно, что во всяком реальном
случае устойцчивого равновесия
жидкости у стенки должно выполняться
условие: |
|
Капиллярные51 явления Капиллярные явления – физические явления, обусловленные поверхностным натяжением на границе раздела несмешивающихся сред (в узком смысле: явления изменения высоты уровня жидкости в капиллярах по сравнению с уровнем жидкости в широких сосудах). К капиллярным явлениям относят обычно явления в жидких средах, вызванные искривление их поверхности, граничащей с другой жидкостью, газом или собственным паром. Искривление поверхности ведёт к появлению в жидкости дополнительного капиллярного давления ∆Р, величина которого связана со средней кривизной r поверхности уравнением Лапласа. Искривление поверхности жидкости у краев сосуда особенно отчетливо видно в капиллярах, где искривляется вся свободная поверхность жидкости. У смачивающей жидкости образуется вогнутый мениск (рис. 151, а), а у несмачивающей — выпуклый (рис. 151, б). Так как площадь поверхности мениска больше, чем площадь поперечного сечения трубки, то под действием молекулярных сил искривленная поверхность жидкости стремится выпрямиться.
Рис. 151 Силы поверхностного натяжения создают дополнительное (лапласово) давление под искривленной поверхностью жидкости. Если поместить капилляр одним концом в жидкость, налитую в широкий сосуд, то вследствие наличия силы лапласова давления жидкость в капилляре поднимается (если жидкость смачивающая) или опускается (если жидкость несмачивающая) (рис.152, а, б), так как под плоской поверхностью жидкости в широком сосуде избыточного давления нет.
|
|||||||||
|
Рис. 152.
На
рис. 153 изображена капиллярная трубка
некоторого радиуса r,
опущенная нижним концом в смачивающую
жидкость плотности ρ.
Верхний конец капилляра открыт. Подъем
жидкости в капилляре продолжается до
тех пор, пока сила тяжести
т,
действующая на столб жидкости в капилляре,
не станет равной по модулю результирующей
н
сил поверхностного натяжения, действующих
вдоль границы соприкосновения жидкости
с поверхностью капилляра: Fт = Fн,
где Fт = mg = ρhπr2g,
Fн = σ2πr cos θ.
Отсюда
следует: h
=
 .
.
|
|
Рис. 153.. Подъем смачивающей жидкости в капилляре. |
При полном смачивании θ = 0, cos θ = 1. В этом случае: h = .
|
При полном несмачивании θ = 180°, cos θ = –1 и, следовательно, h < 0. Уровень несмачивающей жидкости в капилляре опускается ниже уровня жидкости в сосуде, в которую опущен капилляр.
Вода практически полностью смачивает чистую поверхность стекла. Наоборот, ртуть полностью не смачивает стеклянную поверхность. Поэтому уровень ртути в стеклянном капилляре опускается ниже уровня в сосуде.
Благодаря капиллярности возможны жизнедеятельность животных и растений, различные химические процессы, бытовые явления, однако важно отметить, что в биологических объектах капиллярный механизм перемещения жидкости не является единственным (важную роль играет осмос52).
Так, влагообмен в почве осуществляется за счёт поднятия воды по капиллярам. Поэтому перепахивание почвы, разрушающее эти капилляры, способствует сохранению в ней влаги. Примерами капиллярных явлений являются процессы поднятия жидкостей по фитилям, впитывание влаги гигроскопическими телами и др. Защита металлических поверхностей от коррозии с помощью масляных плёнок основана на несмачивании водой жирных поверхностей. Непромокаемую одежду изготовляют из тканей, котрые не смачиваются водой. Наоборот, при крашении важно, чтобы поверхность тела хорошо смачивалась красителем.

 ,
,
 ,
с точки зрения силовой:
коэффициентом
поверхностного натяжения называется
величина,
численно
равная силе поверхностного натяжения,
приходящейся
на единицу длины поверхности раздела
сред:
=
,
с точки зрения силовой:
коэффициентом
поверхностного натяжения называется
величина,
численно
равная силе поверхностного натяжения,
приходящейся
на единицу длины поверхности раздела
сред:
=
 ,
,
 .
.
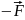 н.
н. Δx
= σ2LΔx
σ =
Δx
= σ2LΔx
σ =
 .
.

 =
=
 .
.
 .
. +
+ ).
(1)
).
(1)
 .
. +
).
(3)
+
).
(3)
 0,073 Н/м,.
Следовательно, для R
получается
следующее значение: R
=
0,073 Н/м,.
Следовательно, для R
получается
следующее значение: R
=
 =
=
 1,5•10-6м
= 1,5
мкм.
1,5•10-6м
= 1,5
мкм.
 ;
13
=
;
13
=
 ;
23
=
;
23
=
 ,
а
величины
,
а
величины
 ,
,
 и
и
 -
равны поверхностному натяжению на
границах раздела газ-жидкость,
газ-твердое тело и жидкость-твердое
тело.
-
равны поверхностному натяжению на
границах раздела газ-жидкость,
газ-твердое тело и жидкость-твердое
тело. +
= 0,
(1)
+
= 0,
(1) .
(2)
.
(2)
 1,
то из формулы (2)
следует условие существования
устойчивого равновесия жидкости на
поверхности твердого тела: |
|
1.
1,
то из формулы (2)
следует условие существования
устойчивого равновесия жидкости на
поверхности твердого тела: |
|
1.
 ,
то имеет место частичное
смачивание,
а при
<
- частичное
несмачивание.
,
то имеет место частичное
смачивание,
а при
<
- частичное
несмачивание.

 Таким
образом, реальной ситуации при
взаимодействии жидкости с твердым
телом реализуются, как правило, две
возможности – либо частичное смачивание
(0<
),
либо частичное несмачивание (
<
Таким
образом, реальной ситуации при
взаимодействии жидкости с твердым
телом реализуются, как правило, две
возможности – либо частичное смачивание
(0<
),
либо частичное несмачивание (
<



