- •1.Белоктың бірінші реттік құрылымы.. Пептидтік байланыс.
- •2. Белоктың екіншіі реттік құрылымы. Сутектік байланыс.
- •3. Белоктың үшінші реттік құрылымы: фолдинг, табиғи конформация, домен, белсенді орталық, лиганда. Үшінші реттік құрылымды түзетін байланыстар.
- •4. Белоктардың төртінші реттік құрылымы. Белоктардың төртінші реттік құрылымына мысалдар.
- •5. Белоктардың физика-химиялық қасиеттері: жоғары молекулалық масса; амфотерлігі, белоктардың гидратациясы (ерігіштігі); белоктардың ионизациясы.
- •8.Белок денатурациясының анықтамасы. Денатурация стадиялары. Денатурациялаушы агенттер және олардың әсер ету ерекшеліктері.
- •9. Ферменттердің анықтамасы және ферменттердің жалпы қасиеттері
- •10. Ферментативтік катализ ерекшеліктері мен әсер ету механизмінің жалпы сипаттамасы. Ферментативтік катализ сатылары
- •11. Ферменттер белсенділігінің өлшем бірліктері. Юнит және Катал.
- •12. Ферменттердің құрылымдық ұйымдасуы – белсенді орталық, аллостерлік орталық, эффекторлар жайындағы түсінік (активаторлар, ингибиторлар).
- •13. Жай (біркомпонентті) және күрделі (екі компонентті) ферменттер жайындағы түсінік.
- •14. Ферменттердің субстраттық талғамдылығы– абсолюттік, топтық және стереоталғамдылық. Ферменттердің каталиттік талғамдылығы.
- •15. Ферменттер белсенділігіне әсер ететін факторлар. Ферментативтік реакция жылдамдығының температураға, рН, ферменттер мен субстраттар концентрациясына тәуелділігі.
- •16. Ферменттердің жіктелуі және олардың аталуы. Ферменттер кластары: оксидоредуктазалар, трансферазалар, гидролазалар, изомеразалар, лиазалар, лигаза; олардың класс ішілік топтары.
- •17.Энзимология
- •18. «Дәрумендер» туралы түсінік.
- •19. Дәрумендердің ерігіштігі бойынша жіктелуі.
- •Липой қышқылы
- •20. Дәрумендердің қызметтері бойынша жіктелуі.
- •21. «Дәрумендердің жеткіліксіздігі» туралы түсінік - дәрумендермен субнормальдық қамтылу, гипо- и авитаминозды жағдай. Біріншілік және екіншілік авитаминоздар (мысалдар)
- •1.2. В2 витамині, (рибофлавин).
- •1.3. В5 витамині (рр, никотин қышқылы, ниацин, никотинамид)
- •1.4. В3 витамині (пантотен қышқылы)
- •1.5. В6 витамині (пиридоксин, пиридоксаль, пиридоксамин).
- •1.11. Р витамині (биофлавоноидтар және полифенолдар)
- •2. Майда еритін витаминдер
- •2.1. А витамині
- •2.3. К витамині (филлохинон)
- •2.4. Е витамині (токоферолдар)
- •2. Мырыш.
- •6.Магний.
- •7. Кобальт.
- •8. Молибден.
- •Катаболизмнің жалпы және арнайы жолдары.
- •Цитрат циклінің биологиялық маңызы.
- •Биологиялық тотығу.
- •Хемиосмостық қосарлану процесі.
- •Хемиосмостық процестің этаптарының жалпы сипаттамасы.
- •Митохондриялық электрон тасымалдаушы тізбек (мэтт).
- •Убихинон
- •Цитохром с
- •Тотығып фосфорлану
- •Тыныс алу мен фосфорланудың ажыратылуы
- •Тыныс алу бақылауы
- •Энергия алмасуының реттелуі.
- •Гипоэнергетикалық жағдай.
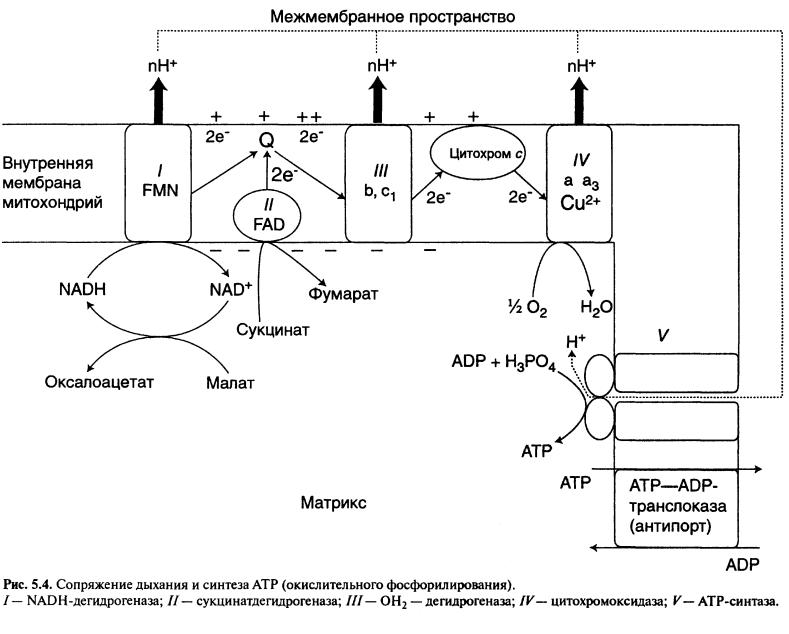
Тотығып фосфорлану
Тыныс алу тізбегіндегі электрондардың ағынынан бөлінген энергия АДФ -тің фосфорлануын қосарландырып жүргізу реакциясына пайдаланылады. Екі процессте бір біріне өте тәуелді, себебі биототығу АДФ болмағанда өтпейді. Тотығу мен фосфорлану қатынасы Р/О -фосфорланған АДФ-тің молінің 1/2 О2-ге моліне мөлшерін көрсетеді, сондықтан, ол тотығып фосфорлану коэффициенті деп аталады.
Электрон тасымалдаушы тізбек протондық насос тәріздес қызмет атқарады, протондарды матрикстен ішкі мембрана арқылы мембранааралық кеңістікке ауыстыруды атқарады.
|
Сур. 8.
Матриксте протондардың жиналуынан электрохимиялық потенциалдар айырмасы пайда болады. Ішкі мембрананың матрикс жағы протондармен оң зарядталған, ал сыртқы беті электрон тасымалдайтындықтан теріс зарядталған. Бұл электрохимиялық потенциал протондарды кері қарай жылжуын туындатады, бірақ протондар мембрананың тек арнайы бөлігі-протондық канал арқылы ғана өте алады. Протондардың кері өтуінде бөлінетін энергия АДФ фосфорлануына жұмсалады және экзоэргиялық процесс деп аталады. Бұл реакцияны Н+-АТФ-синтетаза катализдейді. Ол ішкі мембрананың ішкі бетінде протондық каналда орналасқан. Мембранааралық кеңістікке АДФ-тің жеткізілуін және АТФ-тің цитоплазмаға шығарылуын АТФ-АДФ-транслоказа антипорттық тасымалдану бойынша атқарады.
|
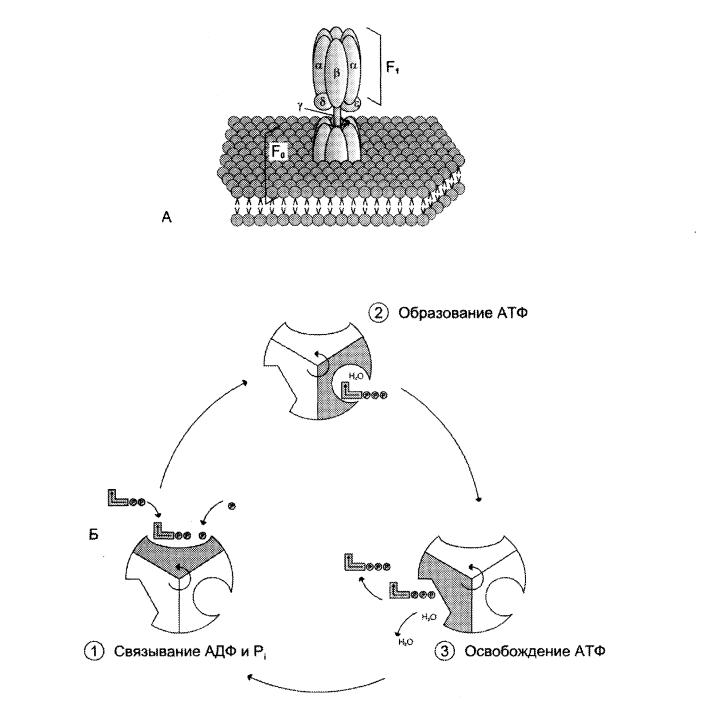
АТФ-синтезаның құрылысы күрделі, 2 компоненттен Ғо және Ғ1 тұрады. Липидтік биқабатқа батырылған Ғо -протон тасымалдаушы каналды құрайды, ал Ғ1 -АТФ синтезін жүргізеді. |
АТФ молекуласының синтезі АТФ-синтеза арқылы минимум 2 протонның оттегінің тотықтыруы үшін өтуі керек ететіндіктен, НАДН+-Н+ тотыққанда 2е- оттегіге түсетіндіктен бір оттегі молекуласына 6 Н+ өтеді. Сондықтан, бұл процесстегі АТФ-тің максимальді мөлшері 3-молекулаға тең. ФАД арқылы тотыққанда 2 АТФ молекуласы түзіледі.
|
Митохондриядағы тотығу тізбегінде протондардың матрикстен мембранааралық кеңістікке өтуі 3 бөлікте (ІІ, ІІІ, IV-комплекстерде) жүреді. Сәйкес түрде 3 реакция мн+ (электрохимиялық потенциал) түзілуін жүргізеді. Протон тасымалдануы туралы гипотез ұсынылған. Ол активті тасымалдану арқылы атқарылады деп қабылданған. Энергия оған тотығу-тотықсыздану циклдерінің кезектесулерінен түседі деп есептелінеді. Бұл гипотезаға сәйкес, тотықсызданғанда ауыстырушы комплекстің конформациялық өзгерісі өтеді. Ол протон байланыстырушы бөлікті активтендіреді, ішкі мембрананың матрикс жағында орналасқан. Конформацияның өзгерісінде байланыстырушы бөлік мембрананың келесі бөлігіне өтіп кетеді және сол мезгілде оның протонды байланыстырушы қабілеті төмендейді, нәтижесінде, протон мембранааралық кеңістікке босатылады. |
|
Протондардың жиналып қалуы мембрананың екі жағында Н+ концентрациясының әртүрлі -сыртқы бетінде жоғары, ал ішкі бетінде аз-болуына әкеледі. Н+ концентрациясының градиентінен мембрана электрленген қалыпта болады - сыртқы беті оң зарядталған. |