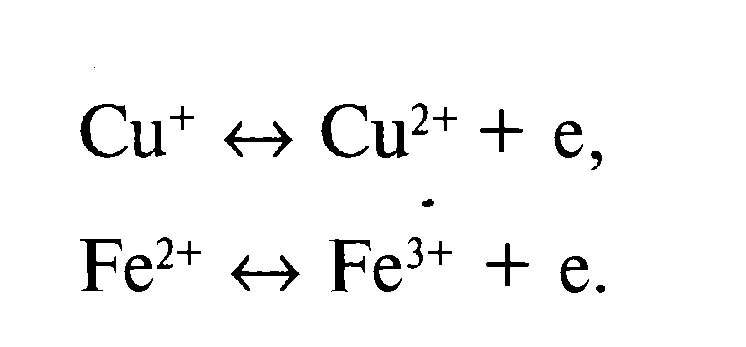- •1.Белоктың бірінші реттік құрылымы.. Пептидтік байланыс.
- •2. Белоктың екіншіі реттік құрылымы. Сутектік байланыс.
- •3. Белоктың үшінші реттік құрылымы: фолдинг, табиғи конформация, домен, белсенді орталық, лиганда. Үшінші реттік құрылымды түзетін байланыстар.
- •4. Белоктардың төртінші реттік құрылымы. Белоктардың төртінші реттік құрылымына мысалдар.
- •5. Белоктардың физика-химиялық қасиеттері: жоғары молекулалық масса; амфотерлігі, белоктардың гидратациясы (ерігіштігі); белоктардың ионизациясы.
- •8.Белок денатурациясының анықтамасы. Денатурация стадиялары. Денатурациялаушы агенттер және олардың әсер ету ерекшеліктері.
- •9. Ферменттердің анықтамасы және ферменттердің жалпы қасиеттері
- •10. Ферментативтік катализ ерекшеліктері мен әсер ету механизмінің жалпы сипаттамасы. Ферментативтік катализ сатылары
- •11. Ферменттер белсенділігінің өлшем бірліктері. Юнит және Катал.
- •12. Ферменттердің құрылымдық ұйымдасуы – белсенді орталық, аллостерлік орталық, эффекторлар жайындағы түсінік (активаторлар, ингибиторлар).
- •13. Жай (біркомпонентті) және күрделі (екі компонентті) ферменттер жайындағы түсінік.
- •14. Ферменттердің субстраттық талғамдылығы– абсолюттік, топтық және стереоталғамдылық. Ферменттердің каталиттік талғамдылығы.
- •15. Ферменттер белсенділігіне әсер ететін факторлар. Ферментативтік реакция жылдамдығының температураға, рН, ферменттер мен субстраттар концентрациясына тәуелділігі.
- •16. Ферменттердің жіктелуі және олардың аталуы. Ферменттер кластары: оксидоредуктазалар, трансферазалар, гидролазалар, изомеразалар, лиазалар, лигаза; олардың класс ішілік топтары.
- •17.Энзимология
- •18. «Дәрумендер» туралы түсінік.
- •19. Дәрумендердің ерігіштігі бойынша жіктелуі.
- •Липой қышқылы
- •20. Дәрумендердің қызметтері бойынша жіктелуі.
- •21. «Дәрумендердің жеткіліксіздігі» туралы түсінік - дәрумендермен субнормальдық қамтылу, гипо- и авитаминозды жағдай. Біріншілік және екіншілік авитаминоздар (мысалдар)
- •1.2. В2 витамині, (рибофлавин).
- •1.3. В5 витамині (рр, никотин қышқылы, ниацин, никотинамид)
- •1.4. В3 витамині (пантотен қышқылы)
- •1.5. В6 витамині (пиридоксин, пиридоксаль, пиридоксамин).
- •1.11. Р витамині (биофлавоноидтар және полифенолдар)
- •2. Майда еритін витаминдер
- •2.1. А витамині
- •2.3. К витамині (филлохинон)
- •2.4. Е витамині (токоферолдар)
- •2. Мырыш.
- •6.Магний.
- •7. Кобальт.
- •8. Молибден.
- •Катаболизмнің жалпы және арнайы жолдары.
- •Цитрат циклінің биологиялық маңызы.
- •Биологиялық тотығу.
- •Хемиосмостық қосарлану процесі.
- •Хемиосмостық процестің этаптарының жалпы сипаттамасы.
- •Митохондриялық электрон тасымалдаушы тізбек (мэтт).
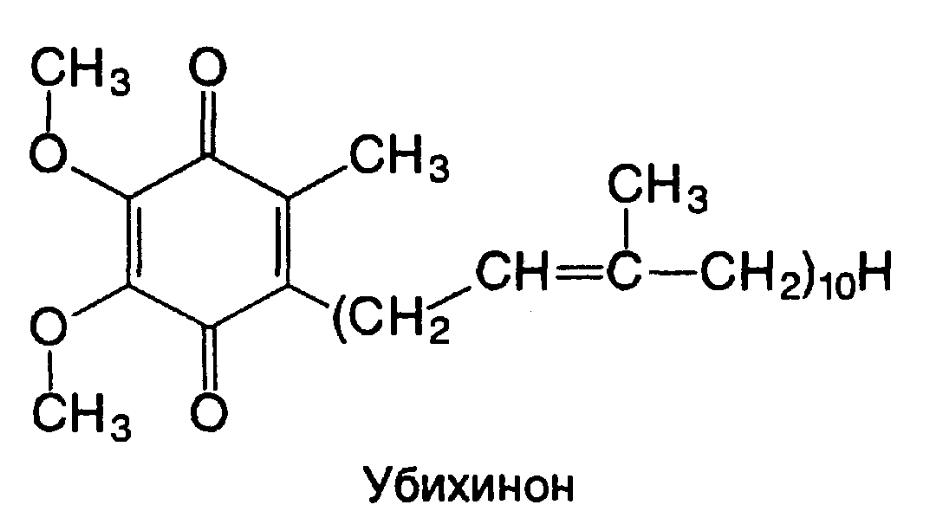
- •Убихинон
- •Цитохром с
- •Тотығып фосфорлану
- •Тыныс алу мен фосфорланудың ажыратылуы
- •Тыныс алу бақылауы
- •Энергия алмасуының реттелуі.
- •Гипоэнергетикалық жағдай.
Убихинон
|
Кофермент Q-белоксыз компонент изопреннің туындысы. Убихинон атауы оның табиғатта кең таралғандығымен байланысты. Негізгі қызметі е- -ды цитохромға, ал Н+ мембранааралық кеңістікке жеткізу.
|
ІІІ-комплекс
Пропильді
топ
Метильді
топ
Винилді
топ
|
ІІІ-комплекс-QН2 -дегидрогеназа цх в және цх С1-ден тұрады. Бұл комплекс құрамына ҒеS-белоктарда кіреді. Бұл фермент тотықсызданған кофермент Q-ді тотықтырып электронды цх С-ға тасымалдайды. Цитохромдар - бұл гемпротеинді белоктар электрондар цх в-дан цх С1, сонан кейін цх С-ға темір ионының тотықсыздануы және қайтадан тотығуы арқылы беріледі. Ғе3+ + е- Ғе2+ Негізгі қызметі электронды цх С-ға тасымалдау. Н+ -мембранааралық кеңістікке ауысуын жүзеге асырады. |
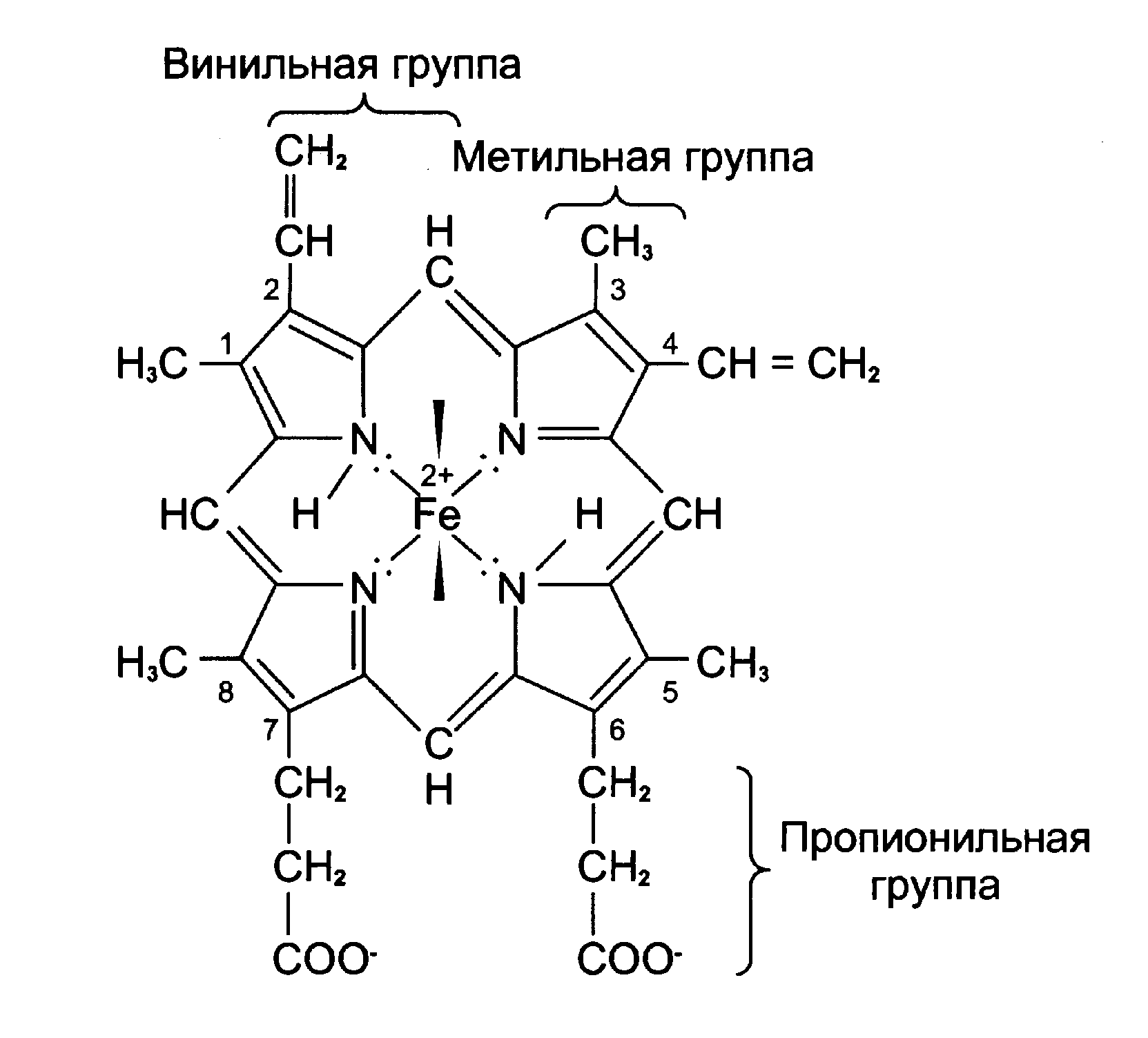
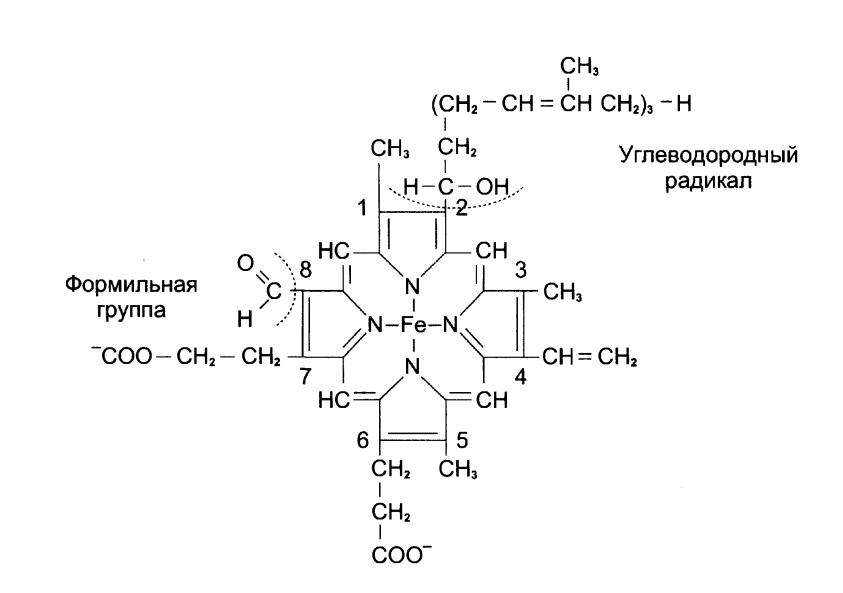
Цитохром с
Цитохром С - кіші молекулалы гем құрамды белок, мембрананың липидтік қабатында қозғалуға қабілетті.
IV-комплекс
|
IV-комплекс-цитохромоксидазалар цх а, цх а3. Олардың орталық иондары Си2+.
Негізгі қызметі - электрондарды цх С-дан О2 -ге дейін жеткізу және Н+ -тің мембранааралық кеңістікте ауысуын қамтамасыз ету. |
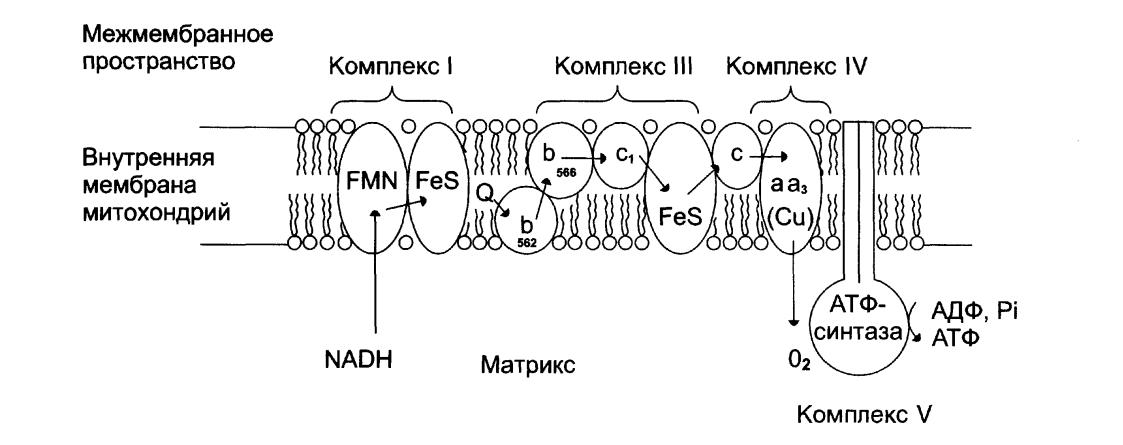
Тыныс алу тізбегіндегі аралық тасымалдаушылардың протондар мен электрондарды тасымалдауының кезектескен реакцияларының реті 7 - сур.
|
Сур. 7. Тыныс алу тізбегіндегі комплекстердің реті.
Процесс протондар мен электрондарды тотығушы субстраттан НАД+ немесе ФАД коферменттеріне ауыстырудан басталады. Бұл бірінші стадияны катализдеуші дегидрогеназаның НАД+ -тәуелді немесе ФАД -тәуелді болуымен айқындалады. НАД+ -тәуелді жағдайда протон доноры ретінде иозцитрат, -кетоглутарат, малат, пируват, глутамат қатысады. ФАД -тәуелді жағдайда протонның доноры -сукцинат, ацил-КоА, -глицерофосфат болады. Егер процесс НАД+ арқылы басталса, онда келесі протон ауыстырушы ФМН болады. ФМН-дан протон мен электрон кофермент Q-ға ауысады. ФАД-тәуелді дегидрогеназадан протон мен электрон бірден убихинонға, бірінші комплексті айналып өткендей, беріледі. Убихиноннан ары қарай протон мен электрондар жолы екіге бөлінеді. Кофермент Q (убихинон) электрондарды ары қарай цитохромдарға ауыстырады.
Тыныс алу тізбегінде цитохромдар тек электрондардың тасымалдаушылары болып табылады және тотығу -тотықсыздану потенциалдарының дәрежесіне сәйкес келесі кезекпен орналасады: цх в, цх С1, цх С, цх а, цх а3. Цитохромның геміндегі темір иондары валенттілігін электрондарды қосу және беру кездерінде өзгерте алады.
Цх а және а3 -цитохромоксидазалар деп аталады. Олардың мыс ионы электрондарды молекулалық оттегіге беруге қабілетті.
1е
Си2+ Си+
Электондардың оттегіге мыс ионынан берілуі фермент молекуласында өтеді. Оттегінің әрбір атомы екі электроннан қосып алады және екі протонды қосып су түзеді.