- •1.Белоктың бірінші реттік құрылымы.. Пептидтік байланыс.
- •2. Белоктың екіншіі реттік құрылымы. Сутектік байланыс.
- •3. Белоктың үшінші реттік құрылымы: фолдинг, табиғи конформация, домен, белсенді орталық, лиганда. Үшінші реттік құрылымды түзетін байланыстар.
- •4. Белоктардың төртінші реттік құрылымы. Белоктардың төртінші реттік құрылымына мысалдар.
- •5. Белоктардың физика-химиялық қасиеттері: жоғары молекулалық масса; амфотерлігі, белоктардың гидратациясы (ерігіштігі); белоктардың ионизациясы.
- •8.Белок денатурациясының анықтамасы. Денатурация стадиялары. Денатурациялаушы агенттер және олардың әсер ету ерекшеліктері.
- •9. Ферменттердің анықтамасы және ферменттердің жалпы қасиеттері
- •10. Ферментативтік катализ ерекшеліктері мен әсер ету механизмінің жалпы сипаттамасы. Ферментативтік катализ сатылары
- •11. Ферменттер белсенділігінің өлшем бірліктері. Юнит және Катал.
- •12. Ферменттердің құрылымдық ұйымдасуы – белсенді орталық, аллостерлік орталық, эффекторлар жайындағы түсінік (активаторлар, ингибиторлар).
- •13. Жай (біркомпонентті) және күрделі (екі компонентті) ферменттер жайындағы түсінік.
- •14. Ферменттердің субстраттық талғамдылығы– абсолюттік, топтық және стереоталғамдылық. Ферменттердің каталиттік талғамдылығы.
- •15. Ферменттер белсенділігіне әсер ететін факторлар. Ферментативтік реакция жылдамдығының температураға, рН, ферменттер мен субстраттар концентрациясына тәуелділігі.
- •16. Ферменттердің жіктелуі және олардың аталуы. Ферменттер кластары: оксидоредуктазалар, трансферазалар, гидролазалар, изомеразалар, лиазалар, лигаза; олардың класс ішілік топтары.
- •17.Энзимология
- •18. «Дәрумендер» туралы түсінік.
- •19. Дәрумендердің ерігіштігі бойынша жіктелуі.
- •Липой қышқылы
- •20. Дәрумендердің қызметтері бойынша жіктелуі.
- •21. «Дәрумендердің жеткіліксіздігі» туралы түсінік - дәрумендермен субнормальдық қамтылу, гипо- и авитаминозды жағдай. Біріншілік және екіншілік авитаминоздар (мысалдар)
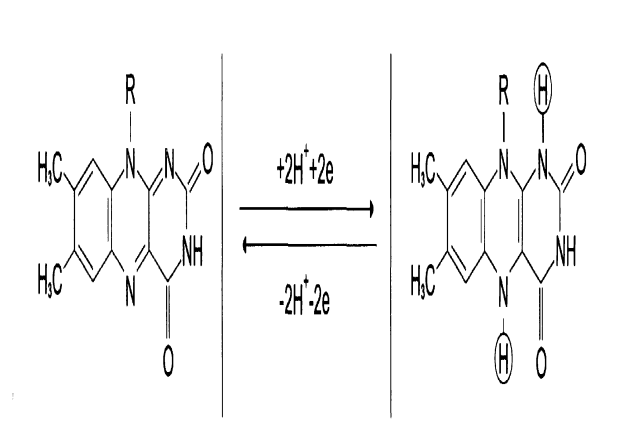
- •1.2. В2 витамині, (рибофлавин).
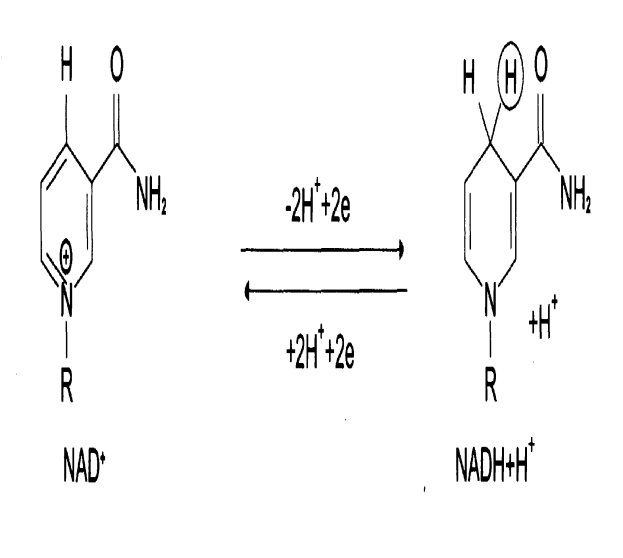
- •1.3. В5 витамині (рр, никотин қышқылы, ниацин, никотинамид)
- •1.4. В3 витамині (пантотен қышқылы)
- •1.5. В6 витамині (пиридоксин, пиридоксаль, пиридоксамин).
- •1.11. Р витамині (биофлавоноидтар және полифенолдар)
- •2. Майда еритін витаминдер
- •2.1. А витамині
- •2.3. К витамині (филлохинон)
- •2.4. Е витамині (токоферолдар)
- •2. Мырыш.
- •6.Магний.
- •7. Кобальт.
- •8. Молибден.
- •Катаболизмнің жалпы және арнайы жолдары.
- •Цитрат циклінің биологиялық маңызы.
- •Биологиялық тотығу.
- •Хемиосмостық қосарлану процесі.
- •Хемиосмостық процестің этаптарының жалпы сипаттамасы.
- •Митохондриялық электрон тасымалдаушы тізбек (мэтт).
- •Убихинон
- •Цитохром с
- •Тотығып фосфорлану
- •Тыныс алу мен фосфорланудың ажыратылуы
- •Тыныс алу бақылауы
- •Энергия алмасуының реттелуі.
- •Гипоэнергетикалық жағдай.
Хемиосмостық процестің этаптарының жалпы сипаттамасы.
Хемиосмостық процесс метаболиттердің тотығуы энергиясын АТФ түзілуімен қосарландырады, ол митохондрияның ішкі мембранасында өтеді. Пируваттың лимон қышқылының циклінде тотығуы нәтижесінде түзілген энергия НАД+-пен ФАД-тардан НАДН-тан және ФАДН2 түзілуіне әкеледі немесе жоғары энергиялы электрондар мен тотықсыздандырушы эквиваленттер түрінде жинақталады.
Бұл электрондар оттегімен байланысып Н2О түзілуіне және тотығып фосфорлану процесінде АТФ өндірілу үшін жұмсалады.
НАДН+-Н және ФАДН2 формасында резервтелген электрондар босатылады және митохондрияның ішкі мембранасында орналасқан тыныс алу тізбегі бойынша тасымалданады.
Электрондар бір комплекстен келесі комплекске өткен кезде бөлінген энергия Н+ -ті матрикстен ішкі мембрана арқылы мембранааралық кеңістікке сорып шығарады.
Бұл процесс митохондрияның ішкі мембранасында электрохимиялық протондық градиентті қалыптастырады. Сондықтан, мембранааралық кеңістікте протондар концентрациясы жоғары болғандықтан, олар протондық градиент бойынша кері матрикске ағылады (бір жағынан матрикстен теріс зарядтың да бағыттауымен). Бұл мембрана байланысқан АТФ-синтазаны (протондық каналдағы) қызметке әкеледі, нәтижесінде АДФ пен Н3РО4 –тен АТФ түзілуі өтеді.
Митохондриялық электрон тасымалдаушы тізбек (мэтт).
Алғашқы донор SH2 –ден электрондардың терминалдық акцептор О2-ге тасымалдану процесіне аралық жеткізушілер қатысады. Толық процесс тотығу-тотықсыздану реакцияларының тізбегін құрайды. Оның өту барысында аралық жеткізушілердің өзара әсерлесуі өтеді. Әрбір аралық жеткізушілер алғашқыда электрондар мен протондардың акцепторлары ролін атқарады. Электронды келесі жеткізушіге бергеннен кейін тотыққан қалыптан тотықсызданған формаға өтеді. Сонан кейін, ол электрондарды келесі жеткізушіге жеткізіп қайтадан тотыққан қалыпқа келеді. Соңғы стадияда жеткізуші электрондарды оттегіге береді, ал ол суға дейін тотықсызданады.
Тотығу-тотықсыздану реакцияларының кезектескен ретінің жиыны электрон тасымалдаушы тізбек немесе тыныс алу тізбегі деп аталады.
Жоғары сатыдағы ағзалардың тыныс алу тізбегіндегі аралық тасымалдаушылар ретінде келесі коферменттер болады: НАД+ (никотинамидадениндинуклеотид), ФАД және ФМН (флавинадениндинуклеотид және флавинмононуклеотид), кофермент Q (KoQ), гемқұрамды белоктар жиыны-цитохромдар (цх в, с1, с, а, а3) және гемсіз темірқұрамды белоктар (FeS, Fe2S2). Бұл тізбектегі барлық қатынасушылар төрт тотығу-тотықсызданушы жүйелерге немесе комплекске бөлінеді.
І-комплекс
|
І комплекс-НАДН+-дегидрогеназа, ФМН, FeS-белоктар. НАДН+-тәуелді дегидрогеназа субстраттың тікелей тотығуы реакциясын катализдейді. НАД+-кофермент және сутектің акцепторы қызметін атқарады. Сутек тасымалдаушысына ФМН-коферменті ол ферментке қосылған сутегінің қосып электрон мен Н+ ҒeS-белок арқылы убихинонға береді. І-комплекстің негізгі қызметі-бұл НАДН+-тан электрон мен Н+ -ті убихинонға жеткізу. Сол арқылы Н+ -тің мембранааралық кеңістікке ауысуын атқару. |
ІІ-комплекс
|
ІІ-комплекс ФАД-тәуелді сукцинатдегидрогеназа және ҒеS-белоктар. Бұл фермент Н+ мен е- -ның бірінші ретті қабылдаушылары болып табылады. Коферменті ФАД ол субстраттан сутегіні қосып алатын акцептор болып табылады. ФАД пен ФМН ферментке простетикалық топ ретінде мықты байланысады. ФМН ферменттің белоктық бөлігімен мықты байланысқан негізгі қызметі сукцинаттың тотығуынан түзілген е- ды және Н+ -ті убихинонға тасымалдайды. |