- •II. Составление уравнения реакции с помощью ионно-электронных уравнений.
- •Блок-схема составления ионно-электронных уравнений
- •Важнейшие окислители и продукты их восстановления
- •Важнейшие восстановители и продукты их окисления
- •Стандартные потенциалы металлов в водном растворе при 298 к.
- •Эквиваленты в овр.
Эквиваленты в овр.
Эквивалент – условная или реальная частица, которая в данной ОВР эквивалентна одному электрону. Фактор эквивалентности fэк – безразмерное число, обозначающее, какая доля формульной единицы вещества в данной ОВР эквивалентна одному электрону. Его конкретное значение зависит от стехиометрии реакции, например:
Уравнение полуреакции |
Факторы эквивалентности |
CH3CHO + H2O – 2 е− = CH3COOH + 2 H+
|
fэк(CH3CHO)
=
|
Cr O + 14 H+ + 6 е− = 2 Cr3+ + 7 H2O |
fэк(K2Cr2O7)
=
|
2 CO2 + 2 H+ + 2 e– = Н2С2O4 |
fэк(CO2)
=
1;
fэк(Н2С2O4)
=
|
1. Какую навеску вещества В надо взять, чтобы на титрование ее было затрачено V мл сэк н. раствора титранта?
Решение.

где nэк – количество вещества эквивалентов В, г; сэк – молярная концентрация эквивалентов титранта, моль/л; V – объем раствора титранта, мл; 1000 мл/л – пересчетный коэффициент.
 ,
,
где
m
– искомая физическая масса В,
г; M
– молярная
масса В,
г/моль; –
фактор
эквивалентности В.
–
фактор
эквивалентности В.
2. Сколько г вещества В надо взять, чтобы приготовить V л сэк н. раствора его для титрования в кислой среде?
Решение.

где nэк – количество вещества эквивалентов В, г; сэк – молярная концентрация эквивалентов В, моль/л; V – объем раствора V , л.
,
где m – искомая физическая масса В, г; M – молярная масса вещества В, г/моль; – фактор эквивалентности В.
3. Сколько граммов x-гидрата вещества В следует взять для приготовления V мл сэк н. раствора.
Решение.
где nэк – количество вещества эквивалентов В, г; сэк – молярная концентрация эквивалентов В, моль/л; V – объем раствора В, мл; 1000 мл/л – пересчетный коэффициент.
 ,
,
где m – искомая физическая масса x-гидрата В, г; M – молярная масса В, г/моль; M(H2O) – молярная масса воды, г/моль; x – число молекул воды в формульной единице кристаллогидрата; – фактор эквивалентности В.
4. Сколько граммов x-гидрата вещества В следует взять для приготовления V мл раствора с титром по веществу В1 T(В/В1) г/мл?
Решение.
m1 = T(В/В1)V,
где m1 – физическая масса В1, г; T(В/В1) – титр раствора В по В1, г/мл; V – объем раствора В, мл.
 ,
,
где
nэк
– количество
вещества
эквивалентов
В, моль;
M1
– молярная масса
В1,
г/моль;
 –
фактор эквивалентности В1.
–
фактор эквивалентности В1.
,
где m – искомая физическая масса x-гидрата В, г; M – молярная масса В, г/моль; M (H2O) – молярная масса воды, г/моль; x – число молекул воды в формульной единице кристаллогидрата; – фактор эквивалентности В.
5. m г x-гидрата вещества В растворили в мерной колбе на V мл. На титрование V1 мл этого раствора расходуется V2 мл раствора титранта. Найти молярную концентрацию эквивалентов раствора титранта.
Решение.

где nэк – количество вещества эквивалентов титранта, моль; m – физическая масса x-гидрата В, г; M – молярная масса В1, г/моль; x – число молекул воды в формульной единице кристаллогидрата; – фактор эквивалентности В;

где сэк,1 – молярная концентрация эквивалентов В, моль/л; 1000 мл/л – пересчетный коэффициент; V – объем исходного раствора В, мл.
 ,
,
где сэк,2 – искомая молярная концентрация эквивалентов титранта, моль/л; V1 – объем оттитрованного исходного раствора x-гидрата В, мл; V2 – объем раствора титранта, пошедший на титрование, мл.
6. Вычислить молярную концентрацию эквивалентов титранта, если на титрование m г вещества В израсходовано V мл этого раствора.
Решение.
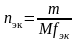 ,
,
где nэк – количество вещества эквивалентов титранта, моль; M – молярная масса В, г/моль; fэк – фактор эквивалентности В.
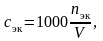 ,
,
где сэк – искомая молярная концентрация эквивалентов титранта, моль/л; 1000 мл/л – пересчетный коэффициент; V – объем раствора титранта, мл.
7. К кислому раствору вещества В прибавили V1 мл сэк,1 н. раствора первого титранта, и выделившееся вещество оттитровали V2 мл раствора второго титранта. Найти молярную концентрацию эквивалентов второго титранта.
Решение.
,
где cэк,2 – искомая молярная концентрация эквивалентов второго титранта, моль/л; cэк,1 – молярная концентрация эквивалентов первого титранта, моль/л; V1 – объем раствора первого титранта, мл; V2 – объем раствора второго титранта, мл.
8. К раствору вещества В добавили избыток раствора первого титранта, и выделившееся вещество оттитровали V мл сэк н. раствора второго титранта. Сколько граммов вещества В содержалось в растворе?
Решение.
 ,
,
где nэк – количество вещества эквивалентов В, моль; сэк – молярная концентрация эквивалентов второго титранта, моль/л; V – объем раствора второго титранта, мл; 1000 мл/л – пересчетный коэффициент.
,
где m – искомая физическая масса В, г; M – молярная масса В, г/моль; fэк – фактор эквивалентности В.
9. Из сплава, содержащего элемент Э, последний рядом операций осадили в виде осадка В. Действием на этот осадок кислоты и вещества В1 было выделено вещество В2, на титрование которого пошло V мл с М раствора титранта. Найти массу элемента Э в навеске сплава.
Решение.
 ,
,
где cэк – молярная концентрация эквивалентов титранта, моль/л; c – молярная концентрация титранта, моль/л; fэк – фактор эквивалентности титранта.
 ,
,
где n – количество вещества Э, моль; V – объем раствора титранта, мл; f(В) – фактор эквивалентности В; 1000 мл/л – пересчетный коэффициент

где m – искомая физическая масса Э, г; M – молярная масса Э, г/моль.
10. К V0 мл исходного раствора соли металла М прибавили V1 мл сэк,1 н. раствора осадителя, затем отделили образовавшийся осадок другой соли М. На титрование оставшегося в избытке раствора осадителя было израсходовано V2 мл сэк,2 н. раствора титранта. Сколько граммов М содержится в V мл исходного раствора?
Решение.
 ,
,
где nэк – количество вещества эквивалентов М в V0 мл исходного раствора, моль; сэк,1 – молярная концентрация эквивалентов осадителя, моль/л; V1 – объем раствора осадителя, мл; сэк,2 – молярная концентрация эквивалентов титранта, моль; V2 – объем раствора титранта, мл; 1000 мл/л – пересчетный коэффициент.

где
 – искомая физическая масса М в
V
мл исходного раствора,
г; M
– молярная масса
М, г/моль; fэк
– фактор
эквивалентности исходной соли М;
V0
– объем
исходного
раствора,
обработанный осадителем, мл.
– искомая физическая масса М в
V
мл исходного раствора,
г; M
– молярная масса
М, г/моль; fэк
– фактор
эквивалентности исходной соли М;
V0
– объем
исходного
раствора,
обработанный осадителем, мл.
11. Навеска m г руды, содержащей оксид элемента Э, обработана избытком смеси растворов веществ В и В1. Раствора В было взято V1 мл, и на титрование его избытка израсходовано V2 мл сэк н. раствора титранта. Найти массовую долю элемента Э в руде, если известно, что на титрование V3 мл такого же раствора вещества В расходуется V4 мл раствора такого же раствора титранта.
Решение.
 ,
,
где сэк(В) – молярная концентрация эквивалентов В, моль/л; V4 – объем раствора титранта, пошедший на титрование, мл; V3 – объем раствора В, мл.
 ,
,
где nэк – количество вещества эквивалентов оксида Э, моль; V1 – объем раствора В, взятый для обработки навески руды, мл; сэк – молярная концентрация эквивалентов титранта, моль/л; V2 – объем раствора титранта, пошедший на титрование избытка раствора В, мл; 1000 мл/л – пересчетный коэффициент.

где m(Э) – физическая масса Э в навеске руды, г; M – молярная масса Э, г/моль; fэк – фактор эквивалентности оксида Э.
 ,
,
где ω – искомая массовая доля Э в руде, %; m – физическая масса навески руды, г.
12. К V мл раствора вещества В (пл. = ρ г/мл) прибавлено V1 мл сэк,1 н. раствора первого титранта, избыток которого затем оттитровали V2 мл сэк,2 н. раствора второго титранта. Найти массовую долю В в растворе, если плотность этого раствора равна ρ г/мл.
Решение.
,
где nэк – количество вещества эквивалентов В в растворе, моль; сэк,1 – молярная концентрация эквивалентов первого титранта, моль/л; V1 – объем раствора первого титранта, мл; сэк,2 – молярная концентрация эквивалентов второго титранта, моль; V2 – объем раствора второго титранта, мл; 1000 мл/л – пересчетный коэффициент.

где m – физическая масса вещества В в растворе, г; M – молярная масса В, г/моль; fэк – фактор эквивалентности В;
 ,
,
где ω – искомая массовая доля вещества В в растворе, %; V – объем раствора В, мл; ρ – плотность раствора вещества В, г/мл.
13. К раствору, содержащему m0 г технического вещества В прилили V1 мл сэк,1 н. раствора первого титранта, избыток которого оттитровали V2 мл сэк,2 н. раствора второго титранта. Вычислите массовую долю (%) вещества В в образце.
Решение.
,
где nэк – количество вещества эквивалентов В в образце, моль; сэк,1 – молярная концентрация эквивалентов первого титранта, моль/л; V1 – объем раствора первого титранта, мл; сэк,2 – молярная концентрация эквивалентов второго титранта, моль; V2 – объем раствора второго титранта, мл; 1000 мл/л – пересчетный коэффициент.
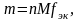
где m – физическая масса вещества В в образце, г; сэк,1 – молярная концентрация эквивалентов раствора первого титранта, моль/л; V1 – объем раствора первого титранта, мл; сэк,2 – молярная концентрация эквивалентов раствора второго титранта, моль; V2 – объем раствора второго титранта, см3; M – молярная масса вещества В, г/моль; fэк – фактор эквивалентности вещества В; 1000 мл/л – пересчетный коэффициент.
 ,
,
где ω – искомая массовая доля вещества В в образце, %; m0 – физическая масса образца, г.
14.
К смеси, содержащей избыток двух веществ,
добавили V1
мл раствора первого титранта. Выделившийся
заместитель оттитровали V2
мл с
М раствора второго титранта. Вычислить
титр первого титранта по веществу В.
Ионно-электронные уравнения полуреакций:
I2
+ 2 e–
=
2 I–;
2 SO3S2–
– 2 e–
=
 .
.
Решение.
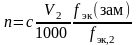 ,
,
где n – количество вещества первого титранта, моль; c – молярная концентрация второго титранта, моль/л; V – объем раствора второго титранта, мл; fэк(зам) – фактор эквивалентности заместителя; 1000 мл/л – пересчетный коэффициент; fэк,2 – фактор эквивалентности второго титранта.
 ,
,
где
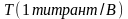 – искомый
титр раствора
первого титранта по В,
г/мл; M
– молярная
масса В, г/моль; fэк
(В) – фактор
эквивалентности В;
V1
– объем
раствора первого титранта,
мл; fэк,1
– фактор
эквивалентности первого
титранта.
– искомый
титр раствора
первого титранта по В,
г/мл; M
– молярная
масса В, г/моль; fэк
(В) – фактор
эквивалентности В;
V1
– объем
раствора первого титранта,
мл; fэк,1
– фактор
эквивалентности первого
титранта.
15. При сожжении m г вещества В элемент Э переведен в оксид, который поглотили раствором вещества А и сразу оттитровали V1 мл раствора первого титранта. Концентрация первого титранта установлена с помощью с2 М раствора второго титранта, причем V2/V1 = y. Найти массовую долю Э в В.
Решение.
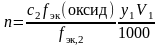 ,
,
где
n
– количество
вещества Э,
моль;
c2
– молярная
концентрация эквивалентов
второго
титранта,
моль/л;
y
– отношение
объемов
растворов
второго
и первого титрантов;
V1
– объем
раствора
первого
титранта,
мл;
 – фактор
эквивалентности
оксида
Э; 1000
мл/л – пересчетный коэффициент; fэк,2
– фактор
эквивалентности второго
титранта.
– фактор
эквивалентности
оксида
Э; 1000
мл/л – пересчетный коэффициент; fэк,2
– фактор
эквивалентности второго
титранта.
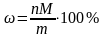 ,
,
где ω – искомая массовая доля Э в В, %; M – молярная масса Э, г/моль; m – физическая масса В, г.
16. m г раствора вещества В разбавили водой в мерной колбе на V мл. На титрование V1 мл этого раствора расходуется V2 мл сэк,2 н. раствора титранта. Какова массовая доля В в исходном растворе?
Решение.
 ,
,
где cэк(В) – молярная концентрация эквивалентов В, моль/л; cэк,2 – молярная концентрация эквивалентов титранта, моль/л; V2 – объем раствора титранта, мл; V1 – объем разбавленного исходного раствора, пошедший на титрование, мл.
 ,
,
где m(В) – физическая масса В в исходном растворе, г; V – объем разбавленного исходного раствора, мл; M – молярная масса В, г/моль; fэк – фактор эквивалентности В; 1000 мл/л – пересчетный коэффициент.
 ,
,
где ω – искомая массовая доля вещества В в исходном растворе, %; m – физическая масса исходного раствора, г.
17. К V мл раствора вещества В добавили V1 мл раствора первого титранта с титром T1 г/мл. Выпавший осадок отфильтровали, и избыток первого титранта в фильтрате оттитровали V2 мл раствора второго титранта с титром T2 г/мл. Определите титр исходного раствора.
Решение.
 ,
,
где сэк,1 – молярная концентрация эквивалентов первого титранта, моль/мл; T1 – титр раствора первого титранта, г/мл; fэк,1 – фактор эквивалентности первого титранта; M1 – молярная масса первого титранта, г/моль.
 ,
,
где сэк,2 – молярная концентрация эквивалентов второго титранта, моль/мл; T2 – титр раствора второго титранта, г/мл; fэк,2 – фактор эквивалентности второго титранта; M2 – молярная масса второго титранта, г/моль.
 ,
,
где n – количество вещества В, моль; V1 – объем раствора первого титранта, мл; V2 – объем раствора второго титранта, мл; fэк – фактор эквивалентности В.
 ,
,
где T – искомый титр исходного раствора, г/мл; M – молярная масса В, г/моль; V – объем исходного раствора, мл.
18. Из m г лекарственного препарата, содержащего вещество В, приготовили раствор и оттитровали его V мл раствора титранта с титром по В, равным Т(титрант/В) г/мл. Найти массу и массовую долю В в препарате.
Решение.
m(В) = Т(титрант/В)V,
где m – искомая физическая масса В, г; Т(титрант/В) – титр раствора титранта по В, г/мл; V – объем раствора титранта, мл.
,
где ω – искомая массовая доля В в препарате, %; m – физическая масса препарата, г.
19. На титрование V1 мл раствора вещества В израсходовали V2 мл сэк н. раствора титранта. Найти титр раствора В, если его фактор эквивалентности равен fэк.
Решение.
 ,
,
где cэк(В) – молярная концентрация эквивалентов В, моль/л; cэк – молярная концентрация эквивалентов титранта, моль/л; V2 – объем раствора титранта, мл; V1 – объем раствора В, мл.
 ,
,
где T – искомый титр раствора В, г/мл; fэк – фактор эквивалентности В; M – молярная масса В, г/моль; 1000 мл/л – пересчетный коэффициент.
20. Сколько мл c1 раствора вещества В потребуется для приготовления V2 мл раствора с молярной концентрацией эквивалентов, равной c2(fэкВ) моль/л?
Решение.
 ,
,
где cэк,1 – молярная концентрация эквивалентов В в исходном растворе, моль/л; c – молярная концентрация В в исходном растворе, моль/л; fэк – фактор эквивалентности В.
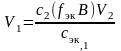 ,
,
где V1 – искомый объем исходного раствора В, мл; c2(fэкВ) – молярная концентрация эквивалентов В в приготовленном растворе, моль/л; V2 – объем приготовленного раствора В, мл.
21. На титрование V1 мл c1 М раствора вещества В пошло V2 мл раствора титранта. Найти молярную концентрацию эквивалентов титранта.
Решение.
 ,
,
где cэк – искомая молярная концентрация эквивалентов титранта, моль/л; c1 – молярная концентрация В, моль/л; V1 – объем раствора В, мл; fэк – фактор эквивалентности В; V2 – объем раствора титранта, мл.
22. V мл раствора вещества В эквивалентны m г вещества В1. Вычислить титр раствора В по В1.
Решение.
 ,
,
где T(В/В1) – искомый титр раствора В по В1, г/мл; m – физическая масса В, г; V – объем раствора В, мл.
23. m г оксида металла М растворили, затем весь металл(III) восстановили до катионов металла(II). На титрование последнего пошло V мл сэк н. раствора титранта. Определить формулу исходного оксида (MO, M3O4, или M2O3).
Решение.
 ,
,
где n1 – количество вещества М2+, моль; сэк – молярная концентрация эквивалентов титранта, моль/л; V – объем раствора титранта, мл; 1000 мл/л – пересчетный коэффициент.
 ,
,
где
m
–
физическая масса оксида М, г;
 ,
,
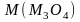 ,
,
 – молярные
массы соответствующих оксидов, г/моль.
– молярные
массы соответствующих оксидов, г/моль.
24. m г пробы, состоящей только из металла М и оксида металла(III), растворили, восстановили металл(III) до катионов металла(II), и оттитровали V мл сэк н. раствора титранта. Найти массовую долю металла в пробе.
Решение.
 ,
,
где n – количество вещества М, моль; сэк – молярная концентрация эквивалентов титранта, моль/л; V – объем раствора титранта, мл; 1000 мл/л – пересчетный коэффициент.
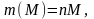
где m(М) – физическая масса М в пробе, г; M – молярная масса М, г/моль.
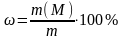 ,
,
где ω – искомая массовая доля М в пробе, %; m0 – физическая масса пробы, г.
25. К V мл раствора вещества В прибавили V1 мл сэк,1 н. раствора первого титранта, а избыток заместителя оттитровали V2 мл сэк,2 н. раствора второго титранта. Найти массово-объемную концентрацию В в исследуемом растворе.
Решение.
,
где n – количество вещества В, ммоль; сэк,1 – молярная концентрация эквивалентов первого титранта, моль/л; V1 – объем раствора первого титранта, мл; сэк,2 – молярная концентрация эквивалентов второго титранта, моль/л; V2 – объем раствора второго титранта, мл; fэк – фактор эквивалентности В.
 ,
,
где ρ – искомая массово-объемная концентрация В, г/л; M – молярная масса В, г/моль; V – объем раствора В, мл..
26. Из m г руды металл М перевели в раствор в виде катионов. При добавлении к этому раствору первого титранта выделился заместитель, на титрование которого пошло V2 мл раствора второго титранта с титром по М, равным Т(2 титрант/М) г/мл. Найти массовую долю М в руде.
Решение.
m(M) = V2Т(2 титрант/М),
где m(M) – физическая масса М, г; Т(2 титрант/М) – титр раствора второго титранта по М, г/мл.
,
где ω – искомая массовая доля М в руде, %; m0 – физическая масса руды, г.
27. m г технического вещества В растворили в мерной колбе на V мл. К V1 мл полученного раствора добавили первый титрант. Выделившийся заместитель оттитровали V2 мл сэк,2 н. раствора второго титранта. Найти массовую долю В в образце.
Решение.
 ,
,
где cэк,1 – молярная концентрация эквивалентов В, моль/л; cэк,2 – молярная концентрация эквивалентов второго титранта, моль/л; V2 – объем раствора второго титранта, мл; V1 – объем оттитрованного раствора В, мл.
 ,
,
где n – количество вещества В, моль; fэк – фактор эквивалентности В; V – объем раствора В, мл; 1000 мл/л – пересчетный коэффициент.
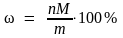 ,
,
где ω – искомая массовая доля В в образце, %; M – молярная масса М, г/моль; m – физическая масса образца, г.