
- •Содержание
- •IV.Молярная концентрация эквивалента 21
- •Вещество в растворе • • • •••• колба • • • • • объемом а) • • • 1 литр
- •Процентная концентрация (массовая доля вещества в растворе)
- •Задачи для самостоятельного решения
- •Молярная концентрация
- •Молярная концентрация эквивалента
- •IV. Молярная концентрация эквивалента. (с1/z).
- •V. Закон эквивалентов
- •Задачи для самостоятельного решения по всей теме
- •Приложение Расчет фактора эквивалентности по уравнению реакции через коэффициент стехиометричности
- •Литература
V. Закон эквивалентов
Вещества взаимодействуют между собой в эквивалентных количествах:
 ν1/z
(1)
= ν1/z
(2)
ν1/z
(1)
= ν1/z
(2)
т.к. ν = С·V тогда С1/я (1)·V1 = С1/я (2)·V2

или: С1/Z(1) V2
-------------- = ---------------
С1/Z(2) V1
26

Как следствие закона эквивалентов: концентрации реагирующих веществ обратно пропорциональны их объемам.
Задача 20: Определите молярную концентрацию эквивалента серной кислоты, 16 мл которой вступило в реакцию нейтрализации с 50 мл гидроксида натрия, молярная концентрация эквивалента которого 0,2 моль/л.

Дано: Решение
V ( NaOH) р-ра = 50 мл С1/Z(NaOH) V(H2SO4)
C
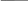 1/я
( NaOH)
р-ра = 0,2 моль/л =
1/я
( NaOH)
р-ра = 0,2 моль/л =
V ( H2SO4) р-ра = 16 мл С1/Z (H2SO4) V(NaOH)
 С1\Z(
H2SO4)
р-ра = ?
С1\Z(
H2SO4)
р-ра = ?
С1/Z(NaOH) · V(NaOH) 0,2 моль/л ·50 мл
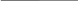
 С1/Z
(H2SO4)
= =
=
С1/Z
(H2SO4)
= =
=
V(H2SO4) 16 мл

= 0,625 моль/л
Задача 21: Сколько мл раствора гидроксида калия с концентрацией 0,2 моль/л потребуется для нейтрализации 20 мл раствора серной кислоты с концентрацией 0,1 моль/л.
Обратите внимание на то, что в задаче речь идет не о молярной концентрации эквивалента кислоты, а о простой молярной концентрации, а дается серная кислота, у которой основность = 2 и число Z = 2. Для гидроксида калия (КОН) безразлично, какая концентрация из молярных дана, т.к. кислотность его равна 1. Чтобы использовать закон эквивалентов в этом случае нам необходимо простую молярную концентрацию - С к-ты перевести в С1/z.
2. В задачах 20 и 21 не нужно размерность «мл» переводить в «л».
Дано: Решение
С (H2SO4) =0,1 моль/л С1/Z(КOH) V(H2SO4)
C ( КOH) р-ра = 0,4 моль/л =
V ( H2SO4) р-ра = 20 мл С1/Z (H2SO4) V(КOH)
V ( КOH) р-ра = ? С1/Z(КOH) = С(КOH) = 0,4 моль/л
С1/Z (H2SO4) = С1/Z (H2SO4) ·Z =0,1 моль/л.· 2= 0,2 моль/л
27
С1/Z (H2SO4) · V(H2SO4 ) 0,2 моль/л ·20 мл
V(КOH) = = =
С1/Z(КOH) 0,4 моль/л

= 10 мл
Если в задаче такого типа используется одноосновная кислота, например, азотная или соляная, то С1/z = С.
Титр.
Титр - это тоже выражение концентрации.
Титр – это масса растворенного вещества, содержащегося в 1 мл раствора.
m
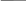 Т
= [г/мл] (формула 1)
Т
= [г/мл] (формула 1)
V
Размерность такая же, как у плотности.
Если указано, что титр кислоты HCl с молярной концентрацией эквивалента 0,1 моль/л равен 0,00365 г/мл, то это означает, что в 1 мл данного раствора содержится 0,00365 г HCl титр вычисляют до 4-х значащих цифр после нулей. Зная титр, можно вычислить массу вещества в любом объеме раствора:
m = Т·V
С1\Z ·M1/Z
 Титр
можно вычислять: Т = (формула 2)
Титр
можно вычислять: Т = (формула 2)
1000
Так как m = С·М·V, то, подставив это значение в формулу 1 получим:
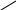 С
·M
·V
С
·M
·V
Т =
V
И далее, чтобы перевести «л» в «мл» необходимо дробь разделить на 1000.
Для записи значения титра сохраняются 4 значащих цифры.
Примеры записи:
28
Т = 1,24365 = 1,2437
Т = 1, 43632 = 1,4363
Т = 0, 012801 = 0,01280 (после всех нулей – 4 значащих цифры)
