
- •Қазақстан республикасы білім және ғылым министрлігі қ.И.Сәтбаев атындағы Қазақ ұлттық техникалық универститеті
- •Алифатты қатардағы қосылыстардың органикалық химиясы
- •Алматы 2010
- •Қ ұрастырушылар: Ермағанбетов м.Е.,Чугунова н.И., Керімқұлова а.Ж. Алматы: ҚазҰту, 2010.117
- •© Қ.И. Сәтбаев атындағы Қазақ ұлттық техникалық университеті
- •Пәннің оқу бағдарламасы – syllabus
- •Контакттық ақпарат
- •1.2 Пән бойынша мәліметтер:
- •1.5 Пәннің қысқаша мазмұны
- •Тапсырма түрлері, атаулары және оларды орындау кестесі
- •1.7 Әдебиеттер тізімі
- •1.8 Білімді тексеру және бағалау
- •Оқу процесінің күнтізбелік кестесі
- •Модульдар бойынша және аралық бақылауға арналған сұрақтар тізімі
- •Аралық бақылауға арналған сұрақтар тізімі
- •1.9 Курс саясаты мен процедурасы
- •2 Активті таратылып берілетін материалдардың мазмұны
- •Курстың тақырыптық жоспары
- •2.2 Дәріс сабақтарының конспектілері
- •1 Дәріс. Кіріспе.Органикалық қосылыстардың жіктелуі
- •2 Дәріс. Химиялық байланыс, құрылым, реакцияға бейімділік туралы ұғымдарға қазіргі көзқарас
- •3 Дәріс. Қаныққан көмірсутектер (алкандар)
- •Изомерлері. Бұл қатардың алғашқы үш мүшесінің (метан, этан, пропан) изомерлері болмайды, ал бутан үшін (с4н10) екі изомер болады:
- •4 Дәріс. Қанықпаған көмірсутектер. Этилендік көмірсутектер (алкендер)
- •Изомерлері. Этилендік көмірсутектердің гомологтық қатарының структуралық изомериясы қаныққан көмірсутектері сияқты төртінші мүшесінен басталады. Алайда, бұларға бірнеше изомер түрі тән.
- •4. Сульфолау реакциясы
- •5. Гидратация реакциясы
- •5 Дәріс. Диен көмірсутектері (алкадиендер)
- •6 Дәріс. Ацетилен қатарының қанықпаған көмірсутектері (алкиндер)
- •7 Дәріс. Көмірсутектердің галогентуындылары
- •8 Дәріс. Спирттер (гидрооксиқосылыстар). Біратомды спирттер
- •9 Дәріс. Көп атомды спирттер
- •Алу әдістері. Гликольдерді бір атомды спирттерге сәйкес немесе басқа әдістермен алуға болады.
- •10 Дәріс. Альдегидтер мен кетондар
- •Альдегидтердің аталуы. Рационалдық аталу бойынша альдегидтерді екі жолмен атауға болады.
- •Кетондар номенклатурасы. Рациональды номенклатура бойынша кетондарды, карбонил тобын қоршаған радикалдарды, орынбасарлардың өсу ретімен атап, соңынан “кетон” деген сөз жалғау арқылы атайды.
- •11 Дәріс. Карбон қышқылдары және олардың туындылары
- •Бір негізді карбон қышқылдары. Номенклатурасы.Олардың бастапқы мүшелеріне тривиалды аталу тән.
- •Химиялық қасиеттері Бұлардың химиялық қасиеттерін толығымен дерлік карбоксил тобы анықтайды. Карбон қышқылдарының химиялық қасиеттерін үш бағытта қарастырған ыңғайлы:
- •3. Галогендеу реакциясы
- •Акрил қышқылы.Өнеркәсіпте мынадай схема бойынша алады:
- •Олеин қышқылы с17н33соон Бұл қышқыл пальмитин және стеарин қышқылдар қатарында майлар түзеді.
- •Екі негізді қаныққан қышқылдар. Қаныққан екі негізді ышқылдардың жалпы формуласы CnH2n(cooh)2
- •Физикалық қасиеттері. Екі негізді қышқылдар - суда ерімтал, түссіз кристалды заттар.
- •Химиялық қасиеттері. Екі негізді қышқылдар, бір негізді қышқылдарға қарағанда күштірек келеді. Оның себебі, диссоциациялануын жеңілдететін карбоксилдердің өзара әсерлері:
- •12 Дәріс. Алифатты қатардың азотты қосылыстары.
- •Алыну жолдары. Аминдер техникада және лабораториялық практикада көп қолданылады. Сондықтан бірнеше жолмен алынады.
- •Химиялық қасиеттері. Нитроқосылыстардың ең маңызды химиялық қасиеттері нитротроптың өзіндік структурасына байланысты.
- •Изомерлері. Бір негізді оксиқышқылдардың гомологтық қатары оксиқұмырсқа немесе көмір қышқылынан , басталады. Одан кейін, гликоль немесе оксисірке қышқылы келеді.
- •Химиялық қасиеттері. Оксиқышқылдар қышқылдардың да, спирттердің де қасиеттерін көрсетеді. Бұлар қышқылдар тәрізді тұздар, күрделі эфирлер, амидтер түзеді. Мысалы сүт қышқылы:
- •Екі негізді төрт атомды қышқылдар. Бұл топтың басты өкілдерінің бірі шарап қышқылы
- •Оптикалық изомерлері. Көптеген оксиқышқылдарда ассиметриялы көміртек атомдары болады. Ассиметриялық көміртек атомы деп, көміртек атомы әр түрлі төрт топпен байланысқан жағдайды айтады.
- •14 Дәріс. Көмірсулар
- •15 Дәріс. Аминоқышқылдар
- •2.3 Зертханалық сабақтардың жоспары.
- •1 Органикалық химия лабораториясындағы жұмыстардың жалпы ережелері. Техника қауіпсіздігі.
- •2 Органикалық қосылыстарды тазалау тәсілдері
- •3 Қаныққан және қанықпаған көмірсутектер
- •4 Қаныққан көмірсутектердің галоген туындылары
- •5 Альдегидтер, кетондар, карбон қышқылдары
- •Бақылау сұрақтары
- •Майлар мен сабындар
- •7 Көмірсулар
- •2.3 Тәжірибелік сабақтар
- •2.4 Оқытушының жетекшілігімен орындалатын студенттердің өзіндік жұмыстары бойынша өткізілетін сабақтардың жоспары (соөж)
- •2.5 Студенттердің өздік жұмыстары бойынша сабақ жоспары (сөж)
- •2.6 Өздік бақылау үшін тест тапсырмалары
- •А) тотығу
- •В) спирт, қышқыл және метал күйіндегі күміс
- •2.7 Курс бойынша емтихандық сұрақтар тізімі
- •Глосарий
- •Алифаттық қатардағы қосылыстардың органикалық химиясы
4 Дәріс. Қанықпаған көмірсутектер. Этилендік көмірсутектер (алкендер)
Этилендік көмірсутектер деп молекулаларындағы көміртек атомы бір-бірімен қос байланыс арқылы байланысқан органикалық қосылыстарды айтады. Этилендік көмірсутектердің жалпы формуласы СnH2n. Бұлардың ең қарапайым өкілі этилен СН2 = СН2.
Изомерлері. Этилендік көмірсутектердің гомологтық қатарының структуралық изомериясы қаныққан көмірсутектері сияқты төртінші мүшесінен басталады. Алайда, бұларға бірнеше изомер түрі тән.
1. Қанықпаған көмірсутектердің құрылымына байланысты изомерлері
Мысалы: C5H10
![]()
![]()
׀
CH3
![]()
׀
CH3
2. Қанықпаған көмірсуктердегі қос байланыстың орналасу орнына байланысты изомерлері:
![]()
3. Геометриялық кеңістіктік изомерлері де тән.
Мысалы: 2-бутен
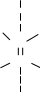
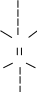
H CH3 H CH3
C C
C C
H CH3 H3C H
цис - 2 - бутен транс - 2 - бутен
Олефиндердің жүйелік номенклатура бойынша аталуы өздерімен құрылысы бірдей парафиндердің атынан түзіледі, бұл үшін парафиндер аттарының ан деген жалғауы ен-ге ауыстырылады және цифрмен қос байланыстың орны көрсетіледі. Көміртек атомдарын нөмірлеу жақын тұрған қос байланыс жағынан басталады.Мысалы:
![]()
СН3 2-метил-2-бутен
Рационалдық номенклатура бойынша олар этиленнің туындысы есебінде қарастырылады. Мысалы:
CH3 - CH = CH - CH - CH3
CH3
метилизопропилэтилен
Тарихи аталу бойынша тиісті қаныққан көміртегіндегі ан жалғауын илен жалғауына айырбастау арқылы атайды.
![]()
бутилен
Алыну тәсілдері 1. Олефин қатарының алғашқы төрт мүшесін таза күйінде мұнай өнімдерін жоғары температурада ыдырату арқылы алады.
2. Зертханалық жағдайда алудың ең көп тараған жолы ол спирттерді сусыздандыру арқылы алу
![]()
׀ ׀
Н ОН
Сусыздандыру катализаторы ретінде әртүрлі қышқылдар (күкірт, фосфор қышқылдары), қышқыл тұздар (КНSO4) т.б. қолданылады.
3. Этиленді өнеркәсіпте ацетиленнен алады:
![]()
Физикалық қасиеттері. Қанықпаған көмірсутектердің гомологтық қатарындағы алғашқы төрт мүшесі газдар.
С5 - С17 - сұйықтар,
С18 - қатты заттар.
Олефиндерді тығыздығы бірден кем, суда ерімейді.
Химиялық қасиеттері. Этилен тобына жататын көмірсутектер құрылысы жөнінен ұқсас, сондықтан химиялық қасиеті жөнінен де бір-біріне ұқсас келеді. Бұлардың химиялық қасиеттері қос байланыстың табиғатына тікелей байланысты. Қос байланыстың біреуі σ, біреуі π – байланыс. σ - байланыс π - байланысқа қарағанда өте берік. Сондықтан π - байланыс жылдам үзіліп, σ - байланысқа айналады, демек, алкендерге тек қос байланыс арқылы қосылу реакциясы тән болғаны.
Қосылу реакциясы барысында қос байланыс электрондар доноры есебінде қатысады. Сондықтан оларға электрофильді қосылу тән.
1. Сутектендіру реакциясы. Жоғары температурада және катализатор қатысқан уақытта алкендер өздеріне сутегін оңай қосып алады.
![]()
К атализатор есебінде Pt; Pd және ұнтақталған Nі қолданылады. Лебедев қағидасы бойынша, алкендердегі қос байланыстың орынбасарлары аз болған сайын, олар оңай сутектенеді. Айталық, RCH = CHR не CH3 - CH = CH - CH3 диметилэтилен бутен-2
CH2 = CH - CH3 метилэтилен, пропилен
Яғни, жоғарыда келтірілген қағида бойынша пропилен, бутен-2-ге қарағанда оңай сутектенеді.
2. Галогендеу реакциясы. Алкендер галогендерді оңай қосып алады да, алкендердің қос галоген туындыларын түзеді.
![]()
этилен дибром этан
Қосылу реакциясы қос байланыстағы орынбасарлар көбейген сайын оңайлана түседі. Бұл этилендік байланыстағы электрондар тығыздығымен түсіндіріледі.
Алкендердің галогендермен әрекеттесу рекациясы, оның ішінде броммен әрекеттесу реакциясы оларды ерітіндіден сапалық және сандық анықтау барысында қолданылады. Жұтылған бром санына байланысты алкендердің құрамын толық анықтауға болады.
3.
Гидрогалогендеу
реакциялары.
Алкендер
галогенсутектерді де, өздеріне оңай
қосып алады. Соның нәтижесінде келесі
теңдеу бойынша галогеналкилді түзеді:![]()
Галогенсутектердің симметриялы емес алкендерге қосылуы Марковников ережесі бойынша жүреді. Ол ереже былай айтылады: галогенсутектер симметриялы емес қанықпаған көмірсутектерге қосылу барысында, олардың құрамындағы сутегі әр уақытта сутегі атомдары көп көміртегіне, ал галоген аз сутектенген көміртегіне қосылады.
Мынадай
мысал келтірейік: ![]()
׀
Br
2-бромпропан
Мұндай заңдылықты қалай түсіндіруге болады? Енді осыны қарастыралық. Пропиленнің этиленнен айырмашылығы- оның молекуласында СН3 радикалы бар. Міне осы радикалдың қос байланысқа әсер етуінен қосылу реакциясы қалай болса солай жүрмей, белгілі бағытта жүреді. Енді осы әсердің мәні неде? Метил радикалындағы С - Н элементтердің теріс зарядтығының әртүрлі болуы салдарынан көміртек атомы байланыстығы сутек атомдарымен бірігіп электрон тығыздығы өз жағына қарай ығыстыратындықтан теріс зарядталады. Оның әсерінен артық электрон тығыздығы радикалмен көршілес көміртек атомына қарай ығысады, осының салдарынан σ - байланысының өте қозғалғыш бұлтын көміртегінің ең шеткі атомына қарай ығыстырады. Электрондардың мұндай ығысуын структуралық формулада былай бейнелеуге болады:
H

H C CH=CH2
H
Алкил тобының мұндай әсерін оң индукциялық эффект деп атайды.
Сөйтіп алкил тобының (+J) қос байланысқа әсерін басқаша түрде былай көрсетуге болады.
![]() .
.
![]() .
(R
- CH3,
C2H5,
C3H7,
т.б.)
.
(R
- CH3,
C2H5,
C3H7,
т.б.)
Дельта плюс (электрон тығыздығы аз), дельта минус (электрон тығыздығы көп) әріптерімен аздаған оң және теріс зарядтарды белгілейміз. Олай болса, галогенсутек молекуласындағы оң зарядталған сутек ионы ішінара теріс зарядталған галоген СН буынына қосылады. Сөйтіп, реакция иондық механизм бойынша, яғни Морковников ережесі бойынша жүреді.
Н2О, Н2SO4 сияқты реагенттер де олефинге галогенсутектер сияқты қосылады.
