
- •Силлабус
- •Силлабус
- •Пререквизиты учебной дисциплины
- •5. Характеристика учебной дисциплины
- •6. Список основной и дополнительной литературы
- •7. Контроль и оценка результатов обучения
- •Политика учебной дисциплины
- •Глоссарий
- •Лекция №1.
- •Лекция № 2. Квантово-механическая модель атома. Квантовые числа, их физический смысл.
- •Лекция № 3
- •Лекция № 4 Теоретические методы, применяемые при изучении строения молекул и химической связи. Основные положения методов валентных связей.
- •Лекция № 5. Энергетика химических реакций. I закон термодинамики. II закон термодинамики
- •II закон термодинамики
- •Контрольные вопросы
- •Лекция № 6. Химическая кинетика
- •Контрольные вопросы
- •Лекция № 7.
- •Контрольные вопросы
- •Лекция №8 Свойства растворов. Растворы электролитов. Теория электролитической диссоциации. Ионное произведение воды.
- •Лекция №9 Растворы неэлектролитов. Закон разбавления Оствальда. План.
- •Контрольные вопросы
- •Окислительно-восстановительные реакции и электрохимические процессы. Процессы окисления и восстановления.
- •Контрольные вопросы
- •1. Коррозия металлов.
- •Методы защиты от коррозии
- •Номенклатура комплексных соединений
- •Методы установления координационных формул
- •Устойчивость комплексных соединений
- •Контрольные вопросы
- •Лекция № 14 Коллоидно-химические основы охраны окружающей среды.
- •Лекция №15 Химическая идентификация: качественный и количественный анализ, физико-химические методы анализа.
- •Тема: Методы очистки веществ. Фильтрование.
- •План занятия:
- •Лабораторный практикум
- •Вопросы и задания
- •Лабораторная работа №3
- •Лабораторный практикум
- •Лабораторная работа №5 Тема: Перегонка. Перекристаллизация.
- •Вопросы и задания:
- •Лабораторная работа № 7 Тема: Скорость химических реакций. Взаимодействие тиосульфата натрия с серной кислотой.
- •Лабораторный практикум
- •Вопросы и задания
- •Лабораторный практикум
- •Лабораторная работа № 8
- •Лабораторный практикум
- •Контрольные вопросы и задачи.
- •Лабораторная работа № 9
- •Лабораторный практикум
- •Лабораторный практикум
- •Вопросы и задания
- •Лабораторный практикум
- •Вопросы и задания
- •Лабораторная работа №12 Тема: Водород. Получение и химические свойства водорода.
- •Лабораторный практикум
- •Лабораторная работа №13 Тема: Кислород. Получение и химические свойства кислорода.
- •Упражнения и задача
- •Лабораторная работа № 14 Тема: Комплексные соединения. Химические свойства комплексных соединений.
- •Получение и свойства окиси кобальта
- •Получение аммиаката никеля
- •Упражнения
- •Лабораторная работа№ 15 Тема: Химия металлов и их соединений. Химия неметаллов и их соединений.
- •1) Плавление серы. Получение пластической серы
- •2) Получение ромбической серы
- •Получение калийной селитры
- •Реакция открытия ионов Na- и к'
- •Вопросы
Устойчивость комплексных соединений
Комплексный ион способен диссоциировать на составные части. В растворе, содержащем комплексные ионы, устанавливается подвижное равновесие, к которому применим закон действующих масс. Например, [Co(NH3)6]3+↔Co3++6NH3.
Константа равновесия
в этом случае называется константой
нестойкости комплексного иона ![]()
Чем меньше Kн, тем более устойчив комплексный ион.
Пример1. Определить концентрации ионов и молекул в 0,1 М растворе [Zn(NH3)4]SO4, Кн=2,6∙10-10.
Решение.
Диссоциация соли происходит по уравнению
[Zn(NH3)4]SO4=[Zn(NH3)]42++SO4-2,
при этом из 0,1 моля соли образуется 0,1
моль комплексного иона и 0,1 моль SO42-.
Диссоциация [Zn(NH3)4]2+
протекает в незначительной степени
ввиду низкого значения Кн.
Из уравнения диссоциации [Zn(NH3)4]2+=Zn2++
4NH3
видно, что [Zn2+]=4[NH3].
Обозначив [Zn2+]=x,
получим![]() Решая это уравнение, найдем
х=2,52∙10-3г∙ион/л
и, следовательно, [NH3]=10,1∙10-3
моль/л.
Решая это уравнение, найдем
х=2,52∙10-3г∙ион/л
и, следовательно, [NH3]=10,1∙10-3
моль/л.
Пример2. Определить степень диссоциации комплексного иона [Zn(NH3)4]2+ в 0,1 молярном растворе [Zn(NH3)4]SO4.
Решение.
Обозначим концентрацию [Zn2+],
образовавшегося при диссоциации
комплексного иона, через х. Тогда
[NH3]=4х,
а [Zn(NH3)4]2+=(0,1-
x) моль/л. Подставим равновесные
концентрации компонентов в уравнение![]() Поскольку х<<0,1, то 0,1–х ≈ 0,1. Тогда
2,6∙10-11=256х5,
х=2,52∙10-3
моль/л и степень диссоциации комплексного
иона
Поскольку х<<0,1, то 0,1–х ≈ 0,1. Тогда
2,6∙10-11=256х5,
х=2,52∙10-3
моль/л и степень диссоциации комплексного
иона
α=2,52∙10-3/0,1=0,025=2,5%.
Контрольные вопросы
1. Установить, в каких случаях произойдет взаимодействие между растворами указанных электролитов. Написать уравнения реакций в молекулярной и ионно- молекулярной форме:
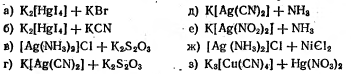
Дать названия следующим соединениям:
K[Fe(NH3)2(CN)4], K4[Fe(CN)6], Na2[PtCl6], [RhI3(NH3)3)], [Ag(NH3)2]Cl, [Co(NO2)3(H2O)3]
Лекция № 14 Коллоидно-химические основы охраны окружающей среды.
Цель: рассмотреть коллоидно-химические основы охраны окружающей среды.
План
Загрязнения биосферы.
Пагубное влияние химикатов на животных.
Анионактивные вещества и СМС
Пагубное влияние ПАВ
Когда говорят о биосфере, то подразумевают под этим термином как растительный мир, включающий высшие и низшие растения, так и животный мир, в том числе и человечество. Очевидно, что только человек в своей, так называемой, «разумной» деятельности способен создать условия, когда все живое может погибнуть. Таковы, например, последствия загрязнения окружающей среды от аварий на атомных электростанциях или химических предприятиях, производящих отравляющие вещества и ядохимикаты для уничтожения растительности.
Установлено, например, что в зоне чернобыльской катастрофы обнаружен радиоактивный элемент Америций-241, обладающий высокойтоксичностью. Этот элемент вызывает отек легких у теплокровных животных и человека и другие болезни, но самое страшное его действие состоит в изменении генетического аппарата человека. Он легко растворим в воде, переносится с пылью и уже обнаружен в Киеве. Образуется он после распада плутония, используемого в качестве топлива АЭС. По количеству обнаруженного Америция-241, период полураспада которого примерно 430 лет, можно утверждать, что выброшено в окружающую среду было не около 4% ядерного топлива, как это утверждалось официальными лицами бывшего Советского Союза, а около 30%. Этот факт вызывает серьезные опасения в дальнейшем развитии событий. Есть сведения об обнаружении Америция-242, критическая масса которого необычайно мала, так что постоянно присутствует опасность микровзрывов и дальнейшего разрушения саркофага чернобыльской АЭС. Период полного распада этого элемента – 16 часов.
Попадающие на растительность радиоактивные загрязнения поглощаются с пищей животными и концентрируются в их организме. Как известно в коровьем молоке содержится не только полезный для человека кальций, но и ряд микроэлементов. Если корова поедает траву с радиоактивными загрязнениями, то они попадают в молоко. Для обезвреживания такого молока и питьевой воды в районах с относительно небольшим загрязнением радиоактивными веществами используют метод ионообменной адсорбции. Целый ряд растений способен накапливать радиоактивные загрязнения. Например, березы в момент образования сока весной активно концентрируют радиоактивный кобальт, являющийся продуктом распада активноговещества атомной бомбы. Есть сведения, что люди, по незнанию употреблявшие такой сок из берез, находившихся вблизи ядерных полигонов, заболевали лучевой болезнью и погибали.
Вредные воздействия на организм человека, а также других представителей животного мира, возможны при попадании вредных веществ через внешние покровы (кожу, глаза), с воздухом через органы дыхания и с пищей и водой через органы пищеварения.
Очевидно, что коллоидно-химические явления могут быть использованы при разработке специальных средств и методов защиты человека, например, при разработке средств защиты внешних покровов – специальной одежды или специальных кремов с защитными свойствами против жидких, пылеобразных и парообразных вредных веществ. Специальной одежде можно придавать заданные свойства – гидрофобность, маслоотталкивание, пыле- и грязеотталкивание, кислотостойкость и т.д., в результате адсорбции полимерных и поверхностно-активных веществ, снижающих свободную поверхностную энергию волокон и подавляющих капиллярное впитывание жидкостей тканями.
Накопление в воде и в живых организмах вредных веществ, в том числе и поверхностно-активных веществ, приводит к аккумуляции их в организмечеловека. В результате этого, попадая в организм человека и концентрируясь в некоторых органах, например, неионогенные ПАВ, вызывают нарушение специфической и неспецифической имунно-биологической реактивности. В присутствии ПАВ в организмах теплокровных животных и человека накапливается большее количество тяжелых металлов, чем без них.
Анионактивные вещества и СМС на их основе способны изменять проницаемость мембран клеток организма и даже повреждать их. В результате этого затрудняется деятельность организма, возникает напряженность защитных сил организма, предшествующая проявлению выраженных патологических сдвигов, развивающихся под влиянием поверхностно-активных веществ и СМС. Возможны нарушения липидного обмена, активация процессов свободнорадикального окисления, различного рода ферментные нарушения.
В связи с этим необходимо осуществлять тщательную очистку сточных вод, содержащих вредные вещества, в том числе и поверхностно-активные вещества и компоненты СМС, с тем, чтобы они не попадали в питьевую воду или не накапливались в пищевых продуктах. Для очистки питьевой водыи сточных вод, сбрасываемых в открытые водоемы, используют методы адсорбции, коагуляции, электрокоагуляции, флотации, пенной сепарации,ультрафильтрации и седиментации. Все эти процессы подробно рассматриваются в курсе коллоидной химии.
Известно, что образование аэрозолей и тонкодисперсных пылей приводит к тому, что при их вдыхании может возникать целый ряд заболеваний дыхательных путей, а также и последующее изменение функций ряда органов. Кроме того, в аэрозольном состоянии многие вещества способны изменять свои свойства. Так, например, угольная, сахарная, мучная пыли приобретают взрывоопасные свойства. В связи с этим возникает необходимость в разработке способов борьбы с запыленностью.
В ряде отраслей промышленности для борьбы с пылью используют увлажнение помещений, в которых осуществляют технологические процессы, связанные с пылеобразованием. Если вода плохо смачивает частицы дисперсной фазы пыли, то для борьбы с пылеобразованием используютрастворы ПАВ. Их применение основано на способности повышать смачивание пылеобразующего материала водным раствором. Было установлено, что апатитовая пыль лучше смачивается растворами неионогенных, а кварцевая пыль – растворами катионактивных ПАВ. Смачивание улучшается при увеличении концентрации растворов ПАВ вплоть до достижения критической концентрации мицеллообразования (ККМ). Таким образом, для снижения расхода ПАВ следует понижать ККМ используемых ПАВ, для чего часто бывает достаточным введение электролитов в используемыйраствор. Процесс адсорбции молекул (ионов) ПАВ на поверхности частиц протекает по миграционному механизму. Поэтому для полного смачиваниячастиц необходим контакт смачивающей жидкости с поверхностью дисперсной фазы не менее 0,5 с.
Для подавления пылеобразования в угольных шахтах рекомендовано использовать растворы неионогенных и анионактивных веществ. Смачиваниеугля для предотвращения пылеобразования возможно не только растворами ПАВ, но и пенами.
В ряде случаев для пылеподавления и пылеулавливания рекомендуют использовать водные растворы полимеров, например, полиэтиленоксида, которые повышают гидрофильность поверхности частиц пыли и улучшают их смачиваемость водой.
При разработке угольных пластов и пустой породы происходит обильное пылеобразование, наносящее непоправимый вред здоровью работающих в шахтах людей. Одним из способов подавления пылеобразования является создание экранов из пены. Такой способ позволяет снижать пылеобразование на 90%. Пенообразователь должен создавать пены устойчивые к действию пылевого аэрозоля различной природы материала частиц. Для снижения расхода пенообразователя используют специальные пеногенераторы, позволяющие получить пену при низкой концентрацииПАВ.
Защита органов дыхания людей от попадания вредных веществ проводится с помощью приборов, действие которых основано на адсорбциигазообразных веществ на специальным образом подобранном адсорбенте, в качестве которого часто используют активированный уголь. Типичным представителем таких приборов является противогаз. Для защиты от пыли используют респираторы, которые фильтруют загрязненный воздух, удаляя пылевидные загрязнения в результате гетероадагуляции частиц на волокнах.
Основные процессы и явления, лежащие в основе борьбы с загрязнением воздушной среды, в которой обитает человек, также подробно изучаются в курсе коллоидной химии.
Коллоидно-химические основы инженерной охраны окружающей среды будут рассмотрены в специальном учебно-методическом пособии, посвященном роли коллоидной химии в технологических процессах текстильного производства.
Контрольные вопросы.
Как используются коллоидные растворы для очищения ОС?
Какие коллоидные растворы в истории химии являлись загрязнителями ОС?
Используются ли на данный момент эти коллоидные растворы?
Какой вред наносят организму человека ПАВ?
