
- •Передмова
- •Тема 1. Шляхи усунення втрат сільськогосподарської продукції
- •Тема 2. Технології збереження сільськогосподарської продукції
- •Норми природних втрат зерна при зберіганні, %
- •Тема 3. Вплив визначальних факторів на якість продукції при її збереженні
- •Тема 4. Основи переробки сільськогосподарської продукції
- •Попередня обробка
- •Види механічної обробки
- •Види термічної обробки
- •Тема 5. Вологий матеріал
- •Тема 2. Способи зневоднення сільськогосподарської продукції
- •Стан системи визначається сукупністю її інтенсивних властивостей – параметрів, якими можуть бути тиск, температура, концентрація, питомий об’єм.
- •Тема 3. Термодинамічні характеристики вологих матеріалів
- •Тема 4. Теплофізичні характеристики (параметри) вологих матеріалів
- •Тема 5. Основи масопередачі
- •Тема 6. Технічні засоби сушіння сільськогосподарських матеріалів Лекція 11. Конструкційні особливості сушарок сільськогосподарського призначення
- •Перелік питань, які включені до екзаменаційних білетів
Тема 5. Вологий матеріал
Лекція 1. Особливості вологих матеріалів
1. Класифікація вологих матеріалів
2. Визначення стану вологого матеріалу
1. Всі тверді вологі матеріали за колоїдально-фізичними властивостями А.В.Ликов запропонував ділити на три групи: капілярно-пористі, колоїдальні і капілярно-пористі колоїдальні.
Така класифікація дозволяє визначитись з технологічним процесом обробітку вологих матеріалів, оскільки при цьому відбуваються зміни їх властивостей, що важливо врахувати для ефективного і якісного отримання продуктів.
Під технологічними властивостями розуміють різні властивості (структурно-механічні, біологічні, фізико-хімічні, теплофізичні та інші), специфічні для кожного матеріалу в певних умовах (режимах) його обробітку.
У процесі сушіння великої кількості сільськогосподарської продукції важливу роль відіграє їх термостійкість, яка визначає збереження початкових якісних параметрів.
До капілярно-пористих тіл відносять матеріали, в яких рідина в основному зв’язана капілярними силами. При зневодненні капілярно-пористі тіла стають крихкими і після висушування їх легко перетворити в порошок. Вони мало стискаються і поглинають будь-яку змочуючу рідину. Для таких тіл капілярні сили значно перевищують сили тяжіння, тому вони повністю визначають розподіл рідини в тілі. Якщо потенціал поля тяжіння (гравітаційний потенціал) рівний капілярному потенціалу в тілі, то такі тіла називають пористими. Прикладом є вологий кварцевий пісок.
До колоїдних тіл відносять матеріали, в яких переважає адсорбційно зв’язана і залишкова втримувана волога. Наприклад, желатин, пресоване тісто з борошна. При зниженні вологості колоїдні тіла зменшуються в об’ємі, зберігають свою еластичність. При зволоженні вони поглинають найбільш близькі за полярністю рідини.
До капілярно-пористих колоїдних тіл відносять матеріали, в яких рідина має різні форми зв’язку, які присутні як у капілярно-пористих, так і в колоїдальних тілах. До них відноситься основна маса харчових продуктів, які за своєю структурою є капілярно-пористі тіла, а за природою колоїдні. Стінки таких капілярів еластичні і при поглинанні збільшують свої розміри, а при зневодненні зменшуються і стають крихкими.
Аналіз властивостей колоїдних капілярно-пористих колоїдних тіл показує, що практично провести межі між окремими видами вологи і їх зв’язком з твердим скелетом фактично неможливо.
Природа утворення різних видів зв’язку вологи обумовлює механізм її видалення при сушінні. Так, для видалення адсорбційно зв’язної води її необхідно всередині матеріалу перетворити в пару, після чого вона почне переміщуватись на поверхню матеріалу.
Волога набухання більшою частиною переміщається всередині матеріалу у вигляді рідини шляхом дифузії через стінки клітин. В залежності від режиму процесу капілярна волога переміщується як у вигляді рідини (за рахунок капілярних сил), так і у вигляді пари (за рахунок різних тисків).
Вологі матеріали є капіляропористими колоїдними тілами. Вони належать до класу зв’язно-дисперсних систем, у яких частини дисперсної фази утворюють більш-менш жорсткі структурні сітки, або каркаси.
Всі вологі матеріали залежно від їх основних колоїдно-фізичних властивостей можна розділити на три види:
- Типові колоїдні тіла (еластичні гелі). У разі видалення з них рідини вони значно змінюють свої розміри – зменшуються, але зберігають свої еластичні властивості.
- Капілярні тіла (крихкі гелі). При видаленні рідини цi тіла стають крихкими, мало стискаються, легко подрібнюються.
- Капілярно-пористі колоїдні тіла, які володіють властивостями перших двох видів. Стінки капілярів цих матеріалів еластичні і за наявності рідини збільшуються.
Загалом вважається, що характерними розмірами для пористого тіла є розміри з довжиною капілярів у межах l= 10 см. Тоді його можна називати також капілярним. Але, якщо радіуси капілярів менші за 0,01 мм, то саме тіло називають капілярнопористим.
Для характеристики стану вологи в матеріалі важливе значення має явище, яке виникає на поверхні розділення фаз (рідка – тверде тіло). Таке явище називають явищем адсорбції. Розрізняють фізичну і хімічну адсорбцію і вивчають їх на рівні молекул.
Щоб перемістити молекулу із об’єму рідини на її поверхню, необхідно перебороти сили притягування, тобто виконати роботу.
Таке переміщення у матеріалах відбувається по капілярах, які поділяються на мікрокапіляри, макрокапіляри й макропори, або каверни.
Під пористим середовищем, як правило, приймають тверде тіло, що складається з щілин. Точного визначення щілин (пор) не існує. В загальному розумінні, це наявність пустих проміжків, які можуть бути з’єднанні між собою або не з’єднанні. Якщо всі щілини з’єднанні між собою, то такий простір називають ефективний поровий простір. Цей термін широко застосовується у теорії фільтрації.
Існує безліч теорій вивчення будови пористих тіл, спроб моделювання їх пор. Найбільш простою моделлю вважається система прямих капілярів, більш складною – система паралельних капілярів, з’єднаних між собою. Капіляри правильної геометричної форми називають ще елементарними (циліндричні, конічні капілярні труби, капілярні щілини і т.д.).
Такі капіляри являються моделями капілярних пор і застосовуються для аналізу поведінки рідини в капілярно пористих тілах. Розглянемо основні співвідношення для елементарних капілярів.
Висота підняття рідини в капілярній трубці радіусом r визначається відомим співвідношенням Жюрена:
Рис. 1.1. Рідина в похилому
капілярі |
h= де θ – рівноважний крайовий кут розтікання рідини по поверхні;
|
Дане відношення справедливе при хорошому змочуванні капіляра. При недостатньому змочувані висота підняття рідини у капілярі буде дещо меншою. Якщо капіляр не циліндричної форми, а має вигляд вузької щілини, то у запропонованому відношенні замість r приймають ширину щілини.
В нециліндричних капілярах (із змінними радіусами за довжиною) може бути не одне, а декілька рівноважних станів. При рівності радіусів (збільшення – зменшення) капілярів картина змочування виглядатиме наступним чином – при опусканні в рідину нециліндричного капіляра висота його змочування буде дорівнювати висоті змочування капіляра з більшим діаметром. Якщо такий капіляр опустити в рідину, а потім підняти, то висота змочування буде рівною висоті капіляра з меншим діаметром. |
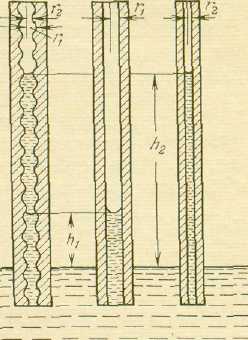
Рис. 1.2 Рівновага рідини в
нециліндричному капілярі
Затримка рідини на більш високому рівні, обумовлена розміщенням меніска на звуженні ділянки капіляра, називається «капілярним гістерезисом».
Отже, якщо капіляри по довжині змінюють свій радіус, то підняття рідини буде рівним висоті капіляра з меншим радіусом. Існує поняття капілярного потенціалу, який вказує на відношення капілярної енергії поля капілярних сил до маси рідини (ерг/г)
![]()
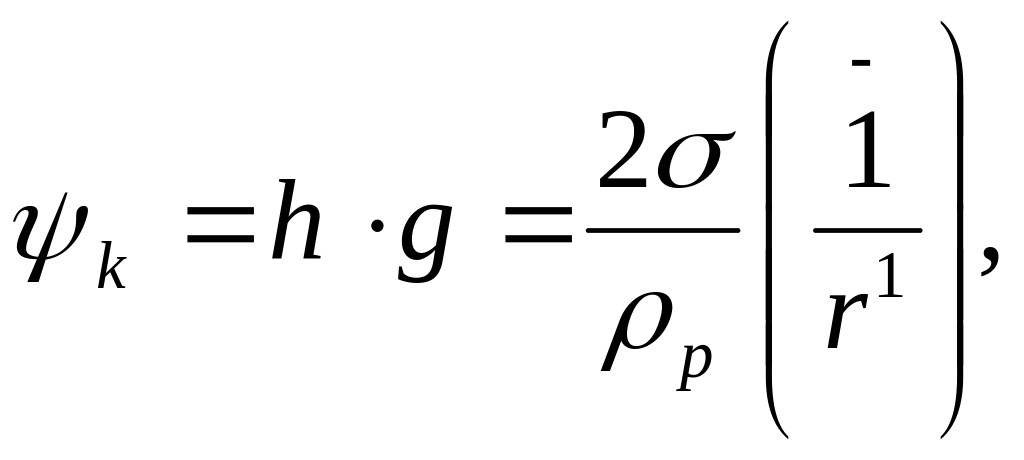 (1.2)
(1.2)
де
![]()
середня кривина меніска (r1=r/cos);
середня кривина меніска (r1=r/cos);
h висота підйому рідини у капілярі.
Р
n
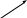
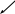

![]() n
n![]() n
n
l
l



Найбільш
негативне явище при зневодненні
матеріалів виникає, коли у них є або,
під дією певних факторів, утворюються
конічні капіляри (рис.3.1). Тоді потенціал
для таких капілярів визначається
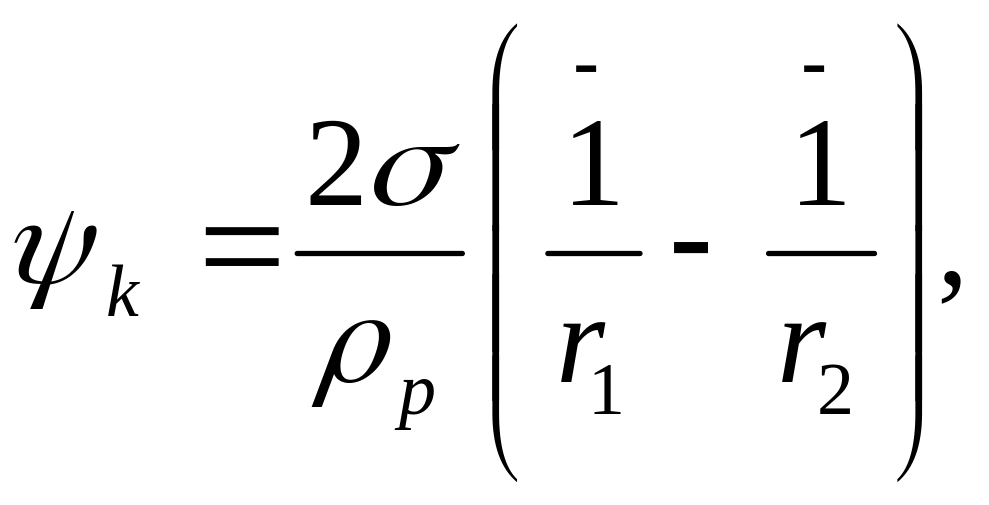 а
рідина переміщається в бік більш вузького
кінця до тих пір, поки меніск займе
крайнє положення і рідина перестане
рухатись.
а
рідина переміщається в бік більш вузького
кінця до тих пір, поки меніск займе
крайнє положення і рідина перестане
рухатись.
2. Сільськогосподарські матеріали у певному стані утримують в собі вологу. Стан вологого матеріалу визначається його температурою і вологістю. Вологість матеріалу визначається за відомими формулами.
Загальна маса вологого матеріалу становить:
![]() ,
(1.3)
,
(1.3)
де
![]() –
маса води, кг;
–
маса води, кг;
![]() – маса
сухої речовини.
– маса
сухої речовини.
Вологість матеріалу визначається у відсотках до маси сухої речовини:
![]() . (1.4)
. (1.4)
Таку вологість називають абсолютною. При встановленні відношення маси вологи до загальної маси матеріалу, у відсотках, отримують відносну вологість:
![]() (1.5)
(1.5)
Існують також формули для переходу від абсолютної вологості до відносної та навпаки:
![]() (1.6)
(1.6)
![]() . (1.7)
. (1.7)
Якщо вологість матеріалу по відношенню до сухої речовини виразити у кг/кг с.р., то матимемо вираз для визначення вологовмісту матеріалу (питомий масовміст)
![]()
![]() . (1.8)
. (1.8)
Розрізняють вологовміст, який характеризує вологість загального об’єму матеріалу і вологість у певному шарі (площині) або окремо взятій точці. Якщо волога рівномірно розподілена по січенню матеріалу, то
![]() або
або
![]() (1.9)
(1.9)
Під концентрацією вологи в матеріалі розуміють масу вологи, яка приходиться на одиницю об’єму матеріалу (в кг/м3). Існує залежність між концентрацією вологи та вологовмістом матеріалу
![]() (1.10)
(1.10)
де
![]() -
маса абсолютно сухої речовини в одиниці
об’єму
вологого матеріалу, кг с.р./м3.
-
маса абсолютно сухої речовини в одиниці
об’єму
вологого матеріалу, кг с.р./м3.
Якщо
об’ємне зменшення матеріалу в процесі
його зневоднення незначне, то
=
![]() ,
де
-
щільність сухої речовини матеріалу, кг
с.р./м3.
,
де
-
щільність сухої речовини матеріалу, кг
с.р./м3.
Знання взаємодії води з різними речовинами дозволяє встановити характер зв’яку вологи з твердим тілом. При цьому змінюють властивості не тільки твердої частини матеріалу, але й самої води.
Вода (грецька назва – гідро, латинська – аква) – окис водню – є найпростішим стійким з’єднанням водню (11,19 мас, %) з киснем (88,81 мас, %). У зв’язку з наявністю трьох ізотопів водню і шести ізотопів кисню існує 36 ізотопних різновидів води, десять з яких знаходиться у природному стані. Молекулярна маса води – 18,016; щільність при температурі 250С – 0,997 г/см3. Тільки при температурі 40С щільність природної води досягає 1,0 г/см3, тоді вона має найбільшу щільність.
Температура нагрівання матеріалу зумовлює збереження його якісних показників. Для кожного рослинного сільськогосподарського матеріалу існує своє граничне допустиме значення температури нагрівання, при якій не погіршуються його якісні показники, а насіннєвий матеріал не гине як живий організм. Гранично допустима температура залежить від вологості матеріалу і тривалості перебування його у нагрітому стані. Вона може бути високою за умови короткотривалого нагрівання і незначній вологості матеріалу.
Головною вимогою щодо сушіння сільськогосподарських рослинних матеріалів є збереження їх якісних показників. До таких показників відносять високі посівні і інші відповідні властивості матеріалів, які висуваються згідно з вимогами щодо подальшого їх використання.
Питання термостійкості, яке обумовлює інтенсифікацію процесу сушіння, є одним із головних при виборі способу сушіння.
Наявність жиру (гідрофобної речовини) у насінні олійних культур впливає на вологість гідрофобної частини. Тому кондиційну вологість насіння таких культур встановлено дещо нижчою і цей параметр необхідно враховувати при виборі температури нагріву насіння.
Якщо сушінню піддають насіннєві матеріали, то його нагрів обмежують температурою 43... 48°С, зернобобові – 30...35°С Продовольче зерно нагрівають не вище 60°С. Окремі листостеблеві матеріали можна нагрівати до 85°С без втрат якості.
Обмеження температури сушильного агенту при сушінні насіннєвих матеріалів пов'язане з тепловою денатурацією його білкового комплексу, яка відбувається при наявності певної кількості води. Безводний білок, якщо його нагрівати, не піддається денатурації навіть за температури, близької до 100°С.
Відомі формули Птіцина С.Р. та Хатчинсона Д. дозволяють визначити гранично допустимі температури насіннєвих матеріалів. Імперичні залежності Хатчинсона мають такий вигляд:
![]() (1.11)
(1.11)
![]() (1.12)
(1.12)
де
![]() –
температура
насіння, за якої настає зниження його
насіннєвих якостей, °С;
–
температура
насіння, за якої настає зниження його
насіннєвих якостей, °С;
t"гр – температура, яка обумовлює повну втрату схожості насіння, °С.
У свою чергу Птіциним С.Р. розділені формули нагріву насіння зернових та олійних культур, з урахуванням вмісту жиру:
![]() (1.13)
(1.13)
![]() ,
(1.14)
,
(1.14)
де Wі – інтегральна вологість,
τ – час обробітку;
W2 – вологість гідрофільної частини, яка має зв'язок із інтегральною вологістю за виразом:
![]() , (1.15)
, (1.15)
де А - вміст жиру в насінні у перерахунку на абсолютно суху речовину.
Гранично допустиму температуру нагріву матеріалу можна визначити і за експериментальними даними. Прикладом визначення гранично допустимої температури для вороху і вільного насіння льону є рис. 1.4. Різниця температур у 2...3о С вказує на демфуючу здатність коробочки насіння льону сприймати температуру у процесі його нагрівання.
40
3540
30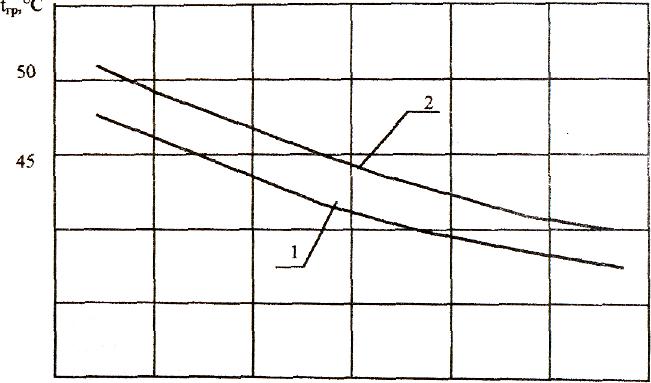
20 25 30 35 40 45 Wr,%
Рис.1.4. Залежність гранично допустимої температури нагрівання насіння льону від його вологості (1- для вільного насіння льону; 2 – для насіння льону в коробочках)
Поревим І.А., на основі проведених досліджень, встановлена точка tкр, яка характерна для процесу сушіння вороху льону. Ця точка знаходиться на перетині кривої часу, необхідного для зниження вологості вороху з 23 до 13% і часу сушіння, при перевищенні якого відбувається зниження енергії проростання насіння (рис.1.5). Даним методом можна побудувати аналогічні графіки для будь-яких насіннєвих матеріалів.

Рис. 1.5. Графічний метод визначення оптимального значення температури сушіння вороху льону
Лекція 2. Загальне поняття про утримання вологи у матеріалах
1. Класифікація форм зв’язку вологи в матеріалах
2. Енергія зв’язку вологи з матеріалом
1. Змінити стан матеріалу можна завдяки зміні їх рідинних умов: тиск, температура або хімічними реакціями. Загалом для спрощення досліджень вважається, що будь-який вологий матеріал у статичному стані може мати два види вологи: вільну і зв’язану. Але якщо враховувати природу утворення форм зв’язку вологи з матеріалом, енергію їх зв’язку, то існує класифікація, запропонована проф. П.А.Ребіндером, згідно з якою всі форми зв’язку вологи діляться на три великі групи:
хімічний зв’язок;
фізико-хімічний зв’язок;
фізико-механічний зв’язок.
1.Хімічний зв’язок вологи в точних кількісних співвідношеннях.
Хімічна зв’язна волога виключно міцно зв’язана з матеріалами і може бути відділена з нього лише при хімічних реакціях або особливим інтенсивним сушінням. При звичайному нагріві така волога не видаляється.
Фізико-хімічний зв’язок вологи в різних, не строго визначених відношеннях. Цій формі відповідають різні види зв’язку вологи:
а) адсорбційно зв’язна волога. Така волога є рідиною, яка утримується на зовнішній і внутрішній поверхнях “міцел” – колоїдних частин, умовний радіус яких складає 0,1-0,001 мкм.
Внаслідок вказаної дисперсності колоїдні тіла мають значну внутрішню поверхню і, відповідно, вільну поверхневу енергію, мірою енергії якої є поверхневий натяг σ.
Н
1
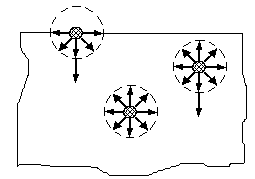
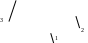
Рис. 1.6. Схема взаємодії двох фаз (рідина – пара) на межі розподілу
При поглинанні води колоїдним тілом виділяється теплота набухання (явище гідратації) і відбувається стискання системи колоїдне тіло – вода. Тому для видалення такого виду вологи, воду необхідно перетворити у пару, після чого вона переміститься до зовнішньої поверхні тіла.
б) залишкова утримувана волога (волога набухання і структурна волога) – відноситься до вологи, яка розміщена у гніздах складно побудованої міцели. Частина води шляхом осмосу потрапляє через стінку клітки, частина залишається на поверхні клітини. Але таке поглинання вологи тілом відбувається без виділення тепла та без стискання системи. Фактично за своїми властивостями осмотична волога не відрізняється від звичайної води.
3. Фізико-механічний зв’язок – утримання води в невизначених кількостях.
Такому зв’язку відповідають певні види вологи:
а) волога макрокапілярів. Ця частина води знаходиться в капілярах (порах), середній радіус яких більше 10-5 см. Тиск пари води над меніском макрокапіляра майже не відрізняється від тиску насиченої пари над вільною поверхнею води. Вода заповнює наскрізні макрокапіляри тільки у разі безпосереднього контакту з ними;
б) волога мікрокапілярів. Така волога заповнює вузькі пори. Середній радіус яких менше 10-5 см. Рідина заповнює будь-які мікрокапіляри як при безпосередньому контакті, так і шляхом сорбції із вологого повітря.
2. У якості єдиного критерію для класифікації форм зв’язку вологи з матеріалом проф. П.А.Ребіндер вважав величину вільної енергії ізотермічного зневоднення. За рахунок зв’язку води з матеріалом знижується тиск пари води на її поверхні. Тому вільна енергія відповідно зменшується.
Види зв’язку вологи: а – осмотична волога колоїдного тіла або волога капілярного стану в порах (r > 10-5см); б – стикова волога (r > 10-5см); в – капілярна волога мікропор (r < 10-5см); г – волога полі молекулярної адсорбції; д – волога мономолекулярної адсорбції. |
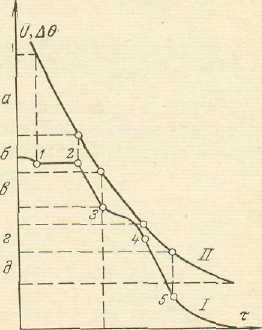
Рис. 1.7 Термограма сушіння(I)
і крива кінетики сушіння (II)
капілярно-пористих матеріалів
різної природи
Згідно схеми (рис.1.7) на основі аналізу термограм сушіння встановлено ряд сингулярних точок, які характеризують різні форми зв’язку вологи з капілярно пористими тілами. Вся волога у матеріалах утримується фізико-механічним та фізико-хімічну зв’язками.
До вологи фізико-механічного зв’язку відносять три види капілярної вологи, два з яких являють воду, різну за особливим станом (капілярну та стикову) в грубих порах тіла, а третій – капілярну вологу мікропор. Волога фізико-хімічного зв’язку може складатись з осмотичної води і двох видів адсорбованої вологи – вологи полі молекулярних і молекулярних шарів.
Зменшення
вільної енергії
![]() при
постійній температурі Т (або енергію
зв’язку) можна виразити затраченою
роботою А на відрив 1 моля води від
матеріалу (без зміни складу) в ерг/моль:
при
постійній температурі Т (або енергію
зв’язку) можна виразити затраченою
роботою А на відрив 1 моля води від
матеріалу (без зміни складу) в ерг/моль:
![]() , (1.16)
, (1.16)
де: R –газова постійна;
![]() – тиск
насиченої пари вільної води;
– тиск
насиченої пари вільної води;
![]() – порційний
тиск зрівноваженої пари води над
матеріалом з вологовмістом U
у
будь-якому середовищі (повітря, інертний
час, вакуум), тому
– порційний
тиск зрівноваженої пари води над
матеріалом з вологовмістом U
у
будь-якому середовищі (повітря, інертний
час, вакуум), тому
![]() .
.
Чим
міцніший зв’язок води з матеріалом,
тим менша величина Рu,
і навпаки, для вільної води Рu
досягає значення Рн.
При цьому
![]() і енергія зв’язку А = 0:
і енергія зв’язку А = 0:
![]() (1.17)
(1.17)
а) при зневодненні матеріалу величина А, віднесена до моля води, поступово зростає, оскільки із зменшенням вологості матеріалу зростає доля адсорбційної зв’язної вологи, яка видаляється зменшується. З моменту видалення хімічної вологи, величина А різко зростає і сягає до 104 дж/моль;
б) в свою
чергу адсорбційна зв’язана
вода відповідає мономолекулярному шару
на зовнішніх і внутрішніх поверхнях
дисперсного матеріалу. Для такої води
залежність тиску пари від вологості
матеріалу може бути отримана згідно з
ізотермою адсорбції. Ця форма зв’язку
вологи характерна для дуже малої
вологості матеріалу, тобто для незначної
величини
![]() ,
якій відповідає значна енергія зв’язку.
,
якій відповідає значна енергія зв’язку.
Так, наприклад, при
![]()
в) енергія зв’язку капілярно-зв’язаної води обумовлена адсорбційним зв’язком мономолекулярного шару у стінок капіляра і зниженням тиску пари над ввігнутим меніском у капілярах (позитивне змочування) у порівнянні з тиском пари над плоскою поверхнею вільної води. Вся вода, яка міститься в капілярі, не відрізняється від вільної води. Тому енергія зв’язку вологи макрокапілярів невелика і вона наближається до енергії вільної вологи.
При
невеликому діаметрі капіляра А досягає
значної величини. Так при
![]()
г) осмотично втримувана вода має дуже незначний енергетичний зв’язок. Це явище пояснюється тим, що тиск пари, наприклад, над розчином Рu менше тиску пари Рн над водою.
д) вода, яка вільно утримується в тонкому об’ємному каркасі тіла, захоплена (иммобілізаційна) при формуванні тіла в процесі його зволоження енергетичний зв’язок практично відсутній. Така вода з матеріалу видаляється механічним шляхом, причому процес зневоднення лімітується лише гідравлічним опаром каркаса тіла.

