
- •Оглавление
- •Глава 1 16
- •Глава 2 химическая связь 33
- •Глава 3 54
- •Глава 4 82
- •Глава 5 110
- •Глава 6 141
- •Глава 7 173
- •Глава 8 196
- •Глава 9 234
- •Глава 10 комплексные соединения и их свойства 272
- •Глава 11 297
- •Глава 12 316
- •Глава 13 377
- •Глава 14 400
- •Глава 15 основные понятия органической химии 419
- •Глава 16 445
- •Глава 17 474
- •Глава 18 499
- •Глава 19 518
- •Глава 20 562
- •Глава 21 аминокислоты, пептиды и белки 578
- •Глава 22 620
- •Глава 23 651
- •Глава 24 692
- •Глава 25 709
- •Глава 26 740
- •Глава 27 771
- •От автора
- •Глава 1 строение атома, периодический закон и периодическая система элементов д. И. Менделеева
- •1.1. Строение атома
- •1.1.1. Квантовые числа
- •1.1.2. Принципы заполнения атомных орбиталей электронами
- •1.2. Периодический закон и периодическая система элементов д. И. Менделеева
- •1.3. Основные характеристики атомов элементов
- •1.3.1. Радиус атома
- •1.3.2. Энергия ионизации
- •1.3.3. Энергия сродства к электрону
- •1.3.4. Относительная электроотрицательность
- •Глава 2 химическая связь
- •2.1. Ковалентная связь
- •2.1.1. И молекулярные орбитали
- •2.1.2. Механизмы возникновения ковалентной связи
- •2.1.3. Особенности ковалентной связи
- •2.2. Ионная связь
- •2.3. Металлическая связь
- •Глава 3 межмолекулярные взаимодействия и агрегатное состояние вещества
- •3.1. Межмолекулярные взаимодействия
- •3.2. Агрегатное состояние вещества
- •3.2.1. Твердое состояние
- •3.2.2. Жидкое состояние
- •3.2.3. Жидкокристаллическое состояние
- •3.2.4. Паро- и газообразное состояния
- •Глава 4 основы химической термодинамики и биоэнергетики
- •4.1. Основные понятия термодинамики
- •4.2. Первый закон термодинамики
- •4.3. Понятие о самопроизвольных процессах.
- •4.4. Второй закон термодинамики. Энергия гиббса
- •4.5. Принцип энергетического сопряжения биохимических реакций
- •Г лава 5 основы кинетики биохимических реакций и химического равновесия
- •5.1. Основные понятия и терминология раздела
- •5.2. Факторы, влияющие на скорость гомогенных реакций
- •5.2.1. Влияние природы реагирующих веществ
- •5.2.2. Влияние концентрации реагентов.
- •5.2.3. Влияние температуры. Энергия активации
- •5.2.4. Влияние катализатора
- •5.3. Особенности кинетики гетерогенных реакций
- •5.4. Особенности кинетики цепных реакций
- •5.5. Химическое равновесие
- •5.5.1. Смещение химического равновесия
- •5.6. Ферментативный катализ и его особенности
- •5.7. Автоколебательные биохимические процессы
- •Г лава 6 растворы и их коллигативные свойства
- •6.1. Вода как растворитель и ее роль в жизнедеятельности организма
- •6.2. Термодинамика процесса растворения
- •6.З. Способы выражения концентрации растворов
- •6.4. Коллигативные свойства растворов
- •6.4.1. Диффузия
- •6.4.2. Осмос. Осмотическое и онкотическое давление
- •6.4.3. Давление насыщенного пара над раствором
- •6.4.4. Температура кипения и замерзания раствора
- •Глава 7 растворы электролитов и ионные равновесия
- •7.1. Электролитическая диссоциация
- •7.2. Равновесие в растворах слабых электролитов
- •7.2.1. Влияние общего иона и противоиона на равновесие
- •7.2.2. Взаимосвязь константы диссоциации и степени диссоциации
- •7.3. Особенности растворов сильных электролитов. Ионная сила раствора
- •7.4. Электролитическая диссоциация и ионное произведение воды
- •7.5. Водородный и гидроксильный показатели (рН и рОн)
- •7.6. Физико-химические основы водно-электролитного баланса в организме
- •Г лава 8 теория кислот и оснований и протолитические равновесия
- •8.1. Протолитическая теория кислот и оснований
- •8.2. Кислотно-основные свойства а-аминокислот
- •8.3. Важнейшие кислотно-основные реакции
- •8.3.1. Гидролиз солей
- •8.3.2. Реакции нейтрализации
- •8.3.3. Общая, активная и потенциальная кислотность растворов
- •8.4. Протолитический баланс. Буферные растворы и их свойства
- •8.5. Буферные системы организма, их взаимодействие, явления ацидоза и алкалоза
- •9.1. Основные понятия и факторы, влияющие на протекание окислительно-восстановительных реакций
- •9.2. Направление протекания окислительно-восстановительных реакций
- •9.3. Особенности биохимических окислительно-восстановительных процессов в организмах
- •9.3.1. Степень окисления углерода в органических соединениях
- •9.3.2. Биохимические реакции внутри- и межмолекулярной окислительно-восстановительной дисмутации за счет атомов углерода
- •9.3.3. Окислительно-восстановительные превращения кофакторов и коферментов оксидоредуктаз
- •9.3.4. Электронотранспортные цепи
- •9.3.5. Дегидрогеназное окисление-восстановление
- •9.3.6. Окислительное фосфорилирование
- •9.3.7. Фотофосфорилирование
- •9.3.8. Оксигеназное окисление-восстановление
- •9.3.9. Свободнорадикальное окисление и антиоксидантная система организма
- •9.4. Использование окислителей и восстановителей в медико-санитарной практике
- •Глава 10 комплексные соединения и их свойства
- •10.1. Основные понятия и терминология
- •10.2. Химическая связь в комплексных соединениях и особенности их строения
- •10.3. Химические свойства комплексных соединений
- •10.4. Медико-биологическая роль комплексных соединений
- •10.5. Металлолигандный баланс и его нарушения
- •10.6. Комплексонометрия
- •Глава 11 гетерогенные процессы и равновесия в растворах
- •11.1. Основные понятия и теоретические основы
- •11.2. Гетерогенные равновесия в растворах, связанные с процессом кристаллизации
- •11.3. Гетерогенные равновесия в растворах, связанные с процессом расслоения
- •11.4. Гетерогенные равновесия в живых системах
- •Глава 12 химия элементов-органогенов
- •12.2. Строение, химические свойства и роль элементов-органогенов и их соединений в растительном и животном мире
- •12.2.1. Водород и его соединения
- •12.2.2. Углерод и его соединения
- •12.2.3. Азот и его соединения
- •12.2.4. Фосфор и его соединения
- •12.2.5. Кислород и его соединения
- •12.2.6. Сера и ее соединения
- •12.3. Строение и химические свойства галогенов и их соединений
- •Глава 13 химия ионов металлов жизни и их роль в растительном и животном мире
- •13.1. Химия ионов s-металлов в организме
- •13.1.1. Натрий и калий
- •13.1.2. Магний и кальций
- •13.2. Химия ионов d-металлов в организме
- •13.2.1. Марганец
- •13.2.2. Железо и кобальт
- •13.2.3. Медь
- •13.2.4. Цинк
- •13.2.5. Молибден
- •Глава 14 химия и анализ загрязнений окружающей среды
- •14.1. Химия загрязнений атмосферы
- •14.1.1. Токсический смог
- •14.1.2. Фотохимический смог
- •14.1.3. Кислотные дожди
- •14.1.4. Загрязнение атмосферы другими токсикантами
- •14.1.5. Разрушение озонового слоя
- •14.2. Методы анализа токсикантов и методы снижения их поступления в атмосферу
- •14.3. Загрязнение гидросферы. Понятие об общих показателях, характеризующих природные и сточные воды
- •Глава 15 основные понятия органической химии
- •15.1. Основы классификации и номенклатуры органических соединений
- •15.2. Пространственная структура биоорганических молекул и виды изомерии
- •15.3. Понятие о взаимном влиянии атомов в молекуле и электронные эффекты
- •15.4. Классификация органических реакций и их компонентов
- •Г лава 16 алифатические и ароматические углеводороды
- •16.1. Строение и реакционная способность алканов
- •16.2. Строение и реакционная способность ненасыщенных углеводородов: алкенов и диенов
- •16.3. Ароматические углеводороды (арены)
- •Глава 17 спирты, фенолы, простые эфиры, тиолы и сульфиды
- •17.2. Физико-химические свойства спиртов и фенолов
- •17.3. Химические свойства спиртов
- •17.4. Химические свойства фенолов
- •17.5. Простые эфиры
- •17.6. Тиолы и сульфиды
- •Г лава 18 альдегиды, кетоны и их производные
- •18.1. Строение, номенклатура и физико-химические свойства альдегидов и кетонов
- •18.2. Химические свойства альдегидов и кетонов
- •18.2.1. Кислотно-основные свойства
- •18.2.2. Электрофильно-нуклеофильные свойства
- •18.2.3. Окислительно-восстановительные свойства
- •18.2.4. Комплексообразующие свойства
- •18.3. Альдегиды и кетоны в окружающей среде
- •Г лава 19 карбоновые кислоты и их функциональные производные
- •19.2. Химические свойства предельных кислот и их производных
- •19.2.1. Кислотно-основные свойства
- •19.2.2. Карбоновые кислоты как ацилирующие реагенты
- •19.2.3. Производные карбоновых кислот, их свойства и взаимные превращения
- •19.2.4. Окислительно-восстановительные свойства карбоновых кислот и их производных
- •19.3. Особенности свойств замещенных карбоновых кислот и их производных
- •19.3.1. Дикарбоновые кислоты
- •19.3.2. Гидроксикарбоновые кислоты
- •19.3.3. Оксокарбоновые кислоты
- •19.3.4. Ненасыщенные карбоновые кислоты
- •19.4. Основные реакции метаболизма карбоновых кислот
- •19.4.1. Биосинтез жирных кислот
- •1 9.4.2. Биологическое окисление жирных кислот
- •19.4.3. Реакции цикла кребса
- •19.5. Кислоты ароматического ряда и их производные как лекарственные средства
- •Г лава 20 Липиды
- •20.1. Жиры и воски
- •20.2. Омыляемые сложные липиды
- •20.3. Неомыляемые липиды - низкомолекулярные биорегуляторы
- •Глава 21 аминокислоты, пептиды и белки
- •21.1. Строение, классификация и физико-химические свойства а-аминокислот
- •21.2. Химические свойства а-аминокислот
- •21.2.1. Кислотно-основные свойства и прототропная таутомерия
- •21.2.2. К0мплекс00бразующие свойства
- •21.2.3. Электрофильно-нуклеофильные свойства
- •21.2.4. Окислительно-восстановительные свойства
- •21.3. Структура и свойства пептидов
- •21.4. Структура и свойства белков
- •Глава 22 углеводы и полисахариды
- •22.1. Строение, изомерия и свойства моносахаридов
- •22.1.1. Химические свойства моносахаридов и их производных
- •22.1.2. Катаболизм глюкозы - гликолиз
- •22.3. Полисахариды, их структура и свойства
- •22.3.1. Гомополисахариды
- •22.3.2. Гетерополисахариды, протеогликаны, гликопротеины
- •Г лава 23 биологически важные азотсодержащие соединения
- •23.1. Электронные состояния атома азота в его соединениях и свойства этих соединений
- •23.2. Роль аммиака для живых организмов и пути его обезвреживания. Цикл мочевины и ее свойства
- •23.3. Азотсодержащие ароматические гетероциклические соединения
- •23.4. Нуклеозиды, нуклеотиды и нуклеиновые кислоты, их структура и свойства
- •Г лава 24 электрохимия. Электрическая проводимость растворов электролитов
- •24.1. Электрическая подвижность ионов в растворе
- •24.2. Удельная электрическая проводимость растворов электролитов
- •24.3. Молярная электрическая проводимость растворов электролитов
- •24.4. Закон независимого движения ионов в разбавленных растворах (закон кольрауша)
- •24.5. Кондуктометрические методы анализа
- •24.5.1. Кондуктометрическое титрование
- •24.6. Электрическая проводимость биологических объектов в норме и патологии
- •Г лава 25 межфазные электрические потенциалы, гальванические цепи, потенциометрия
- •25.1. Возникновение двойного электрического слоя и виды электрических потенциалов
- •25.2. Электродный потенциал. Стандартный водородный электрод. Гальванические цепи. Уравнение нернста
- •25.3. Восстановительный потенциал
- •25.4. Диффузионный потенциал
- •25.5. Мембранный потенциал
- •25.6. Потенциометрия
- •25.6.1. Хлорсеребряный электрод сравнения
- •25.6.2. Ионо- и молекулярноселективные электроды определения
- •25.6.3. Потенциометрическое титрование
- •Глава 26 физико-химические основы поверхностных явлений
- •26.1. Свободная поверхностная энергия
- •26.2. Сорбция и ее виды
- •26.3. Абсорбция
- •26.4. Адсорбция
- •26.4.1. Адсорбция на неподвижной поверхности раздела фаз
- •26.4.2. Молекулярная адсорбция из растворов на твердых адсорбентах
- •26.4.3. Адсорбция ионов из растворов
- •26.4.4. Ионообменная адсорбция
- •26.5. Адсорбция на подвижной поверхности раздела фаз
- •26.6. Поверхностно-активные вещества
- •26.7. Хроматография
- •Глава 27 физикохимия дисперсных систем
- •27.2. Лиофобные коллоидные растворы
- •27.2.1. Строение мицелл в лиофобных коллоидных растворах
- •27.2.2. Свойства лиофобных коллоидных растворов
- •27.2.3. Влияние высокомолекулярных соединений на устойчивость лиофобных коллоидов. Флокуляция
- •27.3. Лиофильные коллоидные растворы
- •27.3.1. Строение мицелл пав и вмс в водных коллоидных растворах в зависимости от их концентрации
- •27. 3. 2. Получение и свойства лиофильных коллоидных растворов
- •27.3.3. Моющее действие растворов пав
- •27.3.4. Особенности растворов биополимеров
- •27.4. Структурообразование в растворах вмс. Возникновение связнодисперсных систем и их свойства
- •27.5. Грубодисперсные системы
- •27.5.1. Суспензии
- •27.5.2. Эмульсии
- •27.5.3. Аэрозоли
- •27.6. Электрокинетические явления в дисперсных системах
- •27.7. Ткани организма - дисперсные системы
- •27.7.1. Строение и свойства межклеточных мембран
- •27.7.2. Кровь - сложная дисперсная система
- •Приложение 1 применение осмолярной и осмоляльной концентраций в практической медицине
10.4. Медико-биологическая роль комплексных соединений
Многие вещества, присутствующие в организме: аминокислоты, белки, нуклеиновые кислоты и их основания, витамины, гормоны, порфирины, - являются активными лигандами и, взаимодействуя с катионами биометаллов, образуют многообразные комплексные соединения, выполняющие определенные биологические функции. Ряд ферментов в составе своих активных центров содержат катионы металлов, что обеспечивает строгое пространственное расположение функциональных групп фермента.
Некоторые природные прочные комплексные соединения содержат в качестве хелатообразующего лиганда порфириновые производные (разд. 10.1), в которых за счет электронодонорных свойств четырех атомов азота образуются четыре связи с комплексообразователем. В зависимости от природы комплексообразователя изменяются биологические функции этих комплексов. Так, комплексы порфирина с катионом железа являются основой гемоглобина и цитохромов, с катионом магния - хлорофилла, а с катионами двух металлов: железа и меди - цито хромоксидазы. Рассмотрим особенности строения гемоглобина миоглобина и метгемоглобина.
Комплексообразователем в гемоглобине и миоглобине является ион Fe2+, который, предоставляя шесть свободных атомных орбиталей, образует шесть связей по донорно-акцепторному механизму. Из них четырьмя связями ион железа связан с атомами азота порфиринового лиганда, образуя гем, пятая связь занята лигандом глобином (белок), а шестая — молекулой воды — лигандом, который связан с комплексообразователем лабильно:
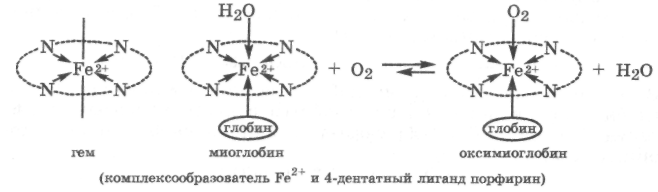
Миоглобин связывает часть кислорода, поступающего в ткани, путем замещения молекулы воды во внутренней сфере на молекулу кислорода, образуя оксимиоглобин, который достаточно прочно удерживает кислород. Это позволяет тканям запасать кислород для его использования в случаях острой кислородной недостаточности. Необходимо обратить внимание на то, что кислород не окисляет комплексообразователь Fe2+ в геме миоглобина.
Г![]() емоглобин
содержится в эритроцитах крови. Его
молекула состоит из четырех гемов,
аналогичных по строению гему миоглобина,
которые объединены четырьмя глобиновыми
цепями. В молекуле гемоглобина (ННb)
различают четыре фрагмента а1
а2
, B1,
B2,
каждый из которых способен к замещению
молекулы воды (лабильного лиганда) на
молекулу 02.
Находясь в легких, гемоглобин присоединяет
в результате лигандообменной реакции
вместо молекул воды молекулы кислорода,
образуя оксигемоглобин
(ННb02),
в котором катион железа сохраняет свой
заряд +2:
емоглобин
содержится в эритроцитах крови. Его
молекула состоит из четырех гемов,
аналогичных по строению гему миоглобина,
которые объединены четырьмя глобиновыми
цепями. В молекуле гемоглобина (ННb)
различают четыре фрагмента а1
а2
, B1,
B2,
каждый из которых способен к замещению
молекулы воды (лабильного лиганда) на
молекулу 02.
Находясь в легких, гемоглобин присоединяет
в результате лигандообменной реакции
вместо молекул воды молекулы кислорода,
образуя оксигемоглобин
(ННb02),
в котором катион железа сохраняет свой
заряд +2:
Таким образом, связывание гемоглобином кислорода является реакцией обмена лиганда, при которой нет окислительно-восстановительных превращений. Поэтому нет никаких оснований называть оксигемоглобин окисленной формой, а гемоглобин — восстановленной формой, что, к сожалению, имеет место даже в современной литературе и учебниках. Кроме этих неудачных терминов используется еще ненужный термин "дезокси-гемоглобин", который означает оксигемоглобин, отдавший кислород, а в действительности это просто гемоглобин.
Оксигемоглобин выполняет функцию транспорта кислорода у высших животных. Благодаря оксигемоглобину литр крови переносит 250 мл кислорода в капилляры различных органов. Здесь оксигемоглобин отдает кислород (разд. 8.5), который диффундирует через плазму и стенки капилляров в ткани. Часть поступившего кислорода соединяется с миоглобином для поддержания необходимого парциального давления кислорода в тканях. Основная часть кислорода вступает в процессы метаболизма, превращаясь в конце концов в оксид углерода(4) и воду, которые с помощью венозной крови выводятся из организма (разд. 8.5).
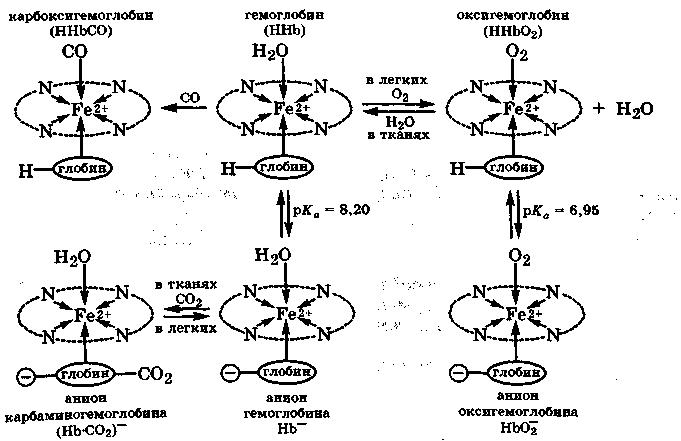
Венозная кровь поглощает С02 из тканей и транспортирует его в легкие на 80 % в виде НСО3(-), 15 % в виде аниона карбамино-гемоглобина (НbСО2)- и 5 % в растворенном виде (С02 * mН2О). В легких, вследствие избытка кислорода, кровь освобождается от СО2 (который далее удаляется при выдохе), а гемоглобин опять насыщается кислородом (разд. 8.5). Гемоглобин и оксигемоглобин являются слабыми кислотами и в крови (рН = 7,40) находятся частично в ионизированном состоянии: Hb- - 12 % и HbO2(-) - 66 %. В приведенной ниже схеме химических превращений гемоглобина с целью упрощения вместо сложной молекулы, состоящей из 4 подобных фрагментов, дается только один:
П![]() ри
вдыхании воздуха, содержащего оксид
углерода(П) ("угарный газ"),
последний взаимодействует с гемоглобином
и окси-гемоглобином с образованием
более устойчивого комплекса
кар-боксигемоглобина
ННbСО:
ри
вдыхании воздуха, содержащего оксид
углерода(П) ("угарный газ"),
последний взаимодействует с гемоглобином
и окси-гемоглобином с образованием
более устойчивого комплекса
кар-боксигемоглобина
ННbСО:
Эти равновесия смещены в сторону образования карбоксигемоглобина, устойчивость которого в 210 раз больше, чем оксигемоглобина, что приводит к накоплению карбоксигемоглобина в крови. В результате кислородная емкость крови уменьшается пропорционально количеству поступившего в организм СО. Серьезной причиной отравления оксидом углерода(П) является курение. Содержание карбоксигемоглобина в крови курильщиков, выкуривающих пачку сигарет в день, составляет в среднем 4,7 %, а у некурящих - всего 0,3-0,5 % (от содержания гемоглобина). Причиной более сильного отравления оксидом углерода(П) может быть преждевременное закрытие вытяжной заслонки протопленной печи или вдыхание выхлопных газов автомобиля. При легких отравлениях (содержание ННbСО в крови 10-15 %) наблюдается головная боль, слабость, тошнота. При отравлениях средней степени (ННЬСО в крови 25-30 %) нарушается координация движений, появляется синюшность кожи лица и помутнение сознания. При тяжелых отравлениях (ННЬСО в крови 60 % и более) происходит потеря сознания, судороги. Смерть наступает от остановки дыхания. Смертельные концентрации СО составляют 2 мг/л при 60-минутной и 5 мг/л при 5-минутной экспозиции. Пострадавшим необходимо тепло, сердечные средства и вдыхание чистого кислорода, так как содержание кислорода в воздухе недостаточно для быстрого вытеснения СО из карбоксигемоглобина.
Под действием окислителей: нитритов, нитратов, NO2, Н2О2, О3 - гемоглобин в результате окисления Fe2+ в Fe3+ и отрыва катионов от воды-лиганда превращается в метгемоглобин (метННb):
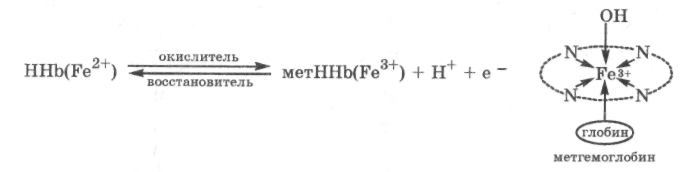
Метгемоглобин не способен переносить кислород, поэтому появление его в крови уменьшает кислородную емкость крови. Для его превращения в гемоглобин необходимо воздействие восстановителей.
Токсическое действие нитратов связано с рядом их химических превращений. Попадая в организм, нитраты легко восстанавливаются до нитритов:
![]()
Н![]() итриты
чрезвычайно эффективно окисляют
гемоглобин в метгемоглобин по
радикальному механизму, образуя оксид
азота(П) и способствуя образованию
различных активных форм кислорода
(разд. 9.3.9).
итриты
чрезвычайно эффективно окисляют
гемоглобин в метгемоглобин по
радикальному механизму, образуя оксид
азота(П) и способствуя образованию
различных активных форм кислорода
(разд. 9.3.9).
Оксид азота(П), подобно СО, образует прочный комплекс с гемоглобином - нитрозогемоглобин:
![]()
В результате воздействия нитратов возникает острое кислородное голодание тканей из-за уменьшения содержания гемоглобина в крови. Кроме того, нитраты и нитриты интенсифицируют свободнорадикальное окисление в организме, что дополнительно повышает их токсичность.
Таким образом, химия гемоглобина включает все три типа свойств: комплексообразующие, кислотно-основные и окислительно-восстановительные.
Цитохромы
- ферменты класса оксидоредуктаз,
содержащие в качестве комплексообразователя
катион железа или меди, а в качестве
лигандов - 4-дентатный порфирин, а также
белок, который занимает пятое и шестое
положения во внутренней сфере. Эти
изменения в составе приводят к новой
биологической функции комплекса,
которая заключается в переносе электрона
за счет обратимого изменения степени
окисления комплексообразователя:![]() ,
а в цитохромоксидазе еще и атома
меди:
,
а в цитохромоксидазе еще и атома
меди:![]() Цитохромы
обеспечивают работу электронотранспортных
цепей при окислительном фосфорилировании,
фотофосфорилировании, работе ансамбля
ферментов цито-хрома Р-450 (разд.
9.3.4-9.3.8).
Цитохромы
обеспечивают работу электронотранспортных
цепей при окислительном фосфорилировании,
фотофосфорилировании, работе ансамбля
ферментов цито-хрома Р-450 (разд.
9.3.4-9.3.8).
Цианиды при попадании в организм быстро проникают в кровь. Ион CN- с гемоглобином взаимодействует слабо, но чрезвычайно эффективно связывается окисленной формой цитохромоксидазы, блокируя в ней оба комплексообразователя (Fe3+ и Си2+), тем самым ингибируя ее действие в дыхательной цепи. Цианид-ион включается во внутреннюю сферу полиядерного комплекса цитохромоксидазы по месту разрыва связи белок - комплексообразователи:
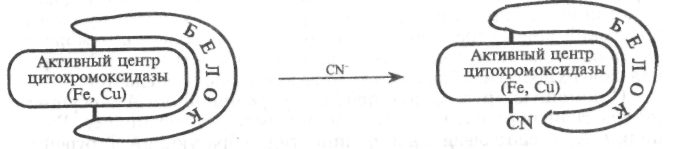
Клеточное дыхание прекращается на самом главном этапе - этапе усвоения кислорода клетками во всех тканях организма, особенно в нервных клетках мозга, где этот процесс идет интенсивно. При этом не нарушаются ни поступление кислорода в кровь, ни перенос его гемоглобином к тканям. Артериальная кровь переходит в вены, оставаясь насыщенной кислородом, что внешне проявляется в ярко-розовой окраске кожных покровов при поражении цианидами. Пероральная токсическая доза цианид-иона для человека LD50 = 1мг/кг.
От действия цианидов может защитить метгемоглобин крови, который благодаря наличию Fe3+ эффективно свяжет этот токсикант еще на пути к цитохромоксидазе с образованием очень прочного цианметгемоглобина:
![]()
При достаточно высокой концентрации метгемоглобина в крови в реакцию с ним вступит не только CN-, содержащийся в крови, но и CN-, уже связанный с цитохромоксидазой, в итоге ее активность будет восстановлена. Поэтому при отравлении цианидами рекомендуется вводить подкожно или внутривенно метгемоглобинообразователи, например NaN02, но осторожно, не допуская превращения гемоглобина в метгемоглобин более чем на 30 %. В противном случае могут наблюдаться явления, сходные с картиной отравления оксидом углерода(П). Другой способ защиты от цианидов заключается в использовании соединений-антидотов, легко реагирующих с CN-с образованием неядовитых продуктов, например роданидов (разд. 12.2.6).
Среди природных комплексных соединений особое место занимают макрокомплексы на основе циклических полипептидов, содержащих внутренние полости определенных размеров, в которых находятся несколько кислородсодержащих групп, способных за счет донорно-акцепторного взаимодействия связывать катионы тех металлов (включая катионы Na+ и К+), размеры которых соответствуют размерам полости. Такие комплексы, находясь в биологических мембранах, обеспечивают транспорт ионов через мембраны и поэтому называются ионофорами. В ионофоре катион комплексообразователя изолирован от окружающей среды гидрофобной оболочкой лиганда, за счет которой ион может свободно плавать в гидрофобном слое клеточной мембраны. Такими свойствами обладает циклический пептид валиномицил (антибиотик), полость которого соответствует размеру катиона К+. Поэтому с помощью ва-линомицина катионы К+ транспортируются через мембрану из зоны с высокой концентрацией К+ (внутренняя поверхность мембраны), где образуется комплекс, в зону низкой концентрации К+ (наружная поверхность мембраны), где этот комплекс распадается.
С помощью другого полипептида - грамицидина А - осуществляется транспорт катионов Na+ по эстафетному механизму. Грамицидин А - спиралевидный полипептид, образующий "трубочку", внутренняя поверхность которой выстлана кислородсодержащими группами. В результате получается достаточно большой длины гидрофильный канал с определенным сечением, соответствующим размеру иона натрия. Внешняя гидрофобная поверхность "трубочки" позволяет ей располагаться поперек фосфолипидного бислоя мембраны, полностью сливаясь с ним. Ион натрия, входя в гидрофильный канал с одной стороны, передается кислородными группировками от одной к другой подобно эстафете. В этом случае получается ионпроводящий канал. Таким об разом, за счет лабильного комплексообразования в ионофорах осуществляется транспорт ионов сквозь клеточные мембраны.
