
- •Оглавление
- •Глава 1 16
- •Глава 2 химическая связь 33
- •Глава 3 54
- •Глава 4 82
- •Глава 5 110
- •Глава 6 141
- •Глава 7 173
- •Глава 8 196
- •Глава 9 234
- •Глава 10 комплексные соединения и их свойства 272
- •Глава 11 297
- •Глава 12 316
- •Глава 13 377
- •Глава 14 400
- •Глава 15 основные понятия органической химии 419
- •Глава 16 445
- •Глава 17 474
- •Глава 18 499
- •Глава 19 518
- •Глава 20 562
- •Глава 21 аминокислоты, пептиды и белки 578
- •Глава 22 620
- •Глава 23 651
- •Глава 24 692
- •Глава 25 709
- •Глава 26 740
- •Глава 27 771
- •От автора
- •Глава 1 строение атома, периодический закон и периодическая система элементов д. И. Менделеева
- •1.1. Строение атома
- •1.1.1. Квантовые числа
- •1.1.2. Принципы заполнения атомных орбиталей электронами
- •1.2. Периодический закон и периодическая система элементов д. И. Менделеева
- •1.3. Основные характеристики атомов элементов
- •1.3.1. Радиус атома
- •1.3.2. Энергия ионизации
- •1.3.3. Энергия сродства к электрону
- •1.3.4. Относительная электроотрицательность
- •Глава 2 химическая связь
- •2.1. Ковалентная связь
- •2.1.1. И молекулярные орбитали
- •2.1.2. Механизмы возникновения ковалентной связи
- •2.1.3. Особенности ковалентной связи
- •2.2. Ионная связь
- •2.3. Металлическая связь
- •Глава 3 межмолекулярные взаимодействия и агрегатное состояние вещества
- •3.1. Межмолекулярные взаимодействия
- •3.2. Агрегатное состояние вещества
- •3.2.1. Твердое состояние
- •3.2.2. Жидкое состояние
- •3.2.3. Жидкокристаллическое состояние
- •3.2.4. Паро- и газообразное состояния
- •Глава 4 основы химической термодинамики и биоэнергетики
- •4.1. Основные понятия термодинамики
- •4.2. Первый закон термодинамики
- •4.3. Понятие о самопроизвольных процессах.
- •4.4. Второй закон термодинамики. Энергия гиббса
- •4.5. Принцип энергетического сопряжения биохимических реакций
- •Г лава 5 основы кинетики биохимических реакций и химического равновесия
- •5.1. Основные понятия и терминология раздела
- •5.2. Факторы, влияющие на скорость гомогенных реакций
- •5.2.1. Влияние природы реагирующих веществ
- •5.2.2. Влияние концентрации реагентов.
- •5.2.3. Влияние температуры. Энергия активации
- •5.2.4. Влияние катализатора
- •5.3. Особенности кинетики гетерогенных реакций
- •5.4. Особенности кинетики цепных реакций
- •5.5. Химическое равновесие
- •5.5.1. Смещение химического равновесия
- •5.6. Ферментативный катализ и его особенности
- •5.7. Автоколебательные биохимические процессы
- •Г лава 6 растворы и их коллигативные свойства
- •6.1. Вода как растворитель и ее роль в жизнедеятельности организма
- •6.2. Термодинамика процесса растворения
- •6.З. Способы выражения концентрации растворов
- •6.4. Коллигативные свойства растворов
- •6.4.1. Диффузия
- •6.4.2. Осмос. Осмотическое и онкотическое давление
- •6.4.3. Давление насыщенного пара над раствором
- •6.4.4. Температура кипения и замерзания раствора
- •Глава 7 растворы электролитов и ионные равновесия
- •7.1. Электролитическая диссоциация
- •7.2. Равновесие в растворах слабых электролитов
- •7.2.1. Влияние общего иона и противоиона на равновесие
- •7.2.2. Взаимосвязь константы диссоциации и степени диссоциации
- •7.3. Особенности растворов сильных электролитов. Ионная сила раствора
- •7.4. Электролитическая диссоциация и ионное произведение воды
- •7.5. Водородный и гидроксильный показатели (рН и рОн)
- •7.6. Физико-химические основы водно-электролитного баланса в организме
- •Г лава 8 теория кислот и оснований и протолитические равновесия
- •8.1. Протолитическая теория кислот и оснований
- •8.2. Кислотно-основные свойства а-аминокислот
- •8.3. Важнейшие кислотно-основные реакции
- •8.3.1. Гидролиз солей
- •8.3.2. Реакции нейтрализации
- •8.3.3. Общая, активная и потенциальная кислотность растворов
- •8.4. Протолитический баланс. Буферные растворы и их свойства
- •8.5. Буферные системы организма, их взаимодействие, явления ацидоза и алкалоза
- •9.1. Основные понятия и факторы, влияющие на протекание окислительно-восстановительных реакций
- •9.2. Направление протекания окислительно-восстановительных реакций
- •9.3. Особенности биохимических окислительно-восстановительных процессов в организмах
- •9.3.1. Степень окисления углерода в органических соединениях
- •9.3.2. Биохимические реакции внутри- и межмолекулярной окислительно-восстановительной дисмутации за счет атомов углерода
- •9.3.3. Окислительно-восстановительные превращения кофакторов и коферментов оксидоредуктаз
- •9.3.4. Электронотранспортные цепи
- •9.3.5. Дегидрогеназное окисление-восстановление
- •9.3.6. Окислительное фосфорилирование
- •9.3.7. Фотофосфорилирование
- •9.3.8. Оксигеназное окисление-восстановление
- •9.3.9. Свободнорадикальное окисление и антиоксидантная система организма
- •9.4. Использование окислителей и восстановителей в медико-санитарной практике
- •Глава 10 комплексные соединения и их свойства
- •10.1. Основные понятия и терминология
- •10.2. Химическая связь в комплексных соединениях и особенности их строения
- •10.3. Химические свойства комплексных соединений
- •10.4. Медико-биологическая роль комплексных соединений
- •10.5. Металлолигандный баланс и его нарушения
- •10.6. Комплексонометрия
- •Глава 11 гетерогенные процессы и равновесия в растворах
- •11.1. Основные понятия и теоретические основы
- •11.2. Гетерогенные равновесия в растворах, связанные с процессом кристаллизации
- •11.3. Гетерогенные равновесия в растворах, связанные с процессом расслоения
- •11.4. Гетерогенные равновесия в живых системах
- •Глава 12 химия элементов-органогенов
- •12.2. Строение, химические свойства и роль элементов-органогенов и их соединений в растительном и животном мире
- •12.2.1. Водород и его соединения
- •12.2.2. Углерод и его соединения
- •12.2.3. Азот и его соединения
- •12.2.4. Фосфор и его соединения
- •12.2.5. Кислород и его соединения
- •12.2.6. Сера и ее соединения
- •12.3. Строение и химические свойства галогенов и их соединений
- •Глава 13 химия ионов металлов жизни и их роль в растительном и животном мире
- •13.1. Химия ионов s-металлов в организме
- •13.1.1. Натрий и калий
- •13.1.2. Магний и кальций
- •13.2. Химия ионов d-металлов в организме
- •13.2.1. Марганец
- •13.2.2. Железо и кобальт
- •13.2.3. Медь
- •13.2.4. Цинк
- •13.2.5. Молибден
- •Глава 14 химия и анализ загрязнений окружающей среды
- •14.1. Химия загрязнений атмосферы
- •14.1.1. Токсический смог
- •14.1.2. Фотохимический смог
- •14.1.3. Кислотные дожди
- •14.1.4. Загрязнение атмосферы другими токсикантами
- •14.1.5. Разрушение озонового слоя
- •14.2. Методы анализа токсикантов и методы снижения их поступления в атмосферу
- •14.3. Загрязнение гидросферы. Понятие об общих показателях, характеризующих природные и сточные воды
- •Глава 15 основные понятия органической химии
- •15.1. Основы классификации и номенклатуры органических соединений
- •15.2. Пространственная структура биоорганических молекул и виды изомерии
- •15.3. Понятие о взаимном влиянии атомов в молекуле и электронные эффекты
- •15.4. Классификация органических реакций и их компонентов
- •Г лава 16 алифатические и ароматические углеводороды
- •16.1. Строение и реакционная способность алканов
- •16.2. Строение и реакционная способность ненасыщенных углеводородов: алкенов и диенов
- •16.3. Ароматические углеводороды (арены)
- •Глава 17 спирты, фенолы, простые эфиры, тиолы и сульфиды
- •17.2. Физико-химические свойства спиртов и фенолов
- •17.3. Химические свойства спиртов
- •17.4. Химические свойства фенолов
- •17.5. Простые эфиры
- •17.6. Тиолы и сульфиды
- •Г лава 18 альдегиды, кетоны и их производные
- •18.1. Строение, номенклатура и физико-химические свойства альдегидов и кетонов
- •18.2. Химические свойства альдегидов и кетонов
- •18.2.1. Кислотно-основные свойства
- •18.2.2. Электрофильно-нуклеофильные свойства
- •18.2.3. Окислительно-восстановительные свойства
- •18.2.4. Комплексообразующие свойства
- •18.3. Альдегиды и кетоны в окружающей среде
- •Г лава 19 карбоновые кислоты и их функциональные производные
- •19.2. Химические свойства предельных кислот и их производных
- •19.2.1. Кислотно-основные свойства
- •19.2.2. Карбоновые кислоты как ацилирующие реагенты
- •19.2.3. Производные карбоновых кислот, их свойства и взаимные превращения
- •19.2.4. Окислительно-восстановительные свойства карбоновых кислот и их производных
- •19.3. Особенности свойств замещенных карбоновых кислот и их производных
- •19.3.1. Дикарбоновые кислоты
- •19.3.2. Гидроксикарбоновые кислоты
- •19.3.3. Оксокарбоновые кислоты
- •19.3.4. Ненасыщенные карбоновые кислоты
- •19.4. Основные реакции метаболизма карбоновых кислот
- •19.4.1. Биосинтез жирных кислот
- •1 9.4.2. Биологическое окисление жирных кислот
- •19.4.3. Реакции цикла кребса
- •19.5. Кислоты ароматического ряда и их производные как лекарственные средства
- •Г лава 20 Липиды
- •20.1. Жиры и воски
- •20.2. Омыляемые сложные липиды
- •20.3. Неомыляемые липиды - низкомолекулярные биорегуляторы
- •Глава 21 аминокислоты, пептиды и белки
- •21.1. Строение, классификация и физико-химические свойства а-аминокислот
- •21.2. Химические свойства а-аминокислот
- •21.2.1. Кислотно-основные свойства и прототропная таутомерия
- •21.2.2. К0мплекс00бразующие свойства
- •21.2.3. Электрофильно-нуклеофильные свойства
- •21.2.4. Окислительно-восстановительные свойства
- •21.3. Структура и свойства пептидов
- •21.4. Структура и свойства белков
- •Глава 22 углеводы и полисахариды
- •22.1. Строение, изомерия и свойства моносахаридов
- •22.1.1. Химические свойства моносахаридов и их производных
- •22.1.2. Катаболизм глюкозы - гликолиз
- •22.3. Полисахариды, их структура и свойства
- •22.3.1. Гомополисахариды
- •22.3.2. Гетерополисахариды, протеогликаны, гликопротеины
- •Г лава 23 биологически важные азотсодержащие соединения
- •23.1. Электронные состояния атома азота в его соединениях и свойства этих соединений
- •23.2. Роль аммиака для живых организмов и пути его обезвреживания. Цикл мочевины и ее свойства
- •23.3. Азотсодержащие ароматические гетероциклические соединения
- •23.4. Нуклеозиды, нуклеотиды и нуклеиновые кислоты, их структура и свойства
- •Г лава 24 электрохимия. Электрическая проводимость растворов электролитов
- •24.1. Электрическая подвижность ионов в растворе
- •24.2. Удельная электрическая проводимость растворов электролитов
- •24.3. Молярная электрическая проводимость растворов электролитов
- •24.4. Закон независимого движения ионов в разбавленных растворах (закон кольрауша)
- •24.5. Кондуктометрические методы анализа
- •24.5.1. Кондуктометрическое титрование
- •24.6. Электрическая проводимость биологических объектов в норме и патологии
- •Г лава 25 межфазные электрические потенциалы, гальванические цепи, потенциометрия
- •25.1. Возникновение двойного электрического слоя и виды электрических потенциалов
- •25.2. Электродный потенциал. Стандартный водородный электрод. Гальванические цепи. Уравнение нернста
- •25.3. Восстановительный потенциал
- •25.4. Диффузионный потенциал
- •25.5. Мембранный потенциал
- •25.6. Потенциометрия
- •25.6.1. Хлорсеребряный электрод сравнения
- •25.6.2. Ионо- и молекулярноселективные электроды определения
- •25.6.3. Потенциометрическое титрование
- •Глава 26 физико-химические основы поверхностных явлений
- •26.1. Свободная поверхностная энергия
- •26.2. Сорбция и ее виды
- •26.3. Абсорбция
- •26.4. Адсорбция
- •26.4.1. Адсорбция на неподвижной поверхности раздела фаз
- •26.4.2. Молекулярная адсорбция из растворов на твердых адсорбентах
- •26.4.3. Адсорбция ионов из растворов
- •26.4.4. Ионообменная адсорбция
- •26.5. Адсорбция на подвижной поверхности раздела фаз
- •26.6. Поверхностно-активные вещества
- •26.7. Хроматография
- •Глава 27 физикохимия дисперсных систем
- •27.2. Лиофобные коллоидные растворы
- •27.2.1. Строение мицелл в лиофобных коллоидных растворах
- •27.2.2. Свойства лиофобных коллоидных растворов
- •27.2.3. Влияние высокомолекулярных соединений на устойчивость лиофобных коллоидов. Флокуляция
- •27.3. Лиофильные коллоидные растворы
- •27.3.1. Строение мицелл пав и вмс в водных коллоидных растворах в зависимости от их концентрации
- •27. 3. 2. Получение и свойства лиофильных коллоидных растворов
- •27.3.3. Моющее действие растворов пав
- •27.3.4. Особенности растворов биополимеров
- •27.4. Структурообразование в растворах вмс. Возникновение связнодисперсных систем и их свойства
- •27.5. Грубодисперсные системы
- •27.5.1. Суспензии
- •27.5.2. Эмульсии
- •27.5.3. Аэрозоли
- •27.6. Электрокинетические явления в дисперсных системах
- •27.7. Ткани организма - дисперсные системы
- •27.7.1. Строение и свойства межклеточных мембран
- •27.7.2. Кровь - сложная дисперсная система
- •Приложение 1 применение осмолярной и осмоляльной концентраций в практической медицине
8.3. Важнейшие кислотно-основные реакции
Протолитическая теория позволяет рассматривать с единой позиции не только ионизацию кислот и оснований, но и многие другие химические процессы, протекающие в водных системах живых организмов и окружающей среде. Прежде всего это относится к реакциям гидролиза солей и нейтрализации.
8.3.1. Гидролиз солей
При растворении некоторых солей в воде самопроизвольно протекают не только диссоциация их на ионы и гидратация ионов, но и процесс гидролиза солей.
Гидролиз солей - это протолитический процесс взаимодействия ионов солей с молекулами воды, в результате которого образуются малодиссоциирующие молекулы или ионы.
Способность ионов солей подвергаться гидролизу и его глубина зависят прежде всего от свойств ионов, образующих соль. Соли, образованные катионом сильного основания и анионом сильной кислоты, например NaCl, KN03, Na2S04, КСlO4, гидролизу не подвергаются, так как ни катион, ни анион этих солей не могут при взаимодействии с водой образовывать молекулы слабых электролитов. Поэтому в водных растворах этих солей величина рН практически не меняется и совпадает с рН воды при той же температуре, т. е. среда остается практически нейтральной.
Малорастворимые соли, например РЬС12, ВаСОз, из-за низкой концентрации ионов в водных растворах практически не гидролизуются.
Гидролизу подвергаются только те соли, которые содержат ионы, соответствующие слабым кислотам или слабым основаниям. С позиции протолитической теории гидролиз ионов солей заключается в переходе протона от молекулы воды к аниону соли или от катиона соли (с учетом его гидратации) к молекуле воды. Таким образом, в зависимости от природы иона вода выступает либо как кислота, либо как основание, а ионы соли при этом являются соответственно сопряженным основанием или сопряженной кислотой.
Возможны три варианта гидролиза ионов солей:
гидролиз по аниону - соли, содержащие катион сильного основания и анион слабой кислоты;
гидролиз по катиону - соли, содержащие катион слабого основания и анион сильной кислоты;
гидролиз и по катиону, и по аниону - соли, содержащие катион слабого основания и анион слабой кислоты.
Рассмотрим эти случаи гидролиза.
гидролиз по аниону. Соли, содержащие анионы слабых кислот, например ацетаты, цианиды, карбонаты, сульфиды, взаимодействуют с водой, так как эти анионы являются сопряженными основаниями, способными конкурировать с водой за протон, связывая его в слабую кислоту:
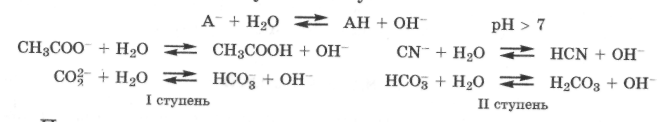
При этом взаимодействии возрастает концентрация ОН", и поэтому рН водных растворов солей, гидролизующихся по аниону, всегда находится в щелочной области (рН > 7). Гидролиз многозарядных анионов слабых кислот в основном протекает по I ступени.
Для характеристики состояния равновесия при гидролизе солей используют константу гидролиза Кг, которая при гидролизе по аниону равна:
![]()
где КH2O - ионное произведение воды (разд. 7.4); Ка — константа диссоциации слабой кислоты НА.
Из этого уравнения видно, что чем слабее кислота, тем полнее гидролиз.
Р![]() асчет
рН раствора соли, гидролизующейся по
аниону, проводят по формуле:
асчет
рН раствора соли, гидролизующейся по
аниону, проводят по формуле:
где с(А-) - концентрация аниона, численно равная или кратная концентрации соли.
В соответствии с принципом смещения химического равновесия для подавления гидролиза, протекающего по аниону, к раствору соли следует добавить щелочь как поставщик иона ОН~, образующегося при гидролизе соли по аниону (ион, одноименный продукту гидролиза).
Г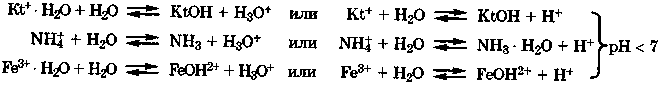 идролиз
по катиону. Соли,
содержащие катионы слабых оснований,
например катионы аммония, алюминия,
железа, цинка, взаимодействуют с водой,
так как являются сопряженными
кислотами, способными отдавать протон
молекулам воды или связывать ионы ОН-
молекул воды с образованием слабого
основания. При этом лучше учитывать,
что катионы металлов в водных растворах
гидратированы:
идролиз
по катиону. Соли,
содержащие катионы слабых оснований,
например катионы аммония, алюминия,
железа, цинка, взаимодействуют с водой,
так как являются сопряженными
кислотами, способными отдавать протон
молекулам воды или связывать ионы ОН-
молекул воды с образованием слабого
основания. При этом лучше учитывать,
что катионы металлов в водных растворах
гидратированы:
П![]() ри
гидролизе по катиону в растворе возрастает
концентрация Н+
и рН водного раствора таких солей всегда
находится в кислой области (рН < 7).
Константа гидролиза в этом случае
рассчитывается по формуле:
ри
гидролизе по катиону в растворе возрастает
концентрация Н+
и рН водного раствора таких солей всегда
находится в кислой области (рН < 7).
Константа гидролиза в этом случае
рассчитывается по формуле:
Равенство Кг соли, гидролизующейся по катиону, величине Ка(ВН+) следует из уравнения гидролиза по катиону, которое идентично уравнению диссоциации сопряженной кислоты слабого основания, содержащего данный катион, в присутствии воды.
Р![]() асчет
рН раствора соли, гидролизующейся по
катиону, проводят по уравнению
асчет
рН раствора соли, гидролизующейся по
катиону, проводят по уравнению
Если вместо показателя рКb использовать рКа(ВН+) сопряженной кислоты данного основания, то в этом случае, учитывая, что рКb = 14 - рКa(ВН+), получаем уравнение:
![]()
где c(Kt+) - концентрация катиона в растворе.
Для подавления гидролиза, протекающего по катиону, к раствору соли необходимо добавить сильную кислоту как поставщик иона Н+, одноименного продукту гидролиза.
Гидролиз по катиону и по аниону. В этом случае в реакции гидролитического взаимодействия с водой участвуют одновременно и катионы, и анионы, а реакция среды определяется природой более сильного протолита.
![]()
Если гидролиз по катиону и по аниону протекает в равной степени (кислота и основание - одинаково слабые электролиты), то раствор соли имеет нейтральную реакцию; например, водный раствор ацетата аммония NH4CH3COO имеет рН = 7, так как рKа(СН3СООН) = 4,76 и рKb(NH3* Н20) = 4,76.
Если в растворе преобладает гидролиз по катиону (основание слабее кислоты), раствор такой соли имеет слабокислую реакцию (рН < 7), например нитрит аммония NH4N02 (рKа(HN02) = 3,29).
Если в растворе преобладает гидролиз по аниону (кислота слабее основания), то раствор такой соли имеет слабощелочную реакцию (рН > 7), например цианид аммония NH4CN (рKа(HCN) = 9,31).
Константу гидролиза солей, гидролизующихся и по катиону, и по аниону, рассчитывают по формуле:
![]()
а![]() расчет рН раствора таких солей ведут
по формуле:
расчет рН раствора таких солей ведут
по формуле:
Следует отметить, что согласно последнему уравнению рН водных растворов солей, гидролизующихся и по катиону, и по аниону, не зависит от концентрации соли.
Н![]() екоторые
соли, гидролизующиеся по катиону и по
аниону, например сульфиды или карбонаты
алюминия, хрома, железа(Ш), гидролизуются
полностью и необратимо, так как при
взаимодействии их ионов с водой
образуются малорастворимые основания
и летучие кислоты, что способствует
протеканию реакции до конца:
екоторые
соли, гидролизующиеся по катиону и по
аниону, например сульфиды или карбонаты
алюминия, хрома, железа(Ш), гидролизуются
полностью и необратимо, так как при
взаимодействии их ионов с водой
образуются малорастворимые основания
и летучие кислоты, что способствует
протеканию реакции до конца:
Эту особенность гидролизаподобных солей следует обязательно учитывать при сливании сточных вод, чтобы избежать их вспенивания за счет образования С02 или отравления окружающей среды сероводородом.
Глубина протекания гидролиза солей в значительной степени зависит и от внешних факторов, в частности от температуры и концентрации раствора. При кипячении растворов гидролиз солей протекает значительно глубже, а охлаждение растворов, наоборот, уменьшает способность соли подвергаться гидролизу. Увеличение концентрации большинства солей в растворах также уменьшает гидролиз, а разбавление растворов заметно усиливает гидролиз солей.
Гидролитические процессы вместе с процессами растворения играют важную роль в обмене веществ. С ними связано поддержание на определенном уровне кислотности крови и других физиологических жидкостей. Действие многих химиотерапевтических средств связано с их кислотно-основными свойствами и склонностью к гидролизу. С этими свойствами необходимо считаться и при решении вопросов о допустимости одновременного назначения пациенту различных препаратов.
