
- •Оглавление
- •Глава 1 16
- •Глава 2 химическая связь 33
- •Глава 3 54
- •Глава 4 82
- •Глава 5 110
- •Глава 6 141
- •Глава 7 173
- •Глава 8 196
- •Глава 9 234
- •Глава 10 комплексные соединения и их свойства 272
- •Глава 11 297
- •Глава 12 316
- •Глава 13 377
- •Глава 14 400
- •Глава 15 основные понятия органической химии 419
- •Глава 16 445
- •Глава 17 474
- •Глава 18 499
- •Глава 19 518
- •Глава 20 562
- •Глава 21 аминокислоты, пептиды и белки 578
- •Глава 22 620
- •Глава 23 651
- •Глава 24 692
- •Глава 25 709
- •Глава 26 740
- •Глава 27 771
- •От автора
- •Глава 1 строение атома, периодический закон и периодическая система элементов д. И. Менделеева
- •1.1. Строение атома
- •1.1.1. Квантовые числа
- •1.1.2. Принципы заполнения атомных орбиталей электронами
- •1.2. Периодический закон и периодическая система элементов д. И. Менделеева
- •1.3. Основные характеристики атомов элементов
- •1.3.1. Радиус атома
- •1.3.2. Энергия ионизации
- •1.3.3. Энергия сродства к электрону
- •1.3.4. Относительная электроотрицательность
- •Глава 2 химическая связь
- •2.1. Ковалентная связь
- •2.1.1. И молекулярные орбитали
- •2.1.2. Механизмы возникновения ковалентной связи
- •2.1.3. Особенности ковалентной связи
- •2.2. Ионная связь
- •2.3. Металлическая связь
- •Глава 3 межмолекулярные взаимодействия и агрегатное состояние вещества
- •3.1. Межмолекулярные взаимодействия
- •3.2. Агрегатное состояние вещества
- •3.2.1. Твердое состояние
- •3.2.2. Жидкое состояние
- •3.2.3. Жидкокристаллическое состояние
- •3.2.4. Паро- и газообразное состояния
- •Глава 4 основы химической термодинамики и биоэнергетики
- •4.1. Основные понятия термодинамики
- •4.2. Первый закон термодинамики
- •4.3. Понятие о самопроизвольных процессах.
- •4.4. Второй закон термодинамики. Энергия гиббса
- •4.5. Принцип энергетического сопряжения биохимических реакций
- •Г лава 5 основы кинетики биохимических реакций и химического равновесия
- •5.1. Основные понятия и терминология раздела
- •5.2. Факторы, влияющие на скорость гомогенных реакций
- •5.2.1. Влияние природы реагирующих веществ
- •5.2.2. Влияние концентрации реагентов.
- •5.2.3. Влияние температуры. Энергия активации
- •5.2.4. Влияние катализатора
- •5.3. Особенности кинетики гетерогенных реакций
- •5.4. Особенности кинетики цепных реакций
- •5.5. Химическое равновесие
- •5.5.1. Смещение химического равновесия
- •5.6. Ферментативный катализ и его особенности
- •5.7. Автоколебательные биохимические процессы
- •Г лава 6 растворы и их коллигативные свойства
- •6.1. Вода как растворитель и ее роль в жизнедеятельности организма
- •6.2. Термодинамика процесса растворения
- •6.З. Способы выражения концентрации растворов
- •6.4. Коллигативные свойства растворов
- •6.4.1. Диффузия
- •6.4.2. Осмос. Осмотическое и онкотическое давление
- •6.4.3. Давление насыщенного пара над раствором
- •6.4.4. Температура кипения и замерзания раствора
- •Глава 7 растворы электролитов и ионные равновесия
- •7.1. Электролитическая диссоциация
- •7.2. Равновесие в растворах слабых электролитов
- •7.2.1. Влияние общего иона и противоиона на равновесие
- •7.2.2. Взаимосвязь константы диссоциации и степени диссоциации
- •7.3. Особенности растворов сильных электролитов. Ионная сила раствора
- •7.4. Электролитическая диссоциация и ионное произведение воды
- •7.5. Водородный и гидроксильный показатели (рН и рОн)
- •7.6. Физико-химические основы водно-электролитного баланса в организме
- •Г лава 8 теория кислот и оснований и протолитические равновесия
- •8.1. Протолитическая теория кислот и оснований
- •8.2. Кислотно-основные свойства а-аминокислот
- •8.3. Важнейшие кислотно-основные реакции
- •8.3.1. Гидролиз солей
- •8.3.2. Реакции нейтрализации
- •8.3.3. Общая, активная и потенциальная кислотность растворов
- •8.4. Протолитический баланс. Буферные растворы и их свойства
- •8.5. Буферные системы организма, их взаимодействие, явления ацидоза и алкалоза
- •9.1. Основные понятия и факторы, влияющие на протекание окислительно-восстановительных реакций
- •9.2. Направление протекания окислительно-восстановительных реакций
- •9.3. Особенности биохимических окислительно-восстановительных процессов в организмах
- •9.3.1. Степень окисления углерода в органических соединениях
- •9.3.2. Биохимические реакции внутри- и межмолекулярной окислительно-восстановительной дисмутации за счет атомов углерода
- •9.3.3. Окислительно-восстановительные превращения кофакторов и коферментов оксидоредуктаз
- •9.3.4. Электронотранспортные цепи
- •9.3.5. Дегидрогеназное окисление-восстановление
- •9.3.6. Окислительное фосфорилирование
- •9.3.7. Фотофосфорилирование
- •9.3.8. Оксигеназное окисление-восстановление
- •9.3.9. Свободнорадикальное окисление и антиоксидантная система организма
- •9.4. Использование окислителей и восстановителей в медико-санитарной практике
- •Глава 10 комплексные соединения и их свойства
- •10.1. Основные понятия и терминология
- •10.2. Химическая связь в комплексных соединениях и особенности их строения
- •10.3. Химические свойства комплексных соединений
- •10.4. Медико-биологическая роль комплексных соединений
- •10.5. Металлолигандный баланс и его нарушения
- •10.6. Комплексонометрия
- •Глава 11 гетерогенные процессы и равновесия в растворах
- •11.1. Основные понятия и теоретические основы
- •11.2. Гетерогенные равновесия в растворах, связанные с процессом кристаллизации
- •11.3. Гетерогенные равновесия в растворах, связанные с процессом расслоения
- •11.4. Гетерогенные равновесия в живых системах
- •Глава 12 химия элементов-органогенов
- •12.2. Строение, химические свойства и роль элементов-органогенов и их соединений в растительном и животном мире
- •12.2.1. Водород и его соединения
- •12.2.2. Углерод и его соединения
- •12.2.3. Азот и его соединения
- •12.2.4. Фосфор и его соединения
- •12.2.5. Кислород и его соединения
- •12.2.6. Сера и ее соединения
- •12.3. Строение и химические свойства галогенов и их соединений
- •Глава 13 химия ионов металлов жизни и их роль в растительном и животном мире
- •13.1. Химия ионов s-металлов в организме
- •13.1.1. Натрий и калий
- •13.1.2. Магний и кальций
- •13.2. Химия ионов d-металлов в организме
- •13.2.1. Марганец
- •13.2.2. Железо и кобальт
- •13.2.3. Медь
- •13.2.4. Цинк
- •13.2.5. Молибден
- •Глава 14 химия и анализ загрязнений окружающей среды
- •14.1. Химия загрязнений атмосферы
- •14.1.1. Токсический смог
- •14.1.2. Фотохимический смог
- •14.1.3. Кислотные дожди
- •14.1.4. Загрязнение атмосферы другими токсикантами
- •14.1.5. Разрушение озонового слоя
- •14.2. Методы анализа токсикантов и методы снижения их поступления в атмосферу
- •14.3. Загрязнение гидросферы. Понятие об общих показателях, характеризующих природные и сточные воды
- •Глава 15 основные понятия органической химии
- •15.1. Основы классификации и номенклатуры органических соединений
- •15.2. Пространственная структура биоорганических молекул и виды изомерии
- •15.3. Понятие о взаимном влиянии атомов в молекуле и электронные эффекты
- •15.4. Классификация органических реакций и их компонентов
- •Г лава 16 алифатические и ароматические углеводороды
- •16.1. Строение и реакционная способность алканов
- •16.2. Строение и реакционная способность ненасыщенных углеводородов: алкенов и диенов
- •16.3. Ароматические углеводороды (арены)
- •Глава 17 спирты, фенолы, простые эфиры, тиолы и сульфиды
- •17.2. Физико-химические свойства спиртов и фенолов
- •17.3. Химические свойства спиртов
- •17.4. Химические свойства фенолов
- •17.5. Простые эфиры
- •17.6. Тиолы и сульфиды
- •Г лава 18 альдегиды, кетоны и их производные
- •18.1. Строение, номенклатура и физико-химические свойства альдегидов и кетонов
- •18.2. Химические свойства альдегидов и кетонов
- •18.2.1. Кислотно-основные свойства
- •18.2.2. Электрофильно-нуклеофильные свойства
- •18.2.3. Окислительно-восстановительные свойства
- •18.2.4. Комплексообразующие свойства
- •18.3. Альдегиды и кетоны в окружающей среде
- •Г лава 19 карбоновые кислоты и их функциональные производные
- •19.2. Химические свойства предельных кислот и их производных
- •19.2.1. Кислотно-основные свойства
- •19.2.2. Карбоновые кислоты как ацилирующие реагенты
- •19.2.3. Производные карбоновых кислот, их свойства и взаимные превращения
- •19.2.4. Окислительно-восстановительные свойства карбоновых кислот и их производных
- •19.3. Особенности свойств замещенных карбоновых кислот и их производных
- •19.3.1. Дикарбоновые кислоты
- •19.3.2. Гидроксикарбоновые кислоты
- •19.3.3. Оксокарбоновые кислоты
- •19.3.4. Ненасыщенные карбоновые кислоты
- •19.4. Основные реакции метаболизма карбоновых кислот
- •19.4.1. Биосинтез жирных кислот
- •1 9.4.2. Биологическое окисление жирных кислот
- •19.4.3. Реакции цикла кребса
- •19.5. Кислоты ароматического ряда и их производные как лекарственные средства
- •Г лава 20 Липиды
- •20.1. Жиры и воски
- •20.2. Омыляемые сложные липиды
- •20.3. Неомыляемые липиды - низкомолекулярные биорегуляторы
- •Глава 21 аминокислоты, пептиды и белки
- •21.1. Строение, классификация и физико-химические свойства а-аминокислот
- •21.2. Химические свойства а-аминокислот
- •21.2.1. Кислотно-основные свойства и прототропная таутомерия
- •21.2.2. К0мплекс00бразующие свойства
- •21.2.3. Электрофильно-нуклеофильные свойства
- •21.2.4. Окислительно-восстановительные свойства
- •21.3. Структура и свойства пептидов
- •21.4. Структура и свойства белков
- •Глава 22 углеводы и полисахариды
- •22.1. Строение, изомерия и свойства моносахаридов
- •22.1.1. Химические свойства моносахаридов и их производных
- •22.1.2. Катаболизм глюкозы - гликолиз
- •22.3. Полисахариды, их структура и свойства
- •22.3.1. Гомополисахариды
- •22.3.2. Гетерополисахариды, протеогликаны, гликопротеины
- •Г лава 23 биологически важные азотсодержащие соединения
- •23.1. Электронные состояния атома азота в его соединениях и свойства этих соединений
- •23.2. Роль аммиака для живых организмов и пути его обезвреживания. Цикл мочевины и ее свойства
- •23.3. Азотсодержащие ароматические гетероциклические соединения
- •23.4. Нуклеозиды, нуклеотиды и нуклеиновые кислоты, их структура и свойства
- •Г лава 24 электрохимия. Электрическая проводимость растворов электролитов
- •24.1. Электрическая подвижность ионов в растворе
- •24.2. Удельная электрическая проводимость растворов электролитов
- •24.3. Молярная электрическая проводимость растворов электролитов
- •24.4. Закон независимого движения ионов в разбавленных растворах (закон кольрауша)
- •24.5. Кондуктометрические методы анализа
- •24.5.1. Кондуктометрическое титрование
- •24.6. Электрическая проводимость биологических объектов в норме и патологии
- •Г лава 25 межфазные электрические потенциалы, гальванические цепи, потенциометрия
- •25.1. Возникновение двойного электрического слоя и виды электрических потенциалов
- •25.2. Электродный потенциал. Стандартный водородный электрод. Гальванические цепи. Уравнение нернста
- •25.3. Восстановительный потенциал
- •25.4. Диффузионный потенциал
- •25.5. Мембранный потенциал
- •25.6. Потенциометрия
- •25.6.1. Хлорсеребряный электрод сравнения
- •25.6.2. Ионо- и молекулярноселективные электроды определения
- •25.6.3. Потенциометрическое титрование
- •Глава 26 физико-химические основы поверхностных явлений
- •26.1. Свободная поверхностная энергия
- •26.2. Сорбция и ее виды
- •26.3. Абсорбция
- •26.4. Адсорбция
- •26.4.1. Адсорбция на неподвижной поверхности раздела фаз
- •26.4.2. Молекулярная адсорбция из растворов на твердых адсорбентах
- •26.4.3. Адсорбция ионов из растворов
- •26.4.4. Ионообменная адсорбция
- •26.5. Адсорбция на подвижной поверхности раздела фаз
- •26.6. Поверхностно-активные вещества
- •26.7. Хроматография
- •Глава 27 физикохимия дисперсных систем
- •27.2. Лиофобные коллоидные растворы
- •27.2.1. Строение мицелл в лиофобных коллоидных растворах
- •27.2.2. Свойства лиофобных коллоидных растворов
- •27.2.3. Влияние высокомолекулярных соединений на устойчивость лиофобных коллоидов. Флокуляция
- •27.3. Лиофильные коллоидные растворы
- •27.3.1. Строение мицелл пав и вмс в водных коллоидных растворах в зависимости от их концентрации
- •27. 3. 2. Получение и свойства лиофильных коллоидных растворов
- •27.3.3. Моющее действие растворов пав
- •27.3.4. Особенности растворов биополимеров
- •27.4. Структурообразование в растворах вмс. Возникновение связнодисперсных систем и их свойства
- •27.5. Грубодисперсные системы
- •27.5.1. Суспензии
- •27.5.2. Эмульсии
- •27.5.3. Аэрозоли
- •27.6. Электрокинетические явления в дисперсных системах
- •27.7. Ткани организма - дисперсные системы
- •27.7.1. Строение и свойства межклеточных мембран
- •27.7.2. Кровь - сложная дисперсная система
- •Приложение 1 применение осмолярной и осмоляльной концентраций в практической медицине
3.2.3. Жидкокристаллическое состояние
Для кристаллического состояния характерны твердость и анизотропность свойств, а для жидкого состояния - текучесть и изотропность свойств. Обычно кристаллические вещества при нагревании до температуры плавления (Тпл) сразу переходят в одно родную прозрачную жидкость. Однако при плавлении некоторых кристаллических веществ при Tнач. пл образуется неоднородная (мутная) жидкость, которая обладает анизотропными свойствами. Только при повышении температуры до Тпросв (температуры просветления) эта жидкость становится полностью прозрачной и изотропной. Подобное поведение возможно для веществ, молекулы которых имеют сильно вытянутую (стержнеобразную) или дискообразную форму. Такие молекулы характеризуются сильно увеличенными размерами вдоль одной или двух осей соответственно и называются анизометрическими. Энергия межмолекулярных взаимодействий анизометрических молекул сильно зависит от взаимной ориентации соседних молекул.
Среди природных соединений сильно вытянутую форму имеют молекулы высших жирных кислот, фосфолипидов, гликолипидов, а дискообразную - молекулы стероидов, холестерина и желчных кислот. Для отдельных фрагментов молекул биополимеров: белков, нуклеиновых кислот и полисахаридов - также может быть характерна анизометричность. Анизометричность молекул перечисленных природных веществ, обусловленная их формой, усиливается при наличии в их структуре одновременно неполярных и полярных фрагментов. При плавлении веществ, молекулы которых анизометричны, при Тнач.пл. происходит частичное разрушение дальнего порядка в кристаллах, в результате возникает состояние, для которого одновременно свойственны и текучесть, и анизотропность свойств. Текучесть объясняется тем, что в системе, как в обычной жидкости, имеются отдельные частицы, мелкие ассоциаты из них и полости между ними, постоянно перемещающиеся и взаимодействующие между собой. Анизотропность свойств обусловлена наличием в системе более крупных ассоциатов, имеющих упорядоченность, близкую к кристаллической, и определенную взаимную ориентацию осей симметрии этих частиц, сохраняемую даже при перемещении их относительно друг друга. Подобная упорядоченность и согласованность в движении таких ассоциатов исчезает только при повышении температуры до Тпросв, когда крупные ассоциаты превращаются в мелкие и вещество переходит в истинно жидкое состояние с изотропными свойствами. Таким образом, в интервале температур от Tнач. пл до Tпросв вещества, молекулы которых анизометричны, находятся в состоянии, называемом жидкокристаллическим (рис. 3.5).
С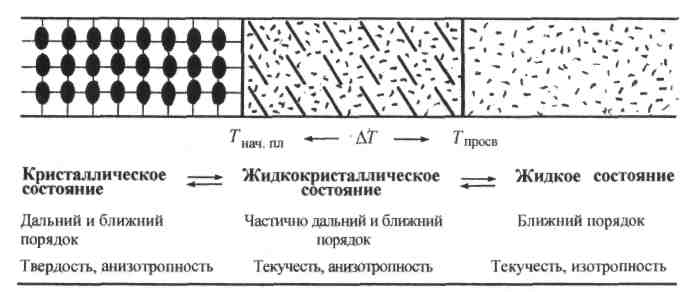 остояние
вещества, характеризующееся наличием
одновременно свойств и жидкости
(текучесть) и кристалла (анизотропность),
называется жидкокристаллическим
состоянием. С
позиции фазового состояния
жидкокристаллическое состояние
является мезофазой (или совокупностью
мезофаз), для которой характерна
определенная динамическая упорядоченность
анизометричных ассоциатов.
Жидкокристаллическое состояние
остояние
вещества, характеризующееся наличием
одновременно свойств и жидкости
(текучесть) и кристалла (анизотропность),
называется жидкокристаллическим
состоянием. С
позиции фазового состояния
жидкокристаллическое состояние
является мезофазой (или совокупностью
мезофаз), для которой характерна
определенная динамическая упорядоченность
анизометричных ассоциатов.
Жидкокристаллическое состояние
Рис. 3.5. Фазовые переходы и свойства конденсированных агрегатных состояний для веществ, молекулы которых анизометричны характеризуется упорядоченностью, промежуточной между кристаллом и жидкостью.
Ширина температурного интервала существования жидкокристаллического состояния T = Tпросв - Тнач. пл тем больше, чем сильнее различие в энергиях межмолекулярного взаимодействия у анизометричных молекул или анизометричных молекулярных ассоциатов вдоль их длинной оси и перпендикулярно к ней.
Достижение жидкокристаллического состояния у веществ за счет их плавления называют термотропией. В организме за счет термотропии поддерживается жидкокристаллическое состояние фосфолипидов, гликолипидов, холестерина в клеточных и внутриклеточных мембранах. В зависимости от типа упорядоченности анизометричных ассоциатов в мембранах реализуются разные мезофазы жидкокристаллического состояния, а переход между ними осуществляется при определенной температуре, называемой температурой фазового перехода (обычно второго рода), которую часто неправильно называют температурой плавления.
Получение
жидкокристаллического состояния путем
растворения веществ, молекулы которых
анизометричны и дифильны, т. е. содержат
и гидрофобный (неполярный) и гидрофильный
(полярный) фрагменты, называется
лиотропией.
Следовательно,
лиотропное жидкокристаллическое
состояние относится не к чистому
веществу, а к его коллоидному раствору,
т. е. к системе вещество
+ растворитель
![]() коллоидный
раствор. В
коллоидных растворах таких веществ
жидкокристаллическое состояние
возникает при концентрациях выше
пороговой, когда из этих веществ с
участием молекул растворителя образуются
подвижные ассоциаты, называемые мицеллами
(разд. 27.3). В крупных мицеллах имеется
ближний и частично дальний порядок, они
могут иметь анизометричную форму, и
тогда в движении мицелл относительно
друг друга из-за взаимодействия между
ними возможна определенная динамическая
упорядоченность в некотором
температурном интервале. Таким образом,
подобные коллоидные растворы находятся
в жидкокристаллическом состоянии,
так как обладают всеми характерными
признаками этого состояния. Это позволяет
считать, что жидкокристаллическое
состояние характерно для коллоидных
систем, в которых наблюдается
динамическая упорядоченность в движении
и расположении их анизометричных
мицелл.
коллоидный
раствор. В
коллоидных растворах таких веществ
жидкокристаллическое состояние
возникает при концентрациях выше
пороговой, когда из этих веществ с
участием молекул растворителя образуются
подвижные ассоциаты, называемые мицеллами
(разд. 27.3). В крупных мицеллах имеется
ближний и частично дальний порядок, они
могут иметь анизометричную форму, и
тогда в движении мицелл относительно
друг друга из-за взаимодействия между
ними возможна определенная динамическая
упорядоченность в некотором
температурном интервале. Таким образом,
подобные коллоидные растворы находятся
в жидкокристаллическом состоянии,
так как обладают всеми характерными
признаками этого состояния. Это позволяет
считать, что жидкокристаллическое
состояние характерно для коллоидных
систем, в которых наблюдается
динамическая упорядоченность в движении
и расположении их анизометричных
мицелл.
Третий путь образования жидкокристаллического состояния в системах, способных находиться в этом состоянии, заключается в индуцировании жидкокристаллического состояния под воздействием электрических, магнитных и акустических полей. За счет индуцирования в жидкокристаллических системах могут происходить полиморфные превращения, т. е. переход одной мезофазы в другую, отличающуюся динамической упорядоченностью анизотропных ассоциатов (табл. 3.3). Возможно, именно этот путь возникновения или изменения жидкокристаллического состояния в тканях нашего организма лежит в основе эффективности многих физиотерапевтических процедур, используемых в медицинской практике.
Свойства веществ, находящихся в жидкокристаллическом состоянии, зависят не только от обычных факторов (состава, структуры молекул и характера их взаимодействия), но и от взаимного расположения их ассоциатов относительно друг друга, от согласованности и динамики их движения. Последние факторы, обеспечиваемые только за счет слабых (0,5-4 кДж/моль) межмолекулярных взаимодействий между анизометричными ассоциатами, очень чувствительны к изменениям в значении и направлении оказываемого воздействия: изменениям температуры или давления, электрическим, магнитным и акустическим полям, т. е. к пространственным и временным градиентам соответствующих физических параметров. Это дает возможность даже при слабом внешнем воздействии температуры, давления, электрических, магнитных или других полей изменять упорядоченность в расположении и согласованность в движении частиц веществ, находящихся в жидкокристаллическом состоянии, что может вызывать изменение других свойств веществ - оптических, электрических, химических, а также их биологических или физиологических функций. Возможно, именно с этим связана большая чувствительность нашего организма к сквознякам и способность его к "закаливанию" при процедурах с контрастным температурным режимом.
Высокая лабильность оптических и электрических свойств веществ, находящихся в жидкокристаллическом состоянии, давно установлена и уже широко используется на практике. На основе веществ, способных образовывать жидкокристаллическое состояние (жидкие кристаллы) и изменять ориентацию частиц под действием электрического поля, в приборостроении созданы экраны для регистрации различной информации (в часах, измерительных приборах, карманных вычислительных машинах).
Производные холестерина, которые, находясь в жидкокристаллическом состоянии, изменяют свой цвет в зависимости от температуры, используют при термографическом изучении поверхности тела человека. Этот метод позволяет обнаружить тромбы в венах и артериях и злокачественные опухоли молочных желез за счет температурных различий между нормальным и патологическим состоянием соответствующего участка тела.
Природные соединения: высшие жирные кислоты, фосфолипиды, гликолипиды, стероиды, холестерин, желчные кислоты, белки, нуклеиновые кислоты и полисахариды, растворенные в воде или в биологических и физиологических средах, - могут находиться в жидкокристаллическом состоянии. С этим состоянием различных биосубстратов связаны важнейшие функции живого организма: движение, метаболизм, энергетический обмен и другие. Поэтому при описании свойств внутри- и межклеточных жидкостей, различных мембран и тканей (крови, головного и спинного мозга, мышц, кожи, сухожилий, хрящей) необходимо учитывать, что им могут быть присущи свойства жидкокристаллического состояния. Основу жидкокристаллического состояния различных биосубстратов в организме составляет подвижность их анизомет-ричных ассоциатов или отдельных групп и фрагментов в молекулах биополимеров. При этом для них возможен большой набор разных жидкокристаллических состояний, т. е. мезофаз, отличающихся по упорядоченности и динамичности их компонентов. Часть этих состояний (мезофаз) обеспечивает нормальные физиологические функции, а другие - вызывают патологию.
Жизнедеятельность высших живых существ, в том числе и человека, связана с постоянным изменением в определенных пределах упорядоченности и динамичности в тканях отдельных органов, т. е. с непрерывными фазовыми переходами второго рода, происходящими в данных тканях. Это проявляется в способности изменять температуру в отдельных тканях и вызывать в них состояние расслабленности или напряженности как рефлекторно, так и по желанию самого человека. Кроме того, поскольку большинство биосубстратов имеют заряды, то их жидкокристаллические состояния являются причиной возникновения электрических и электромагнитных полей в тканях, органах и у всего организма в целом. Причем характеристики этих полей как по величине, так и по направлению могут значительно изменяться во времени из-за специфики жидкокристаллического состояния. Вероятно, именно эта особенность живых организмов позволяет приписывать им особое поле -"биополе", которое в действительности является совокупностью тепловых, электрических, электромагнитных и акустических полей, характеристики которых, включая интенсивность, частоту, поляризацию и направление, изменяются во времени. Поэтому при исследовании этих особенностей живых систем необходимо использовать аппаратуру, содержащую источники и приемники поляризованных излучений, преимущественно слабой интенсивности (например, поляризационный микроскоп).
Поскольку для тканей организма характерно жидкокристаллическое состояние, то эта особенность лежит в основе их чувствительности к воздействию электрических, электромагнитных, магнитных и акустических полей, включая колебания обычного звукового диапазона, а также инфра- и ультразвука. Именно жидкокристаллическое состояние тканей живых организмов позволяет объяснить воздействие на них так называемых экстрасенсов. Эти люди, вероятно, способны вызывать, в большей мере, чем обычные люди, изменения в упорядоченности, согласованности и динамике движения компонентов жидкокристаллического состояния тканей своего организма и тем самым, с помощью совокупности соответствующих полей, индуцировать изменения в жидкокристаллическом состоянии тканей другого человека, а следовательно, влиять на их биологические и физиологические функции.
Живые объекты в значительной степени представляют собой сложные жидкокристаллические системы, которые характеризуются динамической упорядоченностью и чрезвычайно чувствительны к упорядоченности в расположении и движении частиц и воздействию различных физических полей как в самих системах, так и вне их. Это позволяет рассматривать живые организмы как приемники, чувствительные к изменениям упорядоченности движения материи в окружающем мире, и как источники, влияющие на нее. Подобная особенность живых объектов может позволить объяснить многие явления живого мира, включая загадочные.
