
- •Биохимия (часть 1)
- •060101.65 – Лечебное дело
- •060103.65 – Педиатрия
- •060105.65 – Стоматология
- •СОдержАние
- •Предмет биохимии
- •1. Химия белков
- •1.1. Методы выделения и очистки белков
- •1.2. Функции белков
- •1.3. Аминокислотный состав белков
- •5) Положительно заряженные
- •1.4. Структурная организация белков
- •Методы определения n-концевой аминокислоты
- •Методы определения с-концевой аминокислоты
- •1.5. Физико-химические свойства белков
- •1.6. Классификация белков
- •1.6.1. Простые белки
- •1. Альбумины и глобулины.
- •2. Протамины и гистоны.
- •3. Проламины и глютелины.
- •1.6.2. Сложные белки
- •Производные гемоглобина
- •Структура нуклеиновых кислот
- •Контрольные вопросы
- •2. Ферменты
- •2.1. Химическая природа ферментов
- •2.2. Механизм действия ферментов
- •2.3. Кинетика ферментативных реакций
- •2.4. Свойства ферментов
- •2.5. Регуляция активности ферментов
- •1. Контроль количества фермента.
- •2.1. Влияние на ферменты активаторов и ингибиторов.
- •2.2. Химическая модификация фермента.
- •2.3. Аллостерическая регуляция.
- •2.6. Классификация и номенклатура ферментов
- •2.7. Ферменты в медицине
- •2. Приобретенные энзимопатии.
- •Контрольные вопросы
- •3. Витамины
- •3.1. Жирорастворимые витамины
- •D2 (эргокальциферол) d3 (холекальциферол)
- •3.2. Водорастворимые витамины
- •Методы определения витаминов
- •Контрольные вопросы
- •4. Основные принципы организации биомембран
- •4.1. Строение и функции мембран
- •4.2. Транспорт веществ через мембрану
- •Контрольные вопросы
- •5. Механизмы передачи гормонального сигнала
- •Трансмембранная передача гормонального сигнала
- •Контрольные вопросы
- •6. Введение в метаболизм
- •6.1. Общая схема катаболизма
- •6.2. Биоэнергетика
- •6.3. Организация и функционирование дыхательной цепи
- •6.4. Разобщение окисления и фосфорилирования
- •6.5. Микросомальное окисление
- •6.6. Антиоксидантная система
- •6.7. Реакции общего пути катаболизма
- •6.7.1. Окислительное декарбоксилирование пвк
- •6.7.2. Цикл трикарбоновых кислот
- •Анаболические функции цикла Кребса
- •Контрольные вопросы
- •7. Обмен углеводов
- •7.1. Переваривание углеводов
- •7.2. Обмен гликогена
- •7.3. Гликолиз
- •7.4. Включение фруктозы и галактозы в гликолиз
- •7.5. Челночные механизмы
- •7.6. Цикл кори
- •7.7. Спиртовое брожение
- •7.8. Пентозофосфатный путь превращения глюкозы
- •7.9. Глюконеогенез
- •7.10. Регуляция обмена углеводов
- •7.11. Нарушения углеводного обмена Нарушение гидролиза и всасывания углеводов
- •Гликогенозы
- •Нарушения промежуточного обмена углеводов
- •Гипер- и гипогликемия
- •Глюкозурия
- •Контрольные вопросы
- •Литература
- •11. Харитонов, я.Ю. Аналитическая химия. Аналитика 2. Количественный анализ. Физико-химические (инструментальные) методы анализа. / я.Ю. Харитонов. – м.: геотар-Медиа, 2014. – 656 с.
7.2. Обмен гликогена
Гликоген – главный резервный гомолисахарид человека, мономером которого является глюкоза. Остатки глюкозы соединены в линейных участках -1,4-гликозидными связями, в местах разветвления - -1,6-гликозидными связями. Разветвленная структура гликогена создает много концевых мономеров, ускоряющих процессы его распада или синтеза. Гликоген депонируется в печени и скелетных мышцах и хранится в цитозоле в форме гранул. Метаболические пути синтеза и распада гликогена различны.
Синтез гликогена (гликогенез) происходит в течение 1-2 часов после приема углеводной пищи и требует затрат АТФ.
1). Фосфорилирование глюкозы при участии гексокиназы (в печени – глюкокиназы) с образованием глюкозо-6-фосфата, который переходит в глюкозо-1-фосфат (фермент – фосфоглюкомутаза):

2). При участии глюкозо-1-фосфат-уридилилтрансферазы глюкозо-1-фосфат, взаимодействуя с УТФ, образует УДФ-глюкозу и пирофосфат:
глюкозо-1-фосфат + УТФ УДФ-глюкоза + РРi.
3). Перенос глюкозного остатка, входящего в состав УДФ-глюкозы, на гликозидную цепь гликогена («затравочное» количество), фермент - гликогенсинтаза. Гликогенсинтаза катализирует образование -1,4-гликозидной связи. Активация гликогенсинтазы происходит при участии инсулина.

Образование -1,6-гликозидной связи обеспечивает гликогенветвящий фермент, который переносит олигосахаридный фрагмент (6-7 остатков глюкозы) на 6-гидроксильную группу остатка глюкозы той же или другой цепи гликогена.
Распад гликогена (гликогенолиз) – процесс перехода гликогена из запасной формы в метаболическую (глюкоза).
Под действием гликогенфосфорилазы гликоген распадается на глюкозо-1-фосфат без предварительного расщепления на фрагменты.
Фосфорилаза существует в двух формах – фосфорилаза а (активна, состоит из 4 субъежиниц) и фосфорилаза b (неактивна, состоит из 2 субъединиц). Превращение фосфорилазы а в фосфорилазу b осуществляется фосфорилированием белка киназой фосфорилазы:
2фосфорилаза b + 4АТФ → фосфорилаза а + 4АДФ.
Неактивная киназа фосфорилазы превращается в активную при участии фермента цАМФ-зависимой протеинкиназы. цАМФ образуется из АТФ под действием аденилатциклазы, активируемой адреналином и глюкагоном. В результате из гликогена образуется глюкозо-1-фосфат.
Глюкозо-1-фосфат под действием фосфоглюкомутазы превращается в глюкозо-6-фосфат.
В печени из глюкозо-6-фосфата путем гидролитического отщепления фосфата (фермент – глюкозо-6-фосфатаза) получается глюкоза. Т.о., печень участвует в поддержании постоянного уровня глюкозы в крови.
В клетках мышечной ткани отсутствует фермент глюкозо-6-фосфатаза. Образования глюкозы не происходит. Плазматическая мембрана непроницаема для глюкозо-6-фосфата, и он используется мышечной тканью.
7.3. Гликолиз
Гликолиз – последовательность ферментативных реакций, приводящих к расщеплению глюкозы с образованием ПВК, сопровождающихся образованием АТФ (в цитозоле клетки). Различают два вида гликолиза – аэробный и анаэробный.
Аэробный гликолиз: образуется ПВК, поступающая в митохондрии. В аэробных условиях ПВК далее, в общем пути катаболизма, распадается до СО2 и Н2О. Аэробный гликолиз – часть аэробного распада глюкозы.
Анаэробный гликолиз: образуется ПВК, которая затем превращается в лактат. Анаэробный распад глюкозы и анаэробный гликолиз – синонимы. Анаэробный гликолиз протекает в первые минуты мышечной работы, в эритроцитах (нет митохондрий), при недостаточном поступлении кислорода.
Реакции гликолиза:
1). Фосфорилирование глюкозы. Реакцию катализирует гексокиназа, в паренхиматозных клетках печени - глюкокиназа. Образование глюкозо-6-фосфата в клетке - ловушка для глюкозы, т.к. мембрана для фосфорилированной глюкозы непроницаема. Глюкозо-6-фосфат - аллостерический ингибитор реакции.
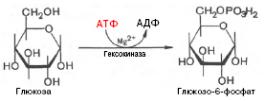
2). Реакция изомеризации при участии глюкозо-6-фосфатизомеразы:
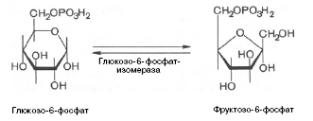
3) Лимитирующая стадия - реакция фосфорилирования, катализируемая 6-фосфофруктокиназой, которая ингибируется АТФ и цитратом, активируется - АМФ.
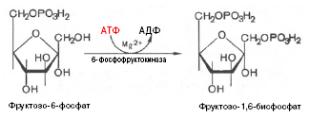
4). Реакция альдольного расщепления при участии альдолазы.

5). Изомеризация диоксиацетонфосфата, фермент – триозофосфатизомераза:

1 молекула глюкозы превращается в 2 молекулы глицеральдегид-3-фосфата (реакции 4, 5).
6). Реакция окисления, фермент - глицеральдегидфосфатдегидрогеназа:

7). Субстратное фосфорилирование при участии фосфоглицераткиназы:

8). Внутримолекулярный перенос фосфатной группы, фермент - фосфоглицеромутаза:

9). Реакция дегидратации при участии енолазы:

10). Субстратное фосфорилирование, фермент - пируваткиназа:

11). В анаэробных условиях протекает реакция восстановления пирувата в лактат под действием фермента лактатдегидрогеназы:

Суммарное уравнение анаэробного гликолиза:
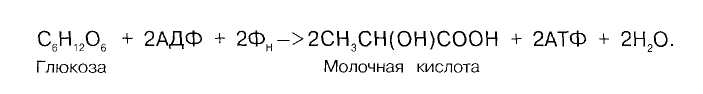
Анаэробный гликолиз не нуждается в дыхательной цепи.
Выход АТФ при анаэробном гликолизе: АТФ образуется за счет двух реакций субстратного фосфорилирования: из 1,3-бисфосфоглицерата – 7 реакция, и из фосфоенолпирувата – 10 реакция. Учитывая, что 1 молекула глюкозы расщепляется на 2 триозы и дает 2 молекулы глицеральдегидфосфата, образуется 4АТФ. 2АТФ расходуется на активацию глюкозы (реакции 1 и 3 гликолиза). Суммарно:
4АТФ - 2АТФ = 2АТФ.
Выход АТФ при аэробном распаде глюкозы: полный аэробный распад глюкозы включает аэробный гликолиз, продуктом которого является пируват, и реакции общего пути катаболизма.
В аэробном гликолизе за счет субстратного фосфорилирования образуется 2АТФ. Также на 1 молекулу глюкозы образуется 2НАДН+Н+, и в результате в дыхательной цепи синтезируется 2х3АТФ = 6АТФ.
Общий путь катаболизма на одну молекулу ПВК дает 15 АТФ, на 2 – 30.
Итого:
2АТФ +6АТФ + 30АТФ = 38АТФ.
