
- •Биохимия (часть 1)
- •060101.65 – Лечебное дело
- •060103.65 – Педиатрия
- •060105.65 – Стоматология
- •СОдержАние
- •Предмет биохимии
- •1. Химия белков
- •1.1. Методы выделения и очистки белков
- •1.2. Функции белков
- •1.3. Аминокислотный состав белков
- •5) Положительно заряженные
- •1.4. Структурная организация белков
- •Методы определения n-концевой аминокислоты
- •Методы определения с-концевой аминокислоты
- •1.5. Физико-химические свойства белков
- •1.6. Классификация белков
- •1.6.1. Простые белки
- •1. Альбумины и глобулины.
- •2. Протамины и гистоны.
- •3. Проламины и глютелины.
- •1.6.2. Сложные белки
- •Производные гемоглобина
- •Структура нуклеиновых кислот
- •Контрольные вопросы
- •2. Ферменты
- •2.1. Химическая природа ферментов
- •2.2. Механизм действия ферментов
- •2.3. Кинетика ферментативных реакций
- •2.4. Свойства ферментов
- •2.5. Регуляция активности ферментов
- •1. Контроль количества фермента.
- •2.1. Влияние на ферменты активаторов и ингибиторов.
- •2.2. Химическая модификация фермента.
- •2.3. Аллостерическая регуляция.
- •2.6. Классификация и номенклатура ферментов
- •2.7. Ферменты в медицине
- •2. Приобретенные энзимопатии.
- •Контрольные вопросы
- •3. Витамины
- •3.1. Жирорастворимые витамины
- •D2 (эргокальциферол) d3 (холекальциферол)
- •3.2. Водорастворимые витамины
- •Методы определения витаминов
- •Контрольные вопросы
- •4. Основные принципы организации биомембран
- •4.1. Строение и функции мембран
- •4.2. Транспорт веществ через мембрану
- •Контрольные вопросы
- •5. Механизмы передачи гормонального сигнала
- •Трансмембранная передача гормонального сигнала
- •Контрольные вопросы
- •6. Введение в метаболизм
- •6.1. Общая схема катаболизма
- •6.2. Биоэнергетика
- •6.3. Организация и функционирование дыхательной цепи
- •6.4. Разобщение окисления и фосфорилирования
- •6.5. Микросомальное окисление
- •6.6. Антиоксидантная система
- •6.7. Реакции общего пути катаболизма
- •6.7.1. Окислительное декарбоксилирование пвк
- •6.7.2. Цикл трикарбоновых кислот
- •Анаболические функции цикла Кребса
- •Контрольные вопросы
- •7. Обмен углеводов
- •7.1. Переваривание углеводов
- •7.2. Обмен гликогена
- •7.3. Гликолиз
- •7.4. Включение фруктозы и галактозы в гликолиз
- •7.5. Челночные механизмы
- •7.6. Цикл кори
- •7.7. Спиртовое брожение
- •7.8. Пентозофосфатный путь превращения глюкозы
- •7.9. Глюконеогенез
- •7.10. Регуляция обмена углеводов
- •7.11. Нарушения углеводного обмена Нарушение гидролиза и всасывания углеводов
- •Гликогенозы
- •Нарушения промежуточного обмена углеводов
- •Гипер- и гипогликемия
- •Глюкозурия
- •Контрольные вопросы
- •Литература
- •11. Харитонов, я.Ю. Аналитическая химия. Аналитика 2. Количественный анализ. Физико-химические (инструментальные) методы анализа. / я.Ю. Харитонов. – м.: геотар-Медиа, 2014. – 656 с.
6.4. Разобщение окисления и фосфорилирования
На всех этапах трансформации энергии пищевых веществ в энергию АТФ часть энергии рассеивается в форме теплоты. При использовании АТФ для совершения работы значительная часть энергии также превращается в теплоту. Однако существуют специальные механизмы, участвующие в поддержании температуры тела.
Разобщители - липофильные вещества, которые способны принимать протоны и переносить их через внутреннюю мембрану митохондрий, минуя ее протонный канал.
Разобщители бывают:
- естественные – продукты перекисного окисления липидов, жирных кислот с длинной цепью, большие дозы тиреоидных гормонов;
- искусственные - динитрофенол, эфир, производные витамина K, анестетики, антибиотики (грамицидин, валиномицин).
Рассмотрим механизм разобщения на примере 2,4-динитрофенола (рис. 35).
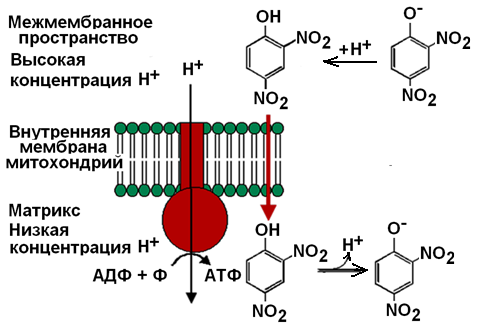
Рис. 35. Разобщение дыхания и фосфорилирования
Динитрофенол способен диффундировать через митохондриальную мембрану как в ионизированной, так и в неионизированной форме и может переносить ионы водорода через мембрану. Поэтому динитрофенол уничтожает ΔрН митохондриальной мембраны. Потребление кислорода и окисление субстратов при этом продолжаются, но синтез АТФ невозможен. Поскольку энергия окисления при разобщении рассеивается в форме теплоты, то разобщители повышают температуру тела (пирогенное действие).
Существует особая ткань, специализирующаяся на теплопродукции посредством разобщенного дыхания. Это бурый жир. Своим названием он обязан большому количеству митохондрий (они коричневого цвета). Около 10% всех белков этих митохондрий приходится на так называемый разобщающий белок. Бурый жир участвует в поддержании температуры тела. Островки бурой жировой ткани облегают крупные кровеносные сосуды, идущие к головному мозгу. Особенно много этой ткани у новорожденных. С возрастом ее количество уменьшается.
6.5. Микросомальное окисление
Биологическое окисление, не сопряженное с запасанием энергии, называется свободным (несопряженным) окислением. На его долю приходится 5-10% кислорода, поступающего в организм. Оно протекает вне митохондрий, чаще всего в эндоплазматическом ретикулуме, поэтому иногда этот процесс называют микросомальным окислением (микросомы – фрагменты ЭПС).
Одна из функций свободного окисления - превращение природных или неприродных субстратов, называемых ксенобиотиками
Свободное окисление проходит при участии оксигеназ. Оксигеназы - ферменты класса оксидоредуктаз; катализируют окисление субстратов путем включения в их молекулы одного атома кислорода (монооксигеназы) или двух атомов кислорода (диоксигеназы).
Оксигеназы работают в составе мультиферментного комплекса, встроенного в мембрану. Мультиферментный комплекс состоит из трех компонентов: флавиновые дегидрогеназы, железосерный белок, цитохром Р450.
Цитохром Р450 – семейство ферментов, относящихся к гемопротеинам. Система цитохрома P450 участвует в окислении как эндогенных (стероиды, желчные кислоты, ненасыщенные жирные кислоты), так и экзогенных веществ - ксенобиотиков («ксено» - несовместимый, «биос» - жизнь) - лекарств, ядов, наркотиков.
В реакциях свободного окисления участвуют также кислород и восстановленные дыхательные переносчики (чаще всего НАДФН). Акцептором электронов является цитохром Р450:
RH + O2 + НАДФН + Н+ ROH + НАДФ+ + Н2О.
Гироксилирование ксенобиотика делает его более растворимым, облегчает последующую деструкцию и выведение из организма.
Регуляция активности микросомальной системы осуществляется на уровне транскрипции или посттранскрипционных изменений. Индукция синтеза позволяет увеличить количество ферментов в ответ на поступление или образование в организме веществ, выведение которых невозможно без участия системы микросомального окисления.
