- •Биохимия (часть 1)
- •060101.65 – Лечебное дело
- •060103.65 – Педиатрия
- •060105.65 – Стоматология
- •СОдержАние
- •Предмет биохимии
- •1. Химия белков
- •1.1. Методы выделения и очистки белков
- •1.2. Функции белков
- •1.3. Аминокислотный состав белков
- •5) Положительно заряженные
- •1.4. Структурная организация белков
- •Методы определения n-концевой аминокислоты
- •Методы определения с-концевой аминокислоты
- •1.5. Физико-химические свойства белков
- •1.6. Классификация белков
- •1.6.1. Простые белки
- •1. Альбумины и глобулины.
- •2. Протамины и гистоны.
- •3. Проламины и глютелины.
- •1.6.2. Сложные белки
- •Производные гемоглобина
- •Структура нуклеиновых кислот
- •Контрольные вопросы
- •2. Ферменты
- •2.1. Химическая природа ферментов
- •2.2. Механизм действия ферментов
- •2.3. Кинетика ферментативных реакций
- •2.4. Свойства ферментов
- •2.5. Регуляция активности ферментов
- •1. Контроль количества фермента.
- •2.1. Влияние на ферменты активаторов и ингибиторов.
- •2.2. Химическая модификация фермента.
- •2.3. Аллостерическая регуляция.
- •2.6. Классификация и номенклатура ферментов
- •2.7. Ферменты в медицине
- •2. Приобретенные энзимопатии.
- •Контрольные вопросы
- •3. Витамины
- •3.1. Жирорастворимые витамины
- •D2 (эргокальциферол) d3 (холекальциферол)
- •3.2. Водорастворимые витамины
- •Методы определения витаминов
- •Контрольные вопросы
- •4. Основные принципы организации биомембран
- •4.1. Строение и функции мембран
- •4.2. Транспорт веществ через мембрану
- •Контрольные вопросы
- •5. Механизмы передачи гормонального сигнала
- •Трансмембранная передача гормонального сигнала
- •Контрольные вопросы
- •6. Введение в метаболизм
- •6.1. Общая схема катаболизма
- •6.2. Биоэнергетика
- •6.3. Организация и функционирование дыхательной цепи
- •6.4. Разобщение окисления и фосфорилирования
- •6.5. Микросомальное окисление
- •6.6. Антиоксидантная система
- •6.7. Реакции общего пути катаболизма
- •6.7.1. Окислительное декарбоксилирование пвк
- •6.7.2. Цикл трикарбоновых кислот
- •Анаболические функции цикла Кребса
- •Контрольные вопросы
- •7. Обмен углеводов
- •7.1. Переваривание углеводов
- •7.2. Обмен гликогена
- •7.3. Гликолиз
- •7.4. Включение фруктозы и галактозы в гликолиз
- •7.5. Челночные механизмы
- •7.6. Цикл кори
- •7.7. Спиртовое брожение
- •7.8. Пентозофосфатный путь превращения глюкозы
- •7.9. Глюконеогенез
- •7.10. Регуляция обмена углеводов
- •7.11. Нарушения углеводного обмена Нарушение гидролиза и всасывания углеводов
- •Гликогенозы
- •Нарушения промежуточного обмена углеводов
- •Гипер- и гипогликемия
- •Глюкозурия
- •Контрольные вопросы
- •Литература
- •11. Харитонов, я.Ю. Аналитическая химия. Аналитика 2. Количественный анализ. Физико-химические (инструментальные) методы анализа. / я.Ю. Харитонов. – м.: геотар-Медиа, 2014. – 656 с.
2.4. Свойства ферментов
Ферменты отличаются от обычных катализаторов рядом свойств.
Термолабильность, или чувствительность к повышению температуры (рис. 22).
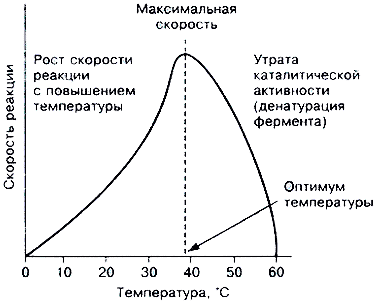
Рис. 22. Зависимость скорости ферментативной реакции от температуры
При температуре, не превышающей 45–50 °С, скорость большинства биохимических реакций повышается в 2 раза при повышении температуры на 10 °С согласно правилу Вант-Гоффа. При температуре выше 50 °С на скорость реакции влияниет тепловая денатурация белка-фермента, постепенно приводящая к его полной дезактивации.
Температура, при которой каталитическая активность фермента максимальна, называется его температурным оптимумом. Температурный оптимум для большинства ферментов млекопитающих лежит в пределах 37-40 °С. При низких температурах (0 °С и ниже) ферменты, как правило, не разрушаются, хотя активность их падает почти до нуля.
Зависимость активности фермента от значения рН среды (рис. 23).
Для каждого фермента существует оптимальное значение рН среды, при котором он проявляет максимальную активность. рН-оптимум действия ферментов животных тканей лежит в пределах узкой зоны концентрации водородных ионов, соответствующей выработанным в процессе эволюции физиологическим значениям рН среды 6,0-8,0. Исключения составляют пепсин – 1,5-2,5; аргиназа – 9,5-10.
|
Рис. 23. Зависимость скорости ферментативной реакции от рН среды
|
Влияние изменений рН среды на молекулу фермента заключается в воздействии на степень ионизации его активных групп, а, следовательно, на третичную структуру белка и состояние активного центра. рН меняет также ионизацию кофакторов, субстратов, фермент-субстратных комплексов и продуктов реакции.
Специфичность. Высокая специфичность действия ферментов обусловлена конформационной и электростатической комплементарностью между молекулами субстрата и фермента и уникальной структурной организацией активного центра, обеспечивающими избирательность протекания реакции.
Абсолютная специфичность – способность фермента катализировать единственную реакцию. Например, уреаза катализирует реакцию гидролиза мочевины до NH3 и СО2, аргиназа – гидролиз аргинина.
Относительная (групповая) специфичность – способность фермента катализировать группу реакций определенного типа. Относительной специфичностью, например, обладают гидролитические ферменты пептидазы, гидролизующие пептидные связи в молекулах белков и пептидов, липаза, гидролизующая сложноэфирные связи в молекулах жиров.
Стереохимической специфичностью обладают ферменты, катализирующие превращения только одного из пространственных изомеров. Фермент фумараза катализирует превращение транс-изомера бутендиовой кислоты - фумаровой кислоты в яблочную, и не действует на цис-изомер - малеиновую кислоту.
Высокая специфичность действия ферментов обеспечивает протекание лишь определенных химических реакций из всех возможных превращений.
2.5. Регуляция активности ферментов
Активность фермента определяют по скорости реакции, катализируемой ферментом, при стандартных условиях измерения (оптимальных условиях температуры, рН среды и полном насыщении фермента субстратом). О скорости ферментативной реакции судят или по скорости убыли субстрата, или по скорости образования продукта реакции.
Одна стандартная единица активности фермента (Е или U) - такое количество фермента, которое катализирует превращение 1 мкмоль вещества за 1 мин.
В связи с введением Международной системы единиц (СИ) предложено выражение активности фермента в каталах (кат, kat): 1 кат - каталитическая активность, способная осуществлять реакцию со скоростью, равной 1 моль/с. 1 U (международная единица) фермента составляет 16,67 нкат.
Удельная активность фермента - число единиц ферментативной активности на 1 мг белка (или число каталов на 1 кг активного белка).
Молярная активность равна числу единиц активности фермента, деленному на количество фермента, выраженное в микромоль. Она показывает, сколько молекул субстрата превращается одной молекулой фермента за 1 мин.
Существует два основных способа контроля скорости ферментативных реакций.