
- •II. Некоторые вопросы общей геохимии
- •III. Минералогия общая часть
- •Описательная часть
- •Безводные фосфаты
- •IV. Петрография
- •Осадочные горные породы
- •Латериты II бокситы (аллиты)
- •Горючие сланцы
- •Приложение 1
- •II. Порошковатые
- •IV. Иного вида
- •5. Цвет минерала синий
- •III. Жилковатого или волокнистого сложения а. Не растворяются или плохо растворяются в воде
- •Б. Легко растворяются в воде
- •Б. Цвет черты иной
- •I. Аморфные, скрыт0кристаллические или в виде натечных
- •6. Цвет минерала синий, голубой
- •7. Цвет минерала серый
Приложение 1
РАСЧЕТ ХИМИЧЕСКОГО СОСТАВА МИНЕРАЛОВ НА ФОРМУЛУ
Химический состав минералов рассчитывают на формулы Для расчета формулы необходимо иметь таблицу молекулярных масс окислов для кислородных соединений и таблицу атомных масс элементов для сульфидов.
I. Пример расчета химического анализа халькопирита. В результате химического анализа халькопирита получено: Си 34,5%; Fe 30,3%; S 35,0% (сумма 99,8%). Атомные массы этих элементов соответственно для Си = 63,5, для Fe = 55,9 и для S = 32,0. Разделив массовую концентрацию (в %) каждого элемента на атомную массу, получим атомные количества! Для удобства, чтобы не иметь дробных атомных количеств, умножаем их на 1000. В виде таблицы это можно изобразить так:

Сравнивая отношения между атомными количествами, получим отношения Си : Fe : S = 543 : 545 : 1093 или, упростив, Си : Fe : : S = 1 : 1 : 2, т. е. имеем: CuFeS2.
II. Пример расчета химического анализа граната. Как известно, минералы группы граната представляют собой изоморфный ряд нескольких составляющих; общая формула гранатов: Rf+RfMSidb, где Ra+ = Mg, Са, Fe2+, Мз и R3+ = Al, Fe3+, Cr.
Химический состав граната, изображенный на табл. Iх, рассчитываем на формулу.
Молекулярные количества получаем, разделив массовую концентрацию каждого окисла на молекулярную массу и умножив на 1000.
Например, для SiO2 это будет 36,76 : 60,06 · 1000 = 612.
Молекулярные количества SiO2 и ФЯП2 объединяют.
Расчет состава граната ведется на 12 атомов кислорода. Атомные количества катионов и кислорода получаем из расчета содержания катионов и кислорода в окислах. Например, атомное количество
1 Химический анализ граната взят из книги А. П. Лебедева «Трапповая формация центральной части Тунгусского бассейна», 1955.
323

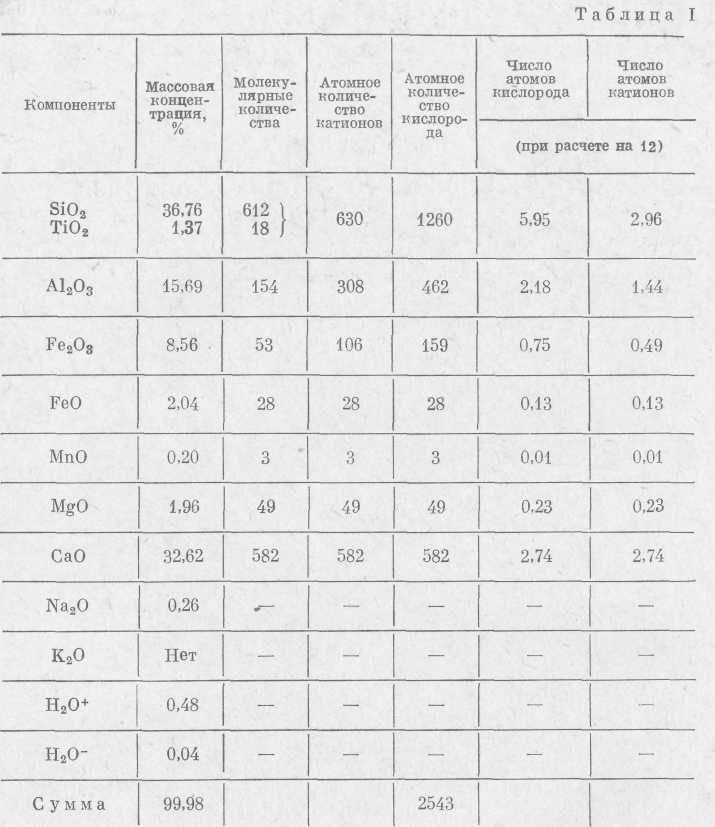
катионов для А12О3 будет 154 X 2 = 308; атомные количества кислорода для А12О3 будут 154 X 3 = 462. Общая сумма атомных количеств кислорода в нашем случае равна 2543. Разделив эту сумму на 12, получаем множитель 212. Затем для каждого компонента узнаем число атомов кислорода. Для этого делим атомное количество на полученный множитель, например для А12О3 462 : 212 = 2,18. Число атомов катионов определяем из соотношения количества катионов и кислорода в окислах. Например, для SiO2 число атомов катиона будет вдвое меньше количества атомов кислорода, т. е. 5,95 : 2 = = 2,96. Теперь объединяем катионы, которые могут изоморфно
324
замещать друг-друга, отдельно двухвалентные (Mn, Ca, Mg, Fe2+) и трехвалентные (Бl и Fe3+). Получаем формулу граната:(Мn0,01,Са2,74Х X Mg0,23Fe2+0,13)3,11 [Аl1,44 Fe3+0,49]1,98 Si2,96O12. Состав этого граната можно выразить в виде отдельных составляющих, которые иногда выделяют как самостоятельные минералы:

Как видно из вышеприведенных формул, некоторые элементы входят в состав только одного минерала, например Mn, Mg, Fe2+, Fe3+, в то время, как другие элементы входят в состав двух (Са), четырех (А1) и пяти (Si) минералов.
Исходя из атомных количеств катионов (табл. III) берем весь Мn и связываем его с эквивалентными количествами А1 и Si (спессартин), Mg и Fe2+ также соответственно связываем с А1 и Si (пироп и альмандин), Fe3+ связываем с эквивалентными количествами Са и Si (андрадит) и наконец, оставшийся А1 связываем с Са и Si (гроссуляр).
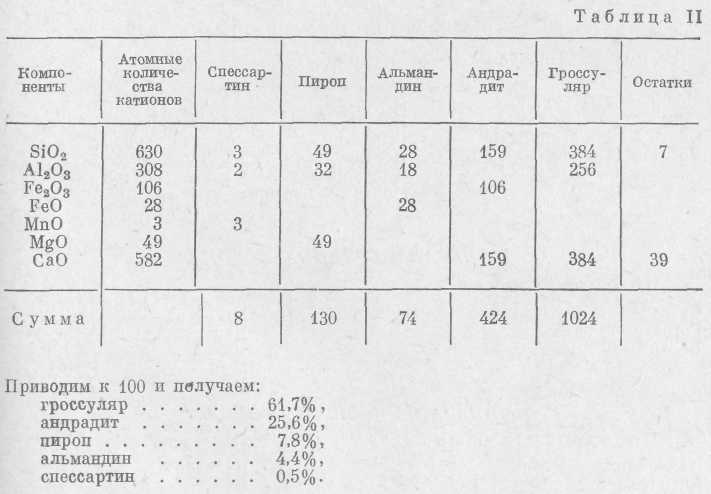
Такое изображение состава граната является приближенным. В данном случае получается избыточное количество СаО ~1%. Присутствие TiO2 свидетельствует о наличии шорломитовой составляющей, а присутствие Н2О — о наличии гидрограната.
325

ПРИЛОЖЕНИЕ 2 ПАРАГЕНЕТИЧЕСКИЕ АССОЦИАЦИИ МИНЕРАЛОВ

327


ПРИЛОЖЕНИЕ 3
ОПРЕДЕЛИТЕЛЬ МИНЕРАЛОВ ПО ВНЕШНИМ ПРИЗНАКАМ
Предлагаемый определитель представляет собой упрощенный вариант определителя минералов по внешним признакам проф. Н. А. Смольянинова1. В качестве основных признаков в определителе приняты блеск, твердость, цвет, формы выделения минералов в природе (порошковатость, волокнистость и т. п.) и растворимость в воде.
Все минералы без металлического блеска по твердости делятся на две группы: с твердостью больше 5 и меньше 5. Эту твердость можно легко установить при помощи ножа или кусочка стекла.
При работе с определителем необходимо пользоваться описательной частью. Она дополняет краткую характеристику минералов, данную в таблицах определителя, позволяя точнее установить определяемый минерал. В частности, необходимо обращать внимание на генетические признаки минералов (условия нахождения в природе, парагенезис и т. п.), которые не вошли в схему определителя, но которым в описательной части уделено больше внимания.
При названии минералов в скобках указаны страницы, на которых они описаны в учебнике.
В определителе приняты следующие сокращения:
Сп. — спайность,
Тв. — твердость,
Плотн. — плотность.
Определение минералов надо вести строго последовательно в том порядке, какой указан в нижеприведенной схеме.
1 Смольянинов Н. А. Практическое руководство по минералогии. М., «Недра», 1972.
329
 СХЕМА
ОПРЕДЕЛЕНИЯ МИНЕРАЛОВ
СХЕМА
ОПРЕДЕЛЕНИЯ МИНЕРАЛОВ
МИНЕРАЛЫ С МЕТАЛЛИЧЕСКИМ БЛЕСКОМ
I. Жидкие, стр. 331. П. Порошковатые, стр. 331.
Игольчатые, волосовидные и жилковатого сложения, стр. 331.
Иного вида.
Цвет минерала железно-черный, стр. 332.
Цвет минерала стально-серый до серебряно-белого, стр. 332.
Цвет минерала от золотистого и соломенно-желтого до медно- красного, стр. 334.
МИНЕРАЛЫ БЕЗ МЕТАЛЛИЧЕСКОГО БЛЕСКА, ТВЕРДОСТЬ ОТ 1 ДО 5
I. Аморфные, скрытокристаллические и в виде натеков и корочек. А. Не растворяются в воде, стр. 334.
Б. Растворяются в воде, стр. 336.
II. Порошковатые
А. Не растворяются в воде.
Цвет минерала буровато-черный, стр. 336.
Цвет минерала красный разных оттенков до вишнево-красного и розовый, стр. 336.
Цвет минерала желтый и зеленовато-желтый, стр. 337.
Цвет минерала зеленый, стр. 337.
Цвет минерала синий, стр. 338.
6. Цвет минерала белый; иногда бесцветен, стр. 338. Б. Растворяются в воде, стр. 338.
III. Жилковатого или волокнистого сложения.
А. Не растворяются или плохо растворяются в воде, стр. 339. Б. Легко растворяются в воде, стр. 339.
IV. Иного вида.
А. Цвет черты красный до оранжево-желтого, стр. 340. Б. Цвет черты иной.
Цвет минерала красный, коричнево-красный, розовый, стр. 340.
Цвет минерала красновато-бурый, бурый до черного, стр. 341.
Цвет минерала желтый разных оттенков, стр. 342.
Цвет минерала изумрудно-зеленый, темно-зеленый и других оттенков зеленого цвета, стр. 343.
5. Цвет минерала голубой, синий, стр. 344.
Цвет минерала фиолетовый, стр. 344.
Цвет минералов белый; серый; бесцветные
а) не растворяются или плохо растворяются в воде, стр. 345.
б) легко растворяются в воде, стр. 348.
330
МИНЕРАЛЫ БЕЗ МЕТАЛЛИЧЕСКОГО БЛЕСКА, ТВЕРДОСТЬ БОЛЬШЕ 5
I. Аморфные, скрытокристаллические или в виде натечных и сфе роидальных форм, стр. 348.
II. В виде кристаллов или зернистых масс.
Цвет минерала черный, зеленовато-черный или темно-бурый, стр. 349.
Цвет минерала красный или розовый, стр. 350.
Цвет минерала желтый или желтовато-зеленый, стр. 351.
Цвет минерала бурый, красновато-бурый, дымчатый, стр. 352.
Цвет минерала зеленый: от бледно-зеленого до темно-зеленого, стр. 352.
Цвет минерала синий, голубой, стр. 353.
Цвет минерала серый, стр. 354.
Цвет минералов белый; иногда бесцветные
а) кристаллы хорошо образованы, различается сингония: кубическая сингония, стр. 355.
тетрагональная сингония, стр. 355.
гексагональная или тригональная сингония, стр. 355.
ромбическая сингония, стр. 356.
б) кристаллы хорошо образованы, сингонию по виду кри сталлов определить нельзя, стр. 356.
в) сплошные зернистые массы и другие образования, стр. 356.
ТАБЛИЦА МИНЕРАЛОВ МИНЕРАЛЫ С МЕТАЛЛИЧЕСКИМ БЛЕСКОМ I. ЖИДКИЕ
Ртуть Hg. Цвет серебряно-белый. Очень подвижные шарики и капельки. Минерал редкий, встречается вместе с киноварью.
