
Строение хромосом интерфазного ядра.
При микроскопическом исследовании интерфазного ядра в нем обнаруживают лишь ядрышко и нежную гранулярную структуру. Это обстоятельство длительное время служило препятствием для защитников теории непрерывности хромосом в клеточных поколениях, а также основой для ложных заключений о полной дезинтеграции хромосом в интерфазном ядре. Электронная микроскопия в течение долгого времени никак не способствовала углублению знаний о субмикроскопической организации хромосом интерфазного ядра. Действительно, и ? ультратонких срезах толщиной 250-500 А основные структуры интерфазного ядра - деспирализованные хромосомы - раскрошены на мельчайшие короткие фрагменты, в результате чего общая картина субмикроскопической организации ядра мало чем отличается от того, что обнаруживается в цитоплазме. Прогресс в исследованиях состояния хромосом в интерфазных ядрах связан с разработкой методов субмикроскопического анализа не срезов ядра, а интактных структур. В настоящее время с этой целью пользуются двумя методами: 1) выделяют из изолированных ядер хромосомные нити в солевом растворе версена (0,07 М NaCl и 0,001 М версен при рН=6,5); 2) изучают интактные хромосомные нити в интерфазных ядрах, распластанных на поверхности выпуклого водного мениска в парафинированной чаше Ландмура. Первым из этих методов, начиная с 1963 г., пользуется Рис (Н. Ris), показавший, что в интерфазных ядрах лимфоцитов тимуса теленка хромосомы представлены многочисленными длинными деспирализованными элементарными нитями диаметром 100-200 А. При рН=8,0 нити в 100 А распадаются на две субъединицы - нити диаметром по 40 А, соответствующие согласно Рису нуклеогистонным нитям.

Рис. 1. Хромосомные нити из ядер эритроцитов тритона, распластанные на выпуклой поверхности воды (по Голлу; х 19 000).
Достоинства второго метода - распластывания интерфазных ядер на поверхности воды - впервые обнаружил Голл (J. G. Gall, 1963), исследовавший таким образом структуру ядра эритроцитов тритона. Ядро оказалось заполненным нитями диаметром 400-600 А (рис. 1). Рис использовал метод распластывания хромосом интерфазного ядра на водной поверхности при более тщательном анализе субмикроскопической их организации в эритроцитах саламандры [Рис и Чандлер (В. L. Chandler), 1963], обнаружив ту же картину, какая была установлена им при анализе интерфазных ядер лимфоцитов тимуса теленка. По Рису, молекулы ДНК сцеплены при помощи гистона в пары, образуя нити диаметром 100А, которые в свою очередь соединяются в пары, формируя нити диаметром 200 А. Такие нити составляют основное содержимое интерфазного ядра (рис. 2).
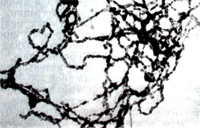
Рис. 2. Хромосомные нити интерфазного ядра из эритроцитов саламандры, распластанные на поверхности воды. Нити толщиной 200-250 А состоят из двух субъединиц по 100 А (по Рису и Чандлеру; X 62 000).
Эти данные подтверждены рядом исследований [Дю Про (Е. L. Du Praw), 1965; Вулфа и Джона (S. L. Wolfe, В. John), 19651. Дю Про, используя тот же метод анализа интактных нитей хромосом, распластанных на поверхности воды, исследовал субмикроскопическую организацию интерфазных ядер в эмбриональных клетках пчелы. Полученные им результаты в принципе аналогичны опубликованным Рисом. Сходную картину описал Вулф, давший анализ субмикроскопической структуры мейотического ядра у Oncopeltes в тот период, когда оно переходит в интерфазное состояние. Таким образом, данные различных исследователей в отношении субмикроскопической организации хромосом интерфазного ядра почти идентичны. Дискуссионными до наст. времени остаются следующие вопросы. 1. Природа нитей диаметром 100 А - представляют ли они пару молекул ДНК, соединенных гистоном, как полагает Рис, или же это одна молекула ДНК, окруженная толстой белковой обкладкой [Дю Про, 1965; Тейлор (J. Н. Taylor), 1963]. 2. Каково соотношение ДНК и гистона в спирализованных, компактно упакованных нитях и в деспирализованных нитях интерфазного ядра и каково соотношение лизинового и аргининового компонентов в гистонах этих нитей. Редупликация хромосомы. Прошло десять лет с тех пор, как впервые в исследованиях репродукции и организации хромосом был применен метод радиоаутографии с использованием предшественника в синтезе ДНК - тимидина, меченного тритием [Тейлор, Вудс и Хьюз (P.S. Woods, YV.L. Hughes), 1957]. Дальнейшие исследования показали, что редупликация белкового компонента хромосом происходит одновременно с репликацией в ней молекул ДНК или протекает немного ранее. Это дало основание рассматривать данные о репликации ДНК как информацию о репродукции хромосом в целом.

Рис. 3. Меченные Н3-тимидином хромосомы Vicia Faba. Метафаза второго деления. Все хромосомы содержат метку только в одной хроматиде (стрелками показаны участки межхроматидных обменов) (по Иорданскому).
Бета-частицы трития обладают низкой энергией; пробег их ограничен 1-1,5 мк. Поэтому положение меченной тритием молекулы в том или ином участке хромосом может быть указано с точностью до 1 мк. Исследованиями последних лет, в том числе и на хромосомах человека, были подтверждены заключения Тейлора (1957), что хроматиды, отходящие к противоположным полюсам во время митоза (см. т. 19), структурно подобны двойной цепи молекулы ДНК: они всегда состоят из двух матриц [Прескотт и Бендер (D. М. Prescott, М. A. Bender), 1963; А. Б. Иорданский, 1964] (рис. 3). Представляют ли собой эти матрицы комплементарные цепи одной молекулы ДНК (как полагает Тейлор) или же матрицы многонитчаты (как следует из многочисленных микроскопических и субмикроскопических исследований структуры хромосом) - этот вопрос интенсивно исследуется в ряде лабораторий. Период синтеза ДНК и, следовательно, редупликации хромосом в клетках различного типа длится 6-12 час. и заканчивается за 3-4 час. до вступления клетки в митоз. Тщательными исследованиями, в том числе и на культуре клеток человека, установлено, что одни хромосомы и их участки редуплицируются в начале этого периода, другие - позднее, и, наконец, имеются хромосомы и их участки, закономерно редуплицирующиеся в самом конце периода синтеза. Другими словами, показано, что у ряда организмов, в том числе у человека, редупликация хромосом протекает асинхронно [Тейлор, 1960; Шмид (W. Schmid), 1963; Джермен (J. German), 1964]. Асинхронность редупликации участков хромосом обусловлена различиями во времени вступления их в период синтеза, а также в скорости и сроках окончания этого процесса (рис. 4).
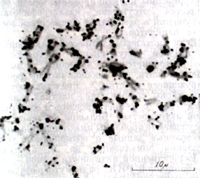
Рис. 4. Меченные H3-тимидином хромосомы в культуре эмбриональных фибробластов человека. Вследствие асинхронности редупликации ДНК метка содержится не во всех хромосомах и не во всех участках хромосом.
В настоящее время усилия многих исследователей сосредоточены на выявлении закономерностей асинхронной редупликации как целых хромосом, так и отдельных участков в пределах одной хромосомы [Кикути и Сандберг (Y. Kikuchi, A. A. Sandberg), 1965; Н. Бьянки и М. Бьянки (N. О. Bianchi, М. S. Bianchi), 1965; С. И. Слезингер и А. А. Прокофьева-Бельговская, 1966]. Есть основания полагать, что специфика поведения хромосом и их отдельных участков в процессе редупликации обусловлена особенностями функционирования хромосом как генетических систем в периоде G1 клеточного цикла. Следует отметить, что постоянство локализации меток на радиоаутографах хромосом позволяет использовать особенности редупликации для идентификации некоторых хромосом.
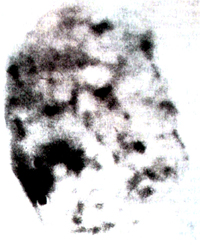
Рис. 5. Ядро из клетки слизистой оболочки полости рта женщины. Компактное тело полового хроматина, сформированное спирализованной X-хромосомой, прилегает к оболочке ядра.
Этот метод особенно перспективен для хромосом тех групп, в пределах которых обычный карпотипический анализ (см. Кариотип, т. 12) затруднен вследствие большого морфологического сходства хромосом между собой (хромосомы 4-5-й, 13-15-й, 21-22-й групп). Особое значение имеет этот метод для идентификации поврежденных хромосом при некоторых заболеваниях. Взаимоотношение структуры, функционирования и особенностей редупликации хромосомы. Функционирование хромосом выражается в двух важнейших процессах: кодировании информационной РНК, обеспечивающем наследственный характер обмена веществ и развития организмов, и собственной репродукции, обусловливающей преемственность генетической структуры хромосом в ряду клеточных поколений и поколений организмов. Период репликации частиц ДНК в хромосомах занимает значительную часть интерфазы, продолжаясь в клетках различного типа от 6 до 12 час. Каковы взаимоотношения в течение этого периода между функционированием хромосом, с одной стороны, и их состоянием в интерфазном ядре, с другой? На уровне микроскопического анализа уже давно установлено, что интерфазные, или покоящиеся, ядра содержат ядрышко и нуклеоплазму, в которой различимы два типа хроматиновых структур: 1) нежно-гранулярная, нитчатая или диффузная и 2) крупные гранулы или массивные хроматиновые тела. Современные электронно-микроскопические исследования подтверждают правильность давно сложившегося представления, что первый тип структур сформирован в разной степени деспирализованными хромосомами, тогда как крупные глыбки и массы хроматина интерфазного ядра - это спирализованные, конденсированные локальные участки хромосом или даже целые отдельные хромосомы (рис. 5). В этой связи особого внимания заслуживают работы, выполненные в лаборатории Мирского (А. Е. Mirsky), в ходе которых была исследована метаболическая активность отдельных фракций конденсированных и диффузно распределенных деспирализованных хромосом. Эти фракции были выделены из изолированных интерфазных ядер лимфоцитов тимуса теленка. Как установлено работами Мирского, основное включение радиоактивных предшественников синтеза РНК и белков происходит лишь во фракции диффузно распределенных деспирализованных хромосом, тогда как конденсированные, спирализованные, хромосомы включают лишь следы этих предшественников, хотя содержат до 80% ДНК интерфазного ядра. Другими словами, метаболическая активность компактных масс спирализованных хромосом в интерфазных ядрах крайне низка. ДНК служит матрицей для РНК только в деспирализованных хромосом [Френстер (J. Н. Frenster) и др.; Оллфри (V. G. Allfrey), Мирский и др., 1963; Литтау (V. С, Littau) и др., 1964]. Установлено, что потеря участком хромосом способности переходить в это состояние сопровождается изменением активности генов, локализованных в данном участке; развитие признака, контролируемого этими генами, изменяется от доминантного проявления к рецессивному [А. А. Прокофьева-Бельговская, 1960; Лайон (М. Lyon), 1962]. Многочисленные данные показывают, что локальная деспирализация участков хромосом сопровождается интенсификацией активности генов, расположенных в этих участках. Эти данные заслуживают самого пристального внимания, так как являются ключом к пониманию одного из механизмов дифференциации функционирования одного и того же участка хромосом в клетках различного типа. Этот механизм состоит в локальном изменении циклического состояния - именно характера спирализации - участка или всей хромосомы, неразрывно связанного с особенностями репликации в них ДНК, - временем начала этого процесса и его окончания. Замечательный феномен контролирования генетической активности хромосом особенностями ее спирализации и репликации в ней ДНК представляет поведение одной из двух Х-хромосом у женщин и у самок млекопитающих. Эта хромосома (по-видимому, независимо от того, отцовского или материнского она происхождения) в течение большей части клеточного цикла находится в спирализованном состоянии, формируя в интеркинетическом ядре компактное хроматическое тело (половой хроматин, или тельце Барра), лежащее под оболочкой ядра (рис. 5). Спирализованное состояние X-хромосомы обусловливает особенности ее репродукции: репликация ДНК в ней протекает с большим запозданием в конце периода синтеза, после окончания этого процесса во всех остальных хромосом. Эти особенности спирализации и репликации Х-хромосомы сопровождаются частичной ее инактивацией как генетической структуры. Следовательно, как у мужчин с системой XY-хромосом, так и у женщин с системой XX-хромосом генетические функции выполняются в основном одинаково лишь одной Х-хромосомой и именно той, которая проходит нормальный цикл спирализации [Грумбах, Морисима (М. Grumbach, А. Morishima); Тейлор, 1963]. У мужчин с нарушенным балансом половых хромосом (XXY, XXXY, XXXXY - различные случаи синдрома Клайнфелтера) в интеркинетических ядрах соответственно обнаруживается одно, два или три компактных хроматических тела - это спирализованные, лишние Х-хромосомы. Радиоаутографические исследования с тимидином-Н3 показали, что в конце периода синтеза в культурах лейкоцитов этих пациентов имеется одна, две или три хромосомы с поздней репликацией ДНК. При помощи указанного выше механизма спирализации, сопровождающегося поздней репликацией молекул ДНК, все лишние Х-хромосомы инактивированы, чем и объясняется отсутствие катастрофических нарушений в развитии и жизнеспособности этих пациентов. Если механизм репрессии активности и поздней редупликации Х-хромосомы распространяется и на аутосомы, то можно предположить, что вообще поздно реплицирующиеся участки хромосом представляют собой районы, содержащие в клетках данного типа гены с репрессированной генетической активностью. Большое значение для обсуждаемой проблемы имеют недавно опубликованные данные о возможности установления локализации на хромосомах продукта непосредственной активности генов - информационной РНК: радиоаутографически исследовалось распределение на хромосомах гранул метки после введения в среду уридина-Н3 [Фудзита, Такеока (S. FuЛta, О. Takeoka); Накадзима (J. Nakaiima) и др., 1966].
