
- •1.1. Гармонические колебания и их характеристики
- •1.2. Пружинный маятник. Математический маятник. Физический маятник
- •2.1. Электрический колебательный контур.
- •2.2. Свободные электрические колебания
- •3.1. Затухающие колебания
- •3.2. Вынужденные колебания
- •6.1. Световая волна и ее виды
- •6.2. Основные определяющие величины
- •6.3. Характер распространения электромагнитных волн
- •7.1. Основные понятия и законы геометрической оптике 7.2. Показатели преломления среды
- •7.3. Линза и ее виды, характеристики
- •8.1.Энергетические величины в фотометрии
- •8.2. Световые величины в фотометрии
- •Лекция 9. Интерференция света
- •14.1. Фотоэффект, его виды и законы
- •14.2. Уравнение Эйнштейна для фотоэффекта
- •14.3. Эффект Комптона
- •15.1. Постулаты Бора
- •15.2. Полная энергия электрона в атоме
- •15.3. Опыт Франка-Герца.
- •Лекция 16. Основные понятия квантовой механики
- •16.1. Корпускулярно-волновой дуализм
- •16.2. Гипотеза де Бройля. Дифракция электронов
- •16.3. Основные понятия квантовой механики
- •17.1. Временное уравнение
- •17.2. Стационарное уравнение Шредингера
- •18.1. Движение частицы в одномерной потенциальной яме.
- •18.2. Прохождение частицы сквозь потенциального барьера. (Туннельный эффект)
- •20.1. Вероятность макросостояния.
- •20.2. Распределение Ферми-Дирака
- •20.3. Распределение Бозе-Эйнштейна
- •22.1. Исходные представления зонной теории твердых тел
- •22.2. Расширение энергетического уровня
- •22.3. Энергетические уровни и зоны
- •23.1. Фотопроводимость полупроводников
- •23.2. Люминесценция твердых тел
- •24.1. Контакт полупроводников p и n типов
- •24.2. Приминение p и n перехода в технике
- •24.3. Транзисторы
- •26.1. Радиоактивность и ее виды
- •26.2. Закон радиоактивного распада
- •26.3. Активность радиоактивного вещества
- •27.1. Правила смещения
- •27.2. Различные виды распадов
- •28.1. Взаимодействие заряженных частиц, нейтронов и γ-квантов со средой
- •28.2. Излучение Вавилова-Черенкова
- •28.3. Взаимодействие нейтронов с веществом
- •30.1. Термоядерные реакции
- •30.2. Условия осуществления управляемых термоядер ных реакции
- •30.3. Физика элементарных частиц.
- •Индивидуальные домашние задания
Лекция 16. Основные понятия квантовой механики
16.1. Корпускулярно-волновой дуализм
16.2. Гипотеза де Бройля. Дифракция электронов
16.3. Основные понятия квантовой механики
Теория Бора оказалась недостаточной для объяснения многих явлений микромира - строения многоэлектронных атомов, молекул, химической связи и т.д. Идеи де Бройля и выявленные на опыте волновые свойства частиц вещества послужили толчком к созданию принципиально новой теории, описывающей поведение микрочастиц с учетом их волновых свойств. Этой теорией стала квантовая (волновая) механика, основы которой были созданы в 1925—1926 гг. В.Гейзенбергом и Э.Шредингером. Квантовая механика раскрывает два основных свойства вещества: квантованность внутриатомных процессов и волновую природу частиц. Квантовая механика лишена наглядности, характерной для классической механики. Образы привычного нам макромира становятся непригодными для описания явлений, происходящих в микромире. При изучении явлений, происходящих в макромире, мы пользовались законами классической физики, которые остаются незыблемыми, если ограничить область их применения. Для того чтобы решить вопрос о том, какими законами механики (классическими или релятивистскими) следует пользоваться для описания рассматриваемого явления, нужно знать, с какой скоростью движется исследуемый объект. Если его скорость соизмерима со скоростью света в вакууме, то нужно применять релятивистские формулы. Скорость света в вакууме является критерием, определяющим границу применимости классических законов, так как она является максимальной скоростью передачи сигналов.
Возникает вопрос: существует ли подобный критерий при описании поведения мельчайших частиц вещества, обладающих корпускулярно-волновым дуализмом? Да, такой критерий существует, им является постоянная Планка.
Для того чтобы описать поведение любой частицы, нужно определить ее координату x, импульс p, энергию Е и т.д. В классической физике нет каких-либо ограничений, запрещающих с любой степенью точности одновременно измерить, например, координату х и соответствую-щую проекцию импульса рх. В квантовой механике положение принципиально иное. Так как движущаяся частица обладает корпускулярно-волновым дуализмом, то одновременное точное определение координаты х и импульса рх невозможно.
Тщательный анализ поведения микроскопических частиц, проведенный Гейзенбергом, показал, что существует принципиальный предел точности измерений указанных величин. Если обозначить Δх, Δу, Δz не точность (неопределенность) определения координаты, а Δрх Δру, Δрz, - неточность (неопределенность) определений соответствующих проекций импульса, то эти величины между собой связаны зависимостями:
![]() (16.1)
(16.1)
Эту зависимость называют соотношением неопределенностей Гейзенберга. Из него следует: чем точнее определена координата (Δx→0), тем менее точно определен импульс (Δрх→0), и наоборот.
Таким образом, соотношение неопределенностей устанавливает пределы, за которыми принципы классической физики становятся неприемлемыми. Если произведение ΔхΔр сравнимо с h, то поведение частицы описывается законами квантовой механики, если ΔхΔр велико по сравнению с h, то поведение частицы описывается законами классической физики. Чтобы понять, почему эксперимент не дает большей точности, чем позволяют соотношения неопределенности, предположим, что необходимо точно определить положение электрона, летящего в пучке со скоростью v, импульсом p (рис, 16.1). На пути пучка находится щель АВ шириной α. За щелью находится экран CD, на котором наблюдается дифракционная картина (ширина щели α сравнима с длиной волны де Бройля λ для электронов). Пунктирной линией изображена плотность вероятности для центрального максимума. При дифракции от одной щели интенсивностью максимумов высшего порядка можно пренебречь по сравнению с интенсивностью центрального максимума.
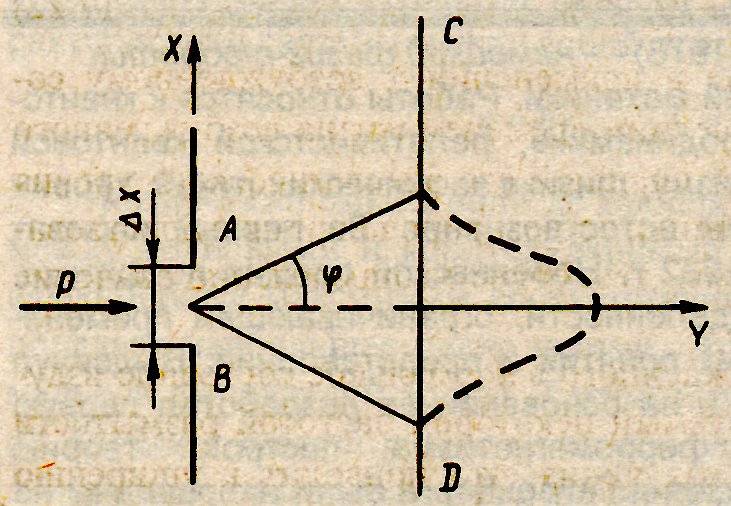
Рис. 16.1
Положение центрального максимума определяется направлением на минимумы первого порядка, т е. углом φ, определяемым из соотношения?
sinφ = 2k λ/2, где k = 1, откуда sinφ=λ/α
где, λ = h/(mv) = h/p (16.2)
Так как каждый электрон до щели движется в пучке перпендикулярно плоскости щели, то составляющая импульса рx = 0, но координата х электрона неопределенная. В момент прохождения щели электрон имеет координату, равную координате щели. В определении координаты электрона содержится неопределенность, зависящая от размеров щели: Δx = α. При дифракции появляется составляющая импульса рx, неопределенность составляющей импульса зависит от угла φ:
Δ рx = р sinφ. (16.3)
Учитывая (16.2), получаем
![]() Δх
Δрx
= h.
(16.4)
Δх
Δрx
= h.
(16.4)
Если учесть наличие второго дифракционного максимума, то неопределенность в определении импульса увеличивается, поэтому выражение можно переписать в виде:
Δх Δрx ≥ h. (16.5)
Соотношение, аналогичное (16.5), имеет место для времени и энергии:
ΔE Δt ≥ h. (16.6)
Рассмотрим это соотношение в применении к возбужденному состоянию атома. Если считать Δt средним временем жизни возбужденного состояния атома, а ΔЕ - средней шириной его энергетического уровня (ценность энергии состояния), то, чем короче время существования какого-либо состояния системы, тем более неопределенно значение его энергии. При переходе атома из возбужденного в нормальное состояние излучается квант энергии, характеризуемый некоторой частотой размытости Δν=ΔЕ/h спектральной линии излучения, что приводит к расширению спектральных линий.
Следует отметить, что волны де Бройля не являются электромагнитными. Они имеют особую природу, не имеющую аналогии в классической физике. Причем волны де Бройля представляют собой универсальное явление для всех движущихся частиц. Гипотеза де Бройля экспериментально подтвердилась в опытах К. Дэвиссона и Л. Джермера в 1927 году, наблюдавших рассеяние электронов монокристаллом никеля.
Электронная пушка
испускала пучок электронов определенней
скорости, которые попадали на монокристалл
никеля и рассеивались им. Приемником
рассеянных электронов служил цилиндр
Фарадея, число электронов, попадавших
в цилиндр Фарадея, было пропорционально
силе тока в электрической цепи цилиндра.
С точки зрения классической физики
электроны рассеивались бы под всевозможными
углами. Однако при наблюдении рассеяния
электронов под углами
![]() оказалось,
что максимум числа отраженных электронов
(максимум силы тока) в электрической
цепи приходился на электроны с энергией
Е
= 54 эВ, что соответствовало волне Де
Бройля
= 0,167 нм. Рассеяние электронов происходило
подобно рассеянию рентгеновских
лучей при выполнении условия Вульфа-Брэгга:
оказалось,
что максимум числа отраженных электронов
(максимум силы тока) в электрической
цепи приходился на электроны с энергией
Е
= 54 эВ, что соответствовало волне Де
Бройля
= 0,167 нм. Рассеяние электронов происходило
подобно рассеянию рентгеновских
лучей при выполнении условия Вульфа-Брэгга:
![]() .
(16.7)
.
(16.7)
Таким образом, опыты Дэвиссона и Джермера подтвердили гипотезу де Бройля о существовании волновых свойств у электронов. Позднее волновые свойства электронов были подтверждены другими независимыми опытами.
В экспериментах по рассеянию электронов на кристаллах, как было показано выше, обнаруживается, что в отдельных направлениях рассеивается большее число электронов, чем во всех других. С волновой точки зрения наличие максимумов числа электронов в некоторых направлениях означает, что в этих направлениях волны де Бройля имеют наибольшую интенсивность. Учитывая, что интенсивность волны пропорциональна квадрату модуля амплитуды волны, можно дать своеобразное вероятностное толкование волн де Бройля. Квадрат модуля амплитуды А2 волн де Бройля в данной точке пространства является мерой вероятности того, что частица находится в этой точке.
Для описания
распределения вероятности нахождения
частицы в данный момент времени в
некоторой области пространства вводится
функция координат и времени, которую
называют волновой функцией
![]() .
Волновая функция
сама
по себе физического смысла не имеет,
смысл имеет квадрат модуля волновой
функции. Определим его следующим
образом: вероятность
.
Волновая функция
сама
по себе физического смысла не имеет,
смысл имеет квадрат модуля волновой
функции. Определим его следующим
образом: вероятность
![]() того, что частица находится в элементе
объема
того, что частица находится в элементе
объема
![]() ,
пропорциональна квадрату модуля волновой
функции
,
пропорциональна квадрату модуля волновой
функции ![]() 2
и элементу объема
,
т.е.
2
и элементу объема
,
т.е.
![]() . (16.8)
. (16.8)
Плотность вероятности будет равна
![]() (16.9)
(16.9)
Она определяет
вероятность пребывания частицы в данной
точке пространства. Следовательно,
квадрат модуля волновой функции,
где
![]() комплексно сопряженная с
волновая функция, представляет собой
вероятность нахождения частицы в данной
точке пространства. Иными словами,
величина
комплексно сопряженная с
волновая функция, представляет собой
вероятность нахождения частицы в данной
точке пространства. Иными словами,
величина![]() определяет интенсивность волн де Бройля.
По определению волновой функции она
должна удовлетворять следующему условию:
определяет интенсивность волн де Бройля.
По определению волновой функции она
должна удовлетворять следующему условию:
![]() , (16.10)
, (16.10)
где тройной интеграл вычисляется по всему пространству от - до . Выражение означает, что нахождение частицы в какой - либо точке всего бесконечного пространства есть достоверное событие и его вероятность должна быть равна единице. Выражение называют также условием нормировки волновой функции или условием нормировки вероятностей.
ЛЕКЦИЯ 17. ОБЩЕЕ УРАВНЕНИЕ ШРЕДИНГЕРА
