
- •Оглавление
- •Введение
- •Тема 1. Структура, функции и технологии получения аминокислот и пептидов
- •1.1. Структура и функции аминокислот и пептидов
- •1.2. Технологии получения аминокислот
- •1.2.1. Получение глутаминовой кислоты
- •1.2.2. Получение лизина
- •1.2.3. Получение триптофана
- •1.3. Технологии получения пептидных антибиотиков
- •1.3.1. Получение тиротрицина
- •1.3.2. Получение грамицидина с
- •1.3.3. Получение бацитрацинов
- •Тема 2. Структура, функции и технологии получения нуклеозидов, нуклеотидов и олигонуклеотидов
- •2.1. Структура и функции нуклеозидов,
- •Нуклеотидов и олигонуклеотидов
- •2.2. Технологии получения нуклеозидов
- •2.2.1. Получение ацикловира
- •2.2.2. Получение рибавирина
- •2.2.3. Получение зидовудина
- •2.3. Технологии получения нуклеотидов и олигонуклеотидов
- •2.3.1. Получение фосфадена
- •2.3.2. Получение нуклеината натрия
- •Тема 3. Структура, функции и технологии получения углеводов
- •3.1. Структура и функции углеводов
- •3.2. Технологии получения углеводов
- •3.2.1. Получение глюкозы
- •3.2.3. Получение инулина
- •3.2.4. Получение гепарина
- •Тема 4. Структура, функции и технологии получения липидов
- •4.1. Структура и функции липидов
- •4.2. Технологии получения липидов
- •4.2.1. Получение эссенциальных фосфолипидов
- •4.2.2. Получение облепихового масла
- •4.2.3. Получение рыбьего жира
- •Тема 5. Структура, функции и технологии получения витаминов
- •5.1. Структура и функции витаминов
- •5.2. Технологии получения витаминов
- •5.2.1. Получение витамина в2
- •5.2.2. Получение витамина с
- •5.2.3. Получение витамина а (ретинол)
- •5.2.4. Получение витамина e
- •Тема 6. Структура, функции и технологии получения стероидов
- •6.1. Структура и функции стероидов
- •6.2. Технологии получения стероидов
- •6.2.1. Получение преднизолона
- •6.2.2. Получение дексаметазона
- •6.2.3. Получение строфантина к
- •Список литературы
- •Химия и технология биологически активных веществ
4.2. Технологии получения липидов
4.2.1. Получение эссенциальных фосфолипидов
Эссенциальные фосфолипиды (ЭФЛ, лецитин) в естественных условиях представляют собой смесь различных фосфолипидов (фосфатидилхолин, фосфатидилсерин, фосфатидилинозит, фосфатидил-этаноламин).
Структурные формулы ЭФЛ представлены на рис. 4.3, где R1 и R2 – остатки ненасыщенных жирных кислот (линолевая, линоленовая, олеиновая).
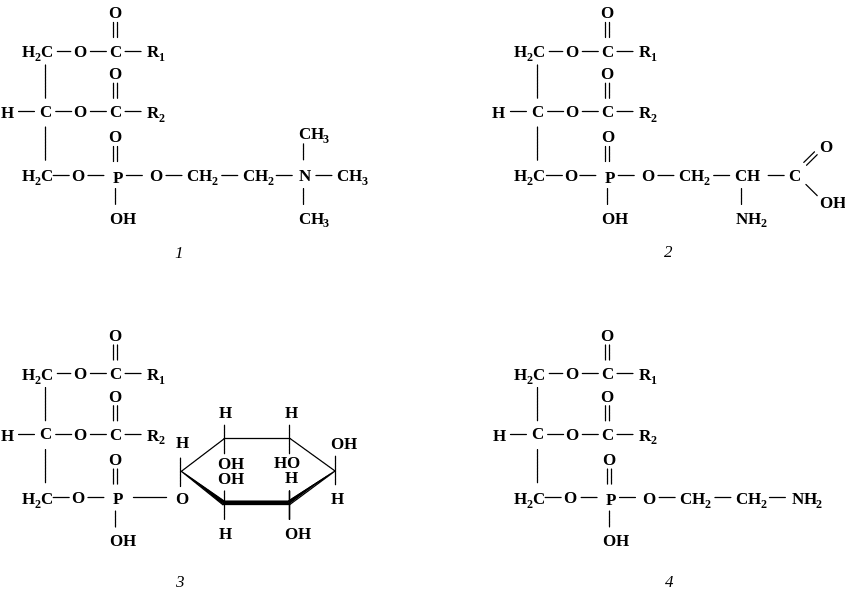
Рис. 4.3. Структурные формулы эссенциальных фосфолипидов:
1 – фосфатидилхолин; 2 – фосфатидилсерин; 3 – фосфатидилинозит;
4 – фосфатидилэтаноламин
Содержание фосфатидилхолина (ФХ), который рассматривается в качестве необходимого компонента пищевого рациона человека, в нативной смеси фосфолипидов составляет 13–20%.
Для профилактики и лечения заболеваний печени применяются специально разработанные лекарственные средства на основе ЭФЛ, такие как «Эссенциале», «Эссенциале форте», «Эссливер форте», «Резалют Про» и др., очищенные от масел и нежелательных примесей, активнодействующим веществом которых является ФХ. При этом содержание ФХ увеличивается в 4–5 раз по сравнению с содержанием в природном лецитине.
Мембраностабилизирующее и гепатопротективное действие ЭФЛ достигается путем непосредственного встраивания их молекул в фосфолипидную структуру поврежденных клеток печени, замещения дефектов и восстановления барьерной функции липидного бислоя мембран. Ненасыщенные жирные кислоты фосфолипидов способствуют повышению активности и текучести мембран, в результате чего уменьшается плотность фосфолипидных структур, нормализуется их проницаемость. Экзогенные фосфолипиды активируют расположенные в мембране фосфолипидзависимые ферменты. Это, в свою очередь, оказывает поддерживающее влияние на обменные процессы в клетках печени, повышая ее детоксикационный и экскреторный потенциал.
Гепатозащитное действие ЭФЛ основывается также на ингибировании процессов перекисного окисления липидов, которые рассматриваются как один из ведущих патогенетических механизмов развития поражений печени.
Технологическая схема получения лекарственных средств на основе ЭФЛ представлена на рис. 4.4.
Исходное сырье – соевые бобы (лецитин – 0,5%) – очищают и измельчают, затем проводят экстракцию липидов гексаном. Полученную смесь фильтруют. Высушенный осадок – соевая мука (побочный продукт) – используют в качестве корма для животных. Из фильтрата при пониженном давлении выпаривают гексан и получают сырое соевое масло, которое нагревают до 60–80°С и смешивают с водой для набухания и осаждения лецитина. Последний отделяют центрифугированием с получением лецитинового осадка и рафинированного соевого масла. Лецитиновый осадок от бледно-желтого до коричневатого цвета, содержащий 33% фосфолипидов, 12% масла и 55% воды, высушивают при пониженном давлении. Получают сырой лецитин, из которого после очистки и фракционирования органическими растворителями выделяют лецитин с высоким содержанием ФХ. Последующим фракционированием с помощью этанола получают высокоочищенную фракцию ФХ.
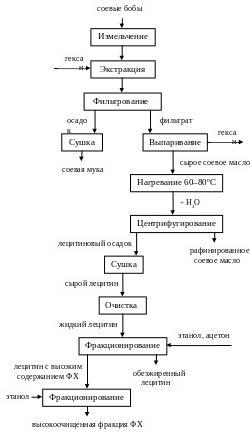
Рис. 4.4. Технологическая схема получения
лекарственных средств на основе ЭФЛ
