- •Н. М. Кузьменок Азотсодержащие производные углеводородов
- •Азотсодержащие производные углеводородов. Нитросоединения лекции 1,2
- •1. Классификация азотсодержащих производных углеводородов.
- •Классы азотсодержащих производных углеводородов
- •2. Нитросоединения. Классификация и номенклатура нитросоединений.
- •3. Способы получения.
- •4. Физические свойства.
- •5. Строение нитрогруппы, параметры связей, электронные смещения нитрогруппы как заместителя (I-, m-эффекты).
- •6. Химические свойства нитросоединений.
- •7. Применение, важнейшие представители.
- •Амины лекции 3,4
- •1. Классификация и номенклатура аминов.
- •2. Способы получения аминов.
- •3. Физические свойства и строение алкиламинов
- •4. Химические свойства алкиламинов
- •В неводных растворах или газовой фазе
- •5. Химические свойства ариламинов
- •Диазо- и азосоединения лекции 5,6
- •1. Классификация азо- и диазосоединений.
- •2. Ароматические соли диазония: строение, номенклатура.
- •2.1. Строение ароматических солей диазония
- •2.2. Номенклатура диазосоединений
- •3. Синтез солей арилдиазония.
- •4. Кислотно-основные равновесия в растворах диазосоединений.
- •5. Химические свойства солей арилдиазония.
- •6. Ароматические азосоединения.
- •7. Элементы теории цветности.
- •8. Общие представления об алифатических диазосоединениях.
- •Учебное издание
- •Азотсодержащие производные углеводородов Курс лекций
Диазо- и азосоединения лекции 5,6
План лекций 5,6
1. Классификация азо- и диазосоединений.
2. Ароматические соли диазония: строение, номенклатура.
3. Синтез солей арилдиазония.
4. Кислотно-основные равновесия в растворах диазосоединений.
5. Химические свойства солей арилдиазония.
6. Ароматические азосоединения.
7. Элементы теории цветности.
8. Общие представления об алифатических диазосоединениях.
1. Классификация азо- и диазосоединений.
Диазо- и азосодинения являются родственными соединениями, содержащими азогруппу. Азогруппа представляет собой два атома азота, которые связаны двойной или тройной связью.
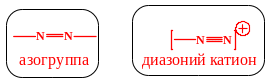
В молекулах диазосоединений азогруппа соединена с одним углеродным радикалом, а в молекулах азосоединений – с двумя.
Диазосоединения.
Диазосоединения – общее название органических веществ, содержащих группировку из двух атомов азота, связанную с одним атомом углерода. Выделяют две группы диазосоединений: ароматические диазосоединения и диазоалканы.
Примеры диазосоединений:
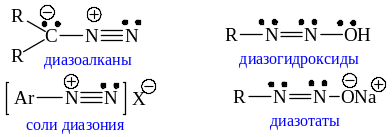
Ароматические диазосоединения – класс органических соединений общей формулы ArN2X, содержащих группировку из двух атомов азота (-N2 или -N2-), связанную только с одним углеводородным радикалом (бензольным кольцом). Ароматические диазосоединения существуют в виде катионов и нейтральных молекул.
Фрагмент Х может быть анионом сильной кислоты (Cl¯, Br¯, HSO4¯, BF4¯ и др.) или ковалентно-связанной группой (-OH, -O¯, -CN, CH3COO-,-I и др.).
Если Х – анион сильной кислоты, то соединения называются солями арилдиазония:
 ,
,
если Х = ОН, то – арилдиазогидроксидами (диазенолы по международной номенклатуре):
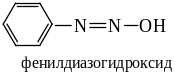 ,
,
если Х = -O¯ или ОМе , где Ме – одновалентный металл, то – арилдиазотатами (по международной номенклатуре диазенолят):
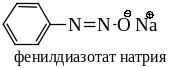
Органические соединения, содержащие в молекуле группу из двух атомов азота – N=N– (азогруппу), не входящую в циклическую систему и связанную с углеводородными радикалами, называются азосоединениями.
В большинстве известных азосоединений оба радикалы являются ароматическими(например,азобензол).
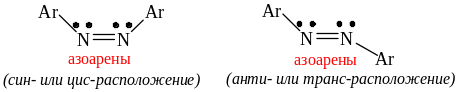
Известны также алифатические азосоединения (простейший представитель – азометан) и соединения, содержащие различные радикалы (алифатические и ароматические или гетероциклические:
 .
.
2. Ароматические соли диазония: строение, номенклатура.
2.1. Строение ароматических солей диазония
Катион арилдиазония представляет собой плоскую систему с линейно расположенными в плоскости ароматического кольца атомами азота. Атомы азота связаны между собой тройной связью:

Ароматические диазокатионы (ArN2+) – гораздо более стабильные частицы, чем алифатические (AlkN2+). Устойчивость объясняется мезомерной стабилизацией ароматического диазокатиона вследствие сопряжения π-электронов ароматического кольца с диазогруппой:
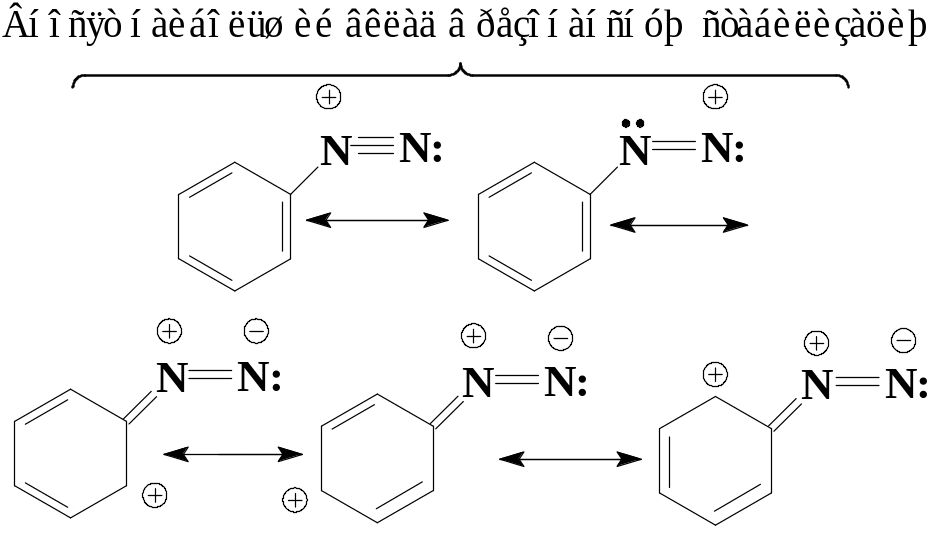 .
.
В случае алифатических диазосоединений подобная стабилизация отсутствует, в связи с чем алифатические диазосоединения менее устойчивы.
Соли диазония имеют ионное строение подобно четвертичным аммониевым солям. Их водные растворы являются электролитами. Водные растворы диазониевых солей с анионами сильных кислот имеют нейтральную среду, что свидетельствует о том, что это соли сильных оснований.
Арилдиазоний хлориды, сульфаты и нитраты в свободном виде неустойчивы и при нагревании разлагаются со взрывом.
Соли арилдиазония, получаемые из ариламиносульфоновых кислот, существуют в виде диполярных ионов, поэтому малорастворимы в воде:

Соли с комплексными анионами менее растворимы в воде и более устойчивы.
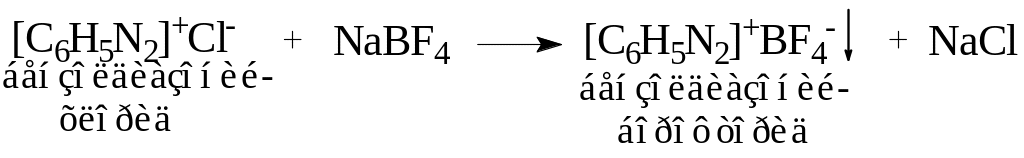
Тетрафторборат фенилдиазония (PhN2BF4) можно хранить в твердом виде в течение нескольких месяцев.
Диазониевые соли слабых кислот (уксусной, синильной, азотистой и др.) обычно превращаются в соединения с ковалентными связями, из которых соль диазония может быть регенерирована действием сильной кислоты: