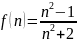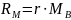- •Углеводы и методы их определения
- •Введение
- •1 Литературный обзор
- •1.1 Общая характеристика углеводов
- •1.2 Химические свойства моносахаридов и полисахаридов
- •1) Реакции карбонильной группы
- •2) Реакции гидроксильных групп
- •3) Кето – енольная таутомерия
- •4) Реакция Молиша
- •5) Реакция Селиванова
- •6) Реакции брожения
- •7) Важные производные моносахаридов
- •8) Реакция Майяра
- •9) Ферментативный гидролиз полисахаридов
- •2 Экспериментальная часть
- •2.1 Методика фотоколориметрического определения общего сахара в кондитерских изделиях
- •2.2 Определение крахмала в зерновом сырье по методу Эверса
- •2.3 Методика определения сахара в сухих винах с использованием колоночной хроматографии методом рефрактометрии
- •Область применения
- •Заключение
- •2) Определение крахмала в зерновом сырье по методу Эверса
- •Список основных источников
2.3 Методика определения сахара в сухих винах с использованием колоночной хроматографии методом рефрактометрии
Общая характеристика метода
Рефрактометрия – оптический метод исследования, основанный на измерении показателя преломления луча света, проходящего через исследуемое вещество.
В основе метода лежит явление рефракции, то есть преломление световых лучей на границе раздела двух различных по своей природе оптических сред.
Рефракция света является следствием его взаимодействия с частицами вещества, через которое проходит свет. Под воздействием электромагнитных колебаний света в атомах вещества возникают вынужденные колебания электронов и ядер. Вследствие этого происходит их смещение относительно друг друга, что приводит к несовпадению «центров тяжести» отрицательного и положительного электричества в атомах и молекулах, то есть атомы, и молекулы вещества поляризуются в электромагнитном поле света.
Преломление света оценивается показателем преломления n, который равен отношению синуса угла падения α к синусу угла преломления β:
|
|
(2.15) |
Показатель преломления зависит от ряда факторов: природы вещества, длины волны падающего света, плотности среды, концентрации раствора и температуры. Существует прямолинейная зависимость между величиной показателя преломления и концентрацией сахара в водном растворе, которая используется при определении концентрации сахара в растворах.
Метод рефрактометрии применяется также для идентификации веществ, определения их чистоты и концентрации в растворе.
Зависимость показателя преломления от плотности вещества выражается формулой:
|
|
(2.16) |
где n – показатель преломления;
r – удельная рефракция вещества, см3/г;
d – плотность вещества, г/см3.
Функция f(n) выражается соотношением:
|
|
(2.17) |
Отсюда
|
|
(2.18) |
Размерность удельной рефракции соответствует удельному объему, то есть r, см3/г.
Умножение удельной рефракции r на молярную массу вещества МВ дает величину молярной рефракции RM:
|
|
(2.19) |
Подставив значение удельной рефракции r в формулу (2.19), получают уравнение, связывающее молярную рефракцию вещества с его плотностью, молярной массой и поляризуемостью:
|
|
(2.20) |
где RM – молярная рефракция вещества В см3/моль;
МВ – молярная масса вещества В, г/моль;
n – показатель преломления вещества В;
d – плотность вещества В, г/см3.
Выражение (2.20) носит название формулы Лорентц – Лоренца. Она при меняется в расчетах и достаточно точно отвечает правилу аддитивности молекулярной рефракции. Рассчитанные по этой формуле результаты мало зависят от изменений температуры, давления и агрегатного состояния вещества во время анализа.
Правило аддитивности молекулярной рефракции заключается в следующем: сумма атомных рефракций элементов, входящих в соединение, равна молекулярной рефракции этого соединения.
|
|
(2.21) |
где α – коэффициент поляризуемости, см3;
NA – постоянная Авогадро, 6,02204∙1023 моль–1.
Коэффициент поляризуемости (α) зависит от объема атомов и молекул вещества и не зависит от температуры. Экспериментально установлено, что α ≈ r3, где r – радиус поляризованной молекулы.
Физический смысл молярной рефракции поясняет соотношение:
|
|
(2.22) |
где NA – число молекул в 1 моль вещества, моль–1;
 –
объем
шара, т.е. объем поляризованной молекулы;
–
объем
шара, т.е. объем поляризованной молекулы;
Отсюда следует, что RM – суммарный объем всех поляризованных молекул, содержащихся в 1 моль вещества. Объем поляризованных молекул состоит из объемов атомов и объемов, занимаемых двойными и тройными связями. Объем атомов называют атомной рефракцией Rат, а объем связи – рефракцией связи Rсв. Из сказанного видно, что молярная рефракция – аддитивная величина.
Значения рефракций атомов некоторых элементов и связей представлены в таблице 2.8
Таблица 2.8– Атомные рефракции и рефракции связей по Фогелю
Атомные рефракции |
Рефракции связи |
|||
Название атома |
Rат |
Вид связи |
Rсв |
|
Углерод |
2,591 |
C – H |
1,676 |
|
Водород |
1,028 |
C – C |
1,296 |
|
Кислород |
1,610 |
C – O в ацеталях |
1,460 |
|
Азот (NH2) |
4,438 |
О – С в спиртах |
1,660 |
|
|
|
С = С |
4,17 |
|
Сущность определения содержания сахара в сухих винах с использованием колоночной хроматографии методом рефрактометрии
Рефрактометрическое определение содержания сахара в пищевых продуктах основано на существовании прямолинейной зависимости между величиной показателя преломления и концентрацией сахара в растворе.
Оборудование
1. Рефрактометр ИРФ – 454 БМ;
2. Аналитические весы;
3. Мерные колбы объемом 25 см3 (5 шт.);
4. Пипетка глазная;
5. Хроматографическая колонка;
6. Фильтровальная бумага.
Применяемые реактивы
1. Водно – спиртовый раствор. Приготовление ведется с учетом содержания спирта. Например, на этикетке указано «Алк. 9 – 11% об.», следовательно, водно – спиртовый раствор готовится в соотношении 91:9 частей;
2. Дистиллированная вода;
3. Вино.
Рефрактометр ИРФ – 454БМ
Измерение показателя преломления исследуемых веществ проводят на рефрактометре ИРФ – 454БМ, принцип действия которого основан на явлении полного внутреннего отражения при прохождении светом границы раздела двух сред с разными показателями преломления. Все измерения проводят в «белом свете» (дневном или электрическом). Для получения высокой точности показатели преломления исследуемых жидкостей замеряют при определенной температуре и определенной длине волны.
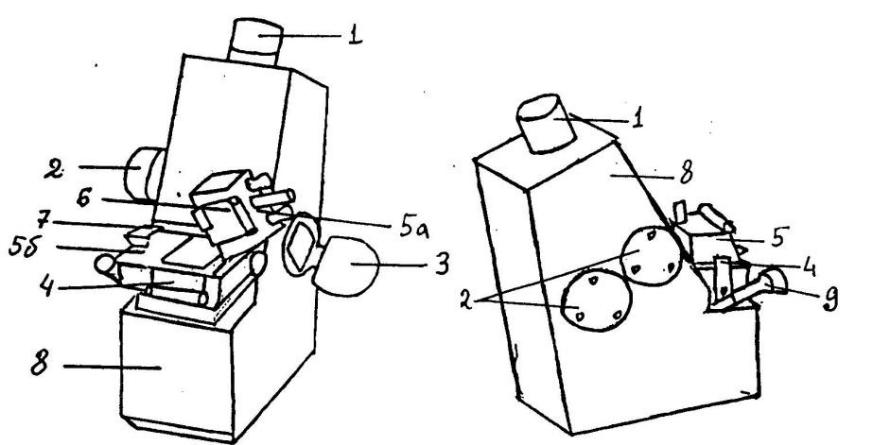
Рисунок 2.14 – Рефрактометр ИРФ – 454БМ
1 – окуляр; 2 – маховики; 3, 4 – зеркала; 5 – рефрактометрический блок с подвижной (а) и неподвижной (б) призмами; 6 – заслонка; 7 – крючок; 8 – корпус прибора; 9 – место установки термометра
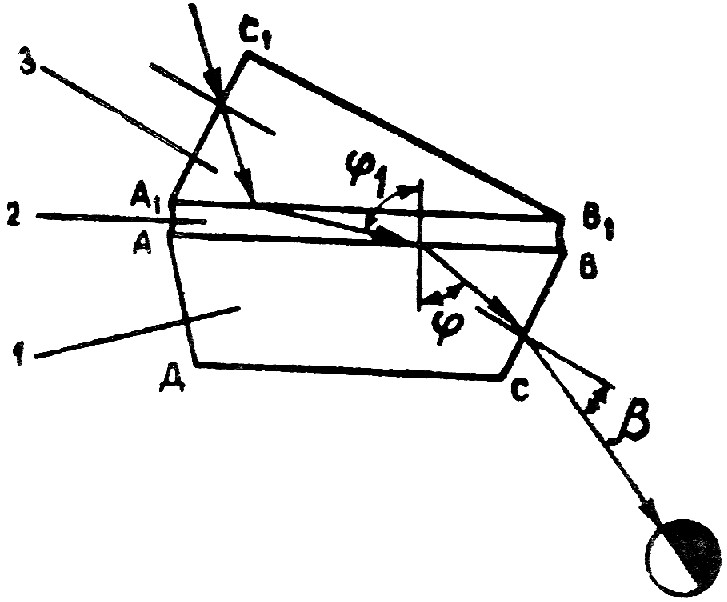
Рисунок 2.15 – Схема призм рефрактометра
1 – измерительная призма; 2 – исследуемая жидкость; 3 – осветительная призма
Порядок работы рефрактометра ИРФ – 454БМ
Рефрактометр устанавливают так, чтобы свет падал на входное окно осветительной призмы и на зеркало, которым направляют свет во входное окно измерительной призмы. Для этого нужно открыть заслонку 6 и зеркала 3, 4 (см. рисунок 2.14).
Осветительную призму открыть на угол 100°. На чистую полированную поверхность измерительной призмы 1 (см. рисунок 2.15) стеклянной палочкой или пипеткой, не касаясь призмы, нанести 2 – 3 капли жидкости так, чтобы вся поверхность была покрыта пленкой жидкости. Опустить осветительную призму 3 и прижать ее крючком 7. Измерения прозрачных жидкостей проводят в проходящем свете, когда он проходит через открытое окно осветительной призмы.
Лучи света проходят осветительную призму 3, рассеиваясь на выходе матовой гранью А1В1, входят в исследуемую жидкость и падают на полированную грань АВ измерительной призмы 1 (см. рисунок 2.15). Поворотом зеркала 3 (см. рисунок 2.14) ярко освещают призму белым светом. Все поле в окуляре должно быть освещено равномерно.
Наличие темных пятен указывает на недостаточное количество взятой для анализа жидкости. В таком случае призмы раскрывают и добавляют несколько капель исследуемой жидкости и снова плотно сжимают их.
До начала измерений проверьте чистоту осветительной и измерительной призм прибора (смочите их дистиллированной водой и протрите чистой мягкой салфеткой).
Перед измерениями проверяют рефрактометр по дистиллированной воде:
а) на чистую полированную поверхность измерительной призмы осторожно, не касаясь ее поверхности, наносят пипеткой 2 – 3 капли дистиллированной воды и опускают осветительную призму;
б) поворотом зеркала добиваются наилучшей освещенности шкалы. Вращением нижнего маховика, расположенного на правой стороне рефрактометра и смотря в окуляр, границу светотени вводят в поле зрения окуляра 1. Вращением верхнего маховика устраняют цветную окраску границы раздела света и тени и наводят ее на резкость;
в) наблюдая в окуляр, совмещают центр перекрестия с линией светотени с помощью нижнего маховика и измеряют значение показателя преломления воды на шкале, расположенной внизу окуляра.
При 20°С показатель преломления воды nD = 1,3330. Если опыт проводился при другой температуре (измерить температуру воды термометром), то вводится температурная поправка к полученному значению показателя преломления для воды:
|
Δn = 0,0565 ∙ 10–4 + 10–4 ∙ (t0 – 10) |
(2.23) |
где 10–4 – температурный коэффициент показателя преломления дистиллированной воды, 1/град.
|
n = n′D + Δn |
(2.24) |
Совпадение экспериментально полученного значения n с данными таблицы 2.9 при той же температуре говорит о том, что рефрактометр настроен.
Таблица 2.9 – Температурные отклонения показателя преломления воды
t,°C |
nD |
t,°C |
nD |
15 |
1,3335 |
23 |
1,3327 |
16 |
1,3334 |
24 |
1,3326 |
17 |
1,3333 |
25 |
1,3325 |
18 |
1,3332 |
26 |
1,3324 |
19 |
1,3331 |
27 |
1,3323 |
20 |
1,3330 |
28 |
1,3322 |
21 |
1,3329 |
29 |
1,3321 |
22 |
1,3328 |
30 |
1,3320 |
Выполнение работы
1) Приготовить растворы для построения градуировочного графика
Готовят пять градуировочных растворов сахарозы в мерных колбах емкостью 25 см3, охватывая диапазон ожидаемой концентрации в исследуемом образце (например, на этикетке вина написано: «сахара 30 – 50 г/дм3», следовательно, нужно приготовить растворы сахара концентрации 20; 30; 40; 50; 60 г/дм3). В качестве растворителя используют водно – спиртовый раствор.
Градуировочные растворы готовятся из массы навески сахарозы при приготовлении 25 см3 раствора с концентрацией сахара 20 г/дм3 по соотношению:
20 г – 1000 см3.
m1, г – 25 см3.
Навеску сахарозы количественно переносят через воронку в мерную колбу вместимостью 25 см3. В колбу добавляют водно – спиртовой раствор на ½ ее объема и перемешивают содержимое до полного растворения сахарозы. Затем оставшийся объем довести до метки водно – спиртовым раствором и перемешивают. Аналогично рассчитывают и готовят растворы других концентраций.
2) Измерить показатель преломления градуировочных растворов:
а) приподнять осветительную призму и поверхности обеих призм осторожно протереть фильтровальной бумагой;
б) нанести 2 капли раствора на поверхность измерительной призмы и опустить осветительную призму;
в) поворотом верхнего маховика установить границу светлого и темного полей. Она должна быть четкой и не иметь радужной окраски;
г) вращать нижний маховик до совпадения границы темного и светлого участка поля зрения.
д) полученные данные занести в таблицу 2.10;
Таблица 2.10 – Результаты эксперимента
№ коблы |
Концентрация сахарозы, г/дм3 |
Показатель преломления |
водно – спиртовой раствор |
– |
|
1 |
|
|
2 |
|
|
3 |
|
|
4 |
|
|
5 |
|
|
3) Подготовить исследуемый продукт к анализу. Вино, полученное для анализа предварительно пропускают через хроматографическую колонку, заполненную активированным углем, чтобы отделить красящие органические вещества. Устанавливают скорость капания, равную вытеканию 1 капли через каждые 3 с. Если вино недостаточно осветлилось, операцию повторяют 2 – 3 раза.
4) Измерения показателя преломления очищенного вина ведется аналогично измерению показателя преломления градуировочных растворов.
5) По окончании измерений промыть обе призмы дистиллированной водой и вытереть насухо фильтровальной бумагой.
6) Построить градуировочный график по результатам таблицы 2.10.
7) Используя градуировочный график, определите содержание сахарозы в вине, и сравнить с данными на этикетке бутылки.
Обработка результатов эксперимента
1) Проверяют рефрактометр по дистиллированной воде
Показатель преломления по дистиллированной воде n = 1,3302 при температуре проведения эксперимента Т = 28,8°С
Δn = 0,0565 ∙ 10–4 + 1 ∙ 10–4(t – 10) = 0,0565 ∙ 10–4 + 1 ∙ 10–4(28,8 – 10) = 1,89 · 10–3
n = n′D + Δn = 1,3302 + 1,89 · 10–3 = 1,33209 ~ 1,3321
2) Построить градуировочный график по результатам таблицы 2.11
Таблица 2.11– Результаты эксперимента
№ колбы |
Концентрация сахарозы, г/дм3 |
Показатель преломления |
водно – спиртовой раствор |
− |
1,3340 |
1 |
25 |
1,3380 |
2 |
30 |
1,3385 |
3 |
35 |
1,3390 |
4 |
40 |
1,3395 |
5 |
45 |
1,3400 |
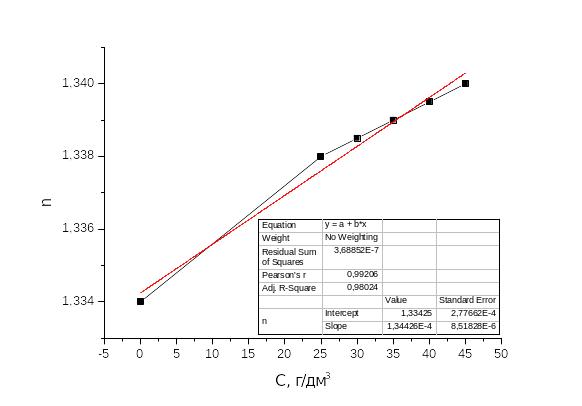
Рисунок 2.16 – График зависимости показателя преломления n от концентрации водно – спиртового раствора сахарозы, г/дм3
3) Используя градуировочный график, определить содержание сахарозы в вине, и сравнить с данными на этикетке бутылки.
Показатель преломления для образца вина n = 1,3390
Уравнение прямолинейной зависимости показателя преломления n от концентрации водно – спиртового раствора сахарозы, г/дм3: n = 1,34426 · 10−4 · C + 1,33425, следовательно:
n = 1,34426 · 10−4 · C + 1,33425
1,3390 = 1,34426 · 10−4 · C + 1,33425
0,00475 = 1,34426 · 10−4 · C
C = 35,3354 ~ 35,33 г/дм3
Анализируемое винное изделие – полусладкое белое столовое вино «Русская Лоза Мускат», алк 10 – 12%, сахар 30 – 40% объем 0,7л