- •Рецензент: профессор, д.Т.Н. Андрей Владимирович Чернышев
- •(С) 2014 мгту им. Н.Э. Баумана введение
- •Цель работы
- •Одноступенчатая парокомпрессионная холодильная машина
- •Свойства хладагентов и термодинамические диаграммы
- •Методика теплового расчета простого парокомпрессионного цикла и холодильного компрессора
- •Пример теплового расчета простого парокомпрессионного цикла с одноступенчатым холодильным компрессором
- •Основные рабочие показатели холодильного компрессора
- •Элементы конструкции холодильной машины
- •Цикл и принципиальная схема регенеративной холодильной машины
- •Контрольные вопросы
- •Индивидуальные задания
- •Литература
- •Оглавление
Свойства хладагентов и термодинамические диаграммы
Свойства основных рабочих тел холодильных машин (хладагентов) подробно изучены и по ним есть большой объём информации [1, 2, 3, 4]. Кратко напомним основные свойства и их размерности.
В отдельных аппаратах холодильной машины реализуются целенаправленные воздействия на одно или несколько свойств рабочего тела. Состояние рабочего тела изменяется в нужном направлении, и такие свойства называются независимыми переменными процесса. В ПКХМ такими переменными являются, как правило: температура, давление и удельный объем. Например, в компрессоре или регулирующем вентиле меняется давление рабочего тела. В однофазном состоянии достаточно знать значения только двух свойств простого рабочего тела, чтобы по ним найти значения всех остальных свойств.
Температура выражается в градусах в шкале Цельсия (t, °С) или в кельвинах в абсолютной шкале Кельвина (T, К). Связь между ними следующая: T = t + 273,16. В СИ абсолютное давление p выражается в Паскалях (Па). Используются также кратные единицы: 1 кПа = 103 Па, 1 МПа = 106 Па. В других системах измерения давление измеряется в барах (1 бар = 106 дин/см2 = 0,1 МПа) и технических атмосферах (1 ат = 1 кгс/см2). Удельный объем v выражается в (м³/кг). Важным свойством веществ является плотность ρ = 1/v, т.е. величина, обратная удельному объему. Размерность плотности - кг/м³.
Кроме простых свойств тел, важными являются функции состояния. Это энтальпия H (кДж) и энтропия S (кДж/К).
Энтальпия (H) – это полная энергия потока рабочего тела. Обычно используется удельная энтальпия h (кДж/кг), отнесенная к единице массы. Она равна сумме внутренней энергии тела u и произведению pv:
h = u + pv.
Произведение pv (кДж/кг) представляет собой потенциальную энергию потока («энергию проталкивания»).
Энтропия S является важной термодинамической функцией, которая меняется только при тепловом воздействии (нагреве или охлаждении) рабочего тела. Поскольку все энергетические потери в конечном итоге превращаются в теплоту, то она служит индикатором потерь, как в отдельных процессах, так и в целом за цикл. На диаграммах и в расчетах используется удельное, на единицу массы, значение этой величины s, кДж/(кг К).
Численные значения конкретных свойств веществ даются в таблицах или специальных программах расчёта свойств. Кроме этого свойства веществ наглядно отображаются в виде графиков или, как их называют, термодинамических диаграмм. Такие диаграммы широко используются для отображения процессов и циклов в холодильных установках и служат теоретической базой для приблизительных расчетов отдельных машин и аппаратов. Наибольшее распространение в холодильной технике получила диаграмма энтальпия-давление (h-ln p-диаграмма), которая была предложена Рихардом Молье и, которую называют диаграммой холодильщиков или диаграммой Молье. При анализе работы холодильных машин широко применяется диаграмма энтропия-температура (s-T-диаграмма), которая называется тепловой. Она удобна для анализа потерь и расчета термодинамической эффективности циклов. Две эти диаграммы для условного хладагента приведены на рисунках 2 и 3.
Диаграммы не только отображают свойства тел, но и позволяют наглядно изобразить процессы, протекающие в машине, понять их действие. Отображая на диаграмме круговой процесс (цикл), протекающий в конкретной холодильной машине, можно приблизительно оценить нагрузки на компрессор и аппараты, проанализировать процессы, протекающие при работе холодильной машины. Кроме того, при использовании диаграмм автоматически учитываются индивидуальные свойства того хладагента, диаграмма которого используется.
Когда требования к точности расчётов высокие, то свойства хладагентов определяются по таблицам или компьютерным программам. В остальных случаях для проектирования холодильных машин достаточно использования диаграмм.
На h-ln p и s-T-диаграммах центральное место занимает область парожидкостных состояний вещества. Из точки критического состояния вещества (т. К), находящейся в верхней части этой области, расходятся две пограничные кривые. Левая кривая называется кривой кипения (x=0), правая кривая называется кривой конденсации (x=1). Параметр x показывает относительную величину содержания пара. Эти кривые разделяют все поле диаграмм на три области: жидкого (Ж), парожидкостного (Ж+П) и газообразного состояния вещества (П).
|
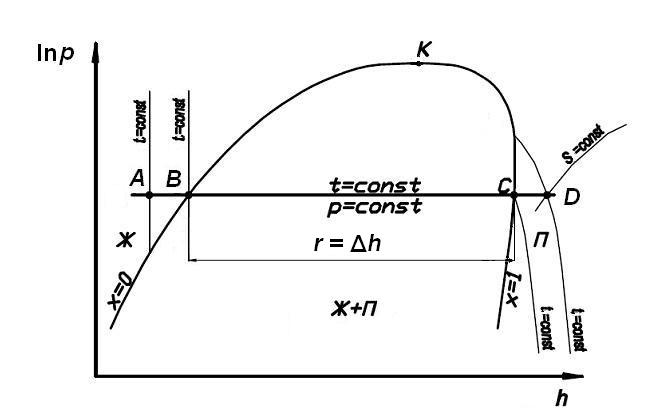
Рис. 2. h-ln p-диаграмма условного хладагента, A-D – изобарический процесс |
Если на h-ln p-диаграмме провести линию постоянного давления p = сonst (изобару), а на s-T-диаграмме линию постоянной температуры T = сonst (изотерму), то они пересекутся с пограничной кривой в точках B и C, которые носят названия насыщенных состояний, соответственно в т. B хладагент находится в состоянии насыщенной жидкости, а в т. C – насыщенного пара.
Испарение жидкого рабочего тела, т.е. фазовый переход жидкости в пар, на этих диаграммах сопровождается смещением точки, характеризующей состояние слева направо. При нагревании (A→B) жидкость сначала достигает состояния насыщения (т. B) и начинает кипеть. По мере подвода теплоты доля кипящей жидкости уменьшается, возрастает паросодержание, пока не достигнет состояния насыщенного пара (т. C). Состояние на линии насыщения со 100% паром называется сухой насыщенный пар (x=1), чтобы подчеркнуть разницу с состоянием влажного пара, когда в нем находятся, как правило в виде мелких капель, жидкость (область Ж+П, рис. 2 и 3). Энтальпия и энтропия рабочего тела всегда возрастают при подводе теплоты. Процесс нагрева пара (C→D) сопровождается повышением температуры.
|
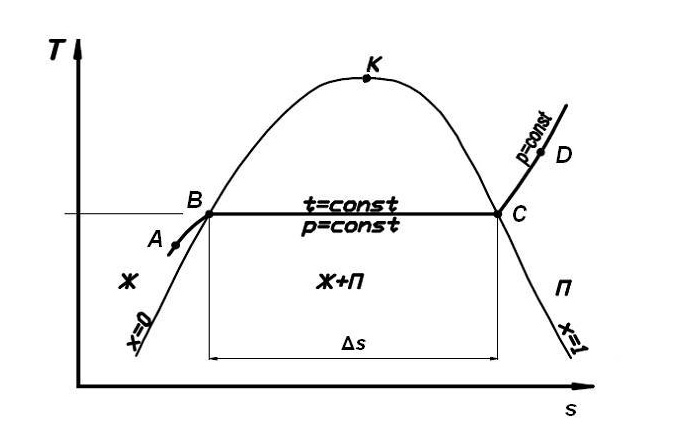
Рис. 3. s-T-диаграмма условного хладагента. A-D - изобара |
Конденсация пара, т.е. фазовый переход пара в жидкость на этих диаграммах идет противоположно, справа налево. Энтальпия и энтропия рабочего тела при отводе теплоты уменьшаются, перегретый пар сначала достигает состояния насыщения (т. C). В точке C начинается конденсация хладагента, которая заканчивается в т. B. Далее протекает процесс переохлаждения жидкости (B → A).
В процессах кипения и конденсации чистого вещества давление и температура остаются постоянными, а подводимая энергия (теплота) расходуется только на изменение агрегатного состояния хладагента. При этом температура кипения определяется только давлением. Эта температура возрастает при повышении давления и понижается при понижении давления. Это свойство веществ очень важно для регулирования работы парокомпрессионных холодильных машин.
В ПКХМ основные процессы протекают изобарически, при постоянном давлении, а количество теплоты, подведенное или отведенное в таких процессах равно изменению энтальпии. На h-ln p-диаграмме разность значений энтальпии h в точках B и C равна удельной «скрытой» теплоте испарения или конденсации. Эта величина обычно обозначается r (кДж/кг). На s-T-диаграмме величина r будет соответствовать площади под процессом B→C, т.к. r = ΔqB→C = TB·Δs.
Параметры, соответствующие состоянию хладагента на левой пограничной кривой, на линии насыщенного пара (x = 0), будем обозначать одним штрихом. Состояния хладагента на правой пограничной кривой, на линии насыщенной жидкости (x = 1) будем обозначать двумя штрихами. Таким образом:
![]()
Если при подводе теплоты жидкость полностью испаряется, то далее происходит «перегрев пара» и это состояние помечено символом D на диаграммах (рис. 2 и 3). Перегрев пара характеризуется разностью ΔTD=TD – TC.
Аналогично, если после окончания процесса конденсации C→B продолжить отводить теплоту, то дальнейший процесс B→A будет сопровождаться понижением температуры. Жидкость в т. A называется переохлажденной жидкостью. Мерой переохлаждения служит разность ΔTA= TB – TA. На h-ln p-диаграмме изотермы (T=const) в области жидкости идут почти вертикально вверх, т.е. совпадают с изоэнтальпами (h=const), в области парожидкостных состояний идут горизонтально, т.е. совпадают с изобарами (p=const), а в области пара эти линии по кривой резко уходят вниз (рис. 2). На этой же диаграмме линии постоянной энтропии (s=const) располагаются наклонно, примерно под углом 45° к горизонту.
На s-T-диаграмме (рис. 3) изотермы горизонтальны. Линии изобар (p=const) для жидкости идут резко вниз и почти совпадают с пограничной кривой (x=0), в парожидкостной области они горизонтальны и совпадают с изотермами, а в области пара – круто поднимаются вверх. Изоэнтальпы (h=const) составляют сложное семейство кривых, но, в основном, особенно в области парожидкостных состояний, они круто уходят вниз. Линии постоянной энтропии (s=const) вертикальны.
С небольшим подъемом к горизонтали идут на обеих диаграммах линии постоянного удельного объема (v=const). Большим давлениям p соответствует меньший удельный объем v.
Поясним, почему для расчёта и анализа ПКХМ удобно использовать h-ln p-диаграмму. Большинство процессов в холодильных машинах протекают на изобарах. При работе ПКХМ на установившемся режиме давления кипения (pи) и конденсации (pк) хладагента почти постоянны. Количество подводимой или отводимой теплоты в таких процессах равно разности энтальпий начала и конца процесса. Поэтому эта теплота количественно отображается в виде отрезка горизонтальной прямой на изобарах. При анализе циклов с использованием диаграмм автоматически учитываются индивидуальные свойства того хладагента, диаграмма которого используется. Все эти особенности h-ln p-диаграмм обуславливают широкое применение их при расчетах ПКХМ.
СХЕМА И ЦИКЛ ОДНОСТУПЕНЧАТОЙ ПАРОКОМПРЕССИОННОЙ ХОЛОДИЛЬНОЙ МАШИНЫ
Принципиальная схема одноступенчатой парокомпрессионной холодильной машины, включающая только основные аппараты и машины, необходимые для реализации этого цикла, была приведена на рис. 1. Ниже она приведена вновь (рис. 4) и на ней дополнительно проставлены характерные точки, которые помогут более подробно изучить процессы, протекающие в машине и построить рабочий цикл этой холодильной машины в h-ln p-диаграмме и s-T-диаграмме. Дополнительно цифрами 1", 2" и 3' на этой схеме обозначены характерные точки, лежащие на линии насыщения, т.е. соответствующие насыщенному состоянию хладагента.
На схеме (рис. 4) т. 1 соответствует состоянию перегретого пара на входе в компрессор. Этот перегрев защищает от случайного попадания жидкого хладагента в цилиндры компрессора. Это явление называется «гидравлический удар» или «влажный ход» и может привести к тяжёлой аварии компрессора, особенно если он поршневой. Для исключения этого явления пар перед компрессором несколько «перегревают». Процесс перегрева происходит:
- в испарителе;
- во всасывающем трубопроводе;
- в специальном теплообменнике-переохладителе;
- в электродвигателе компрессора;
- во всасывающей полости самого компрессора.
Изображение цикла в h-ln p-диаграмме приведено на рис. 5 и в s-T-диаграмме – на рис. 6. Процесс сжатия пара 1–2 реализуется в компрессоре. Давление пара повышается от давления кипения хладагента (pи) до давления конденсации (pк). Процесс сжатия показан как в идеальном компрессоре, без потерь. В этом случае процесс протекает по изоэнтропе (s=const), что хорошо видно на s-T-диаграмме (рис. 6). В реальном компрессоре процесс сжатия протекает с возрастанием энтропии. Современные методы позволяют учитывать потери в компрессоре, но это не сильно уточнит конечные результаты, а для простоты понимания удобнее пока опустить этот вопрос.
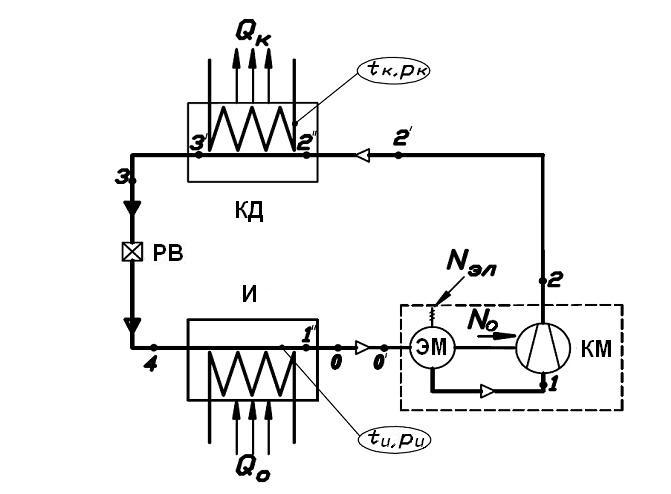
Рис. 4. Принципиальная схема парокомпрессионной холодильной машины с характерными точками цикла и процессов
После компрессора, в состоянии 2 температура хладагента в цикле наибольшая. Это состояние характеризуется как сильно перегретый пар при давлении конденсации (pк). Удельная работа сжатия в этом случае определяется как разность энтальпий в начале и конце процесса сжатия: ls = h2 – h1. Индекс s подчёркивает, что работа относится к изоэнтропному сжатию и поэтому ls называется изоэнтропной работой.
Для того чтобы осуществить процесс конденсации, необходимо сначала понизить температуру перегретого пара до температуры насыщенного пара (т. 2") при давлении pк. Процесс охлаждения пара называется «сбив перегрева» (процесс 2→2") и начинается он частично уже в нагнетательном тракте компрессора, а заканчивается в конденсаторе. Поэтому т. 2" показана «внутри» конденсатора (рис. 4) и служит границей между процессом сбива перегрева и процессом конденсации (процесс 2"→3').
|
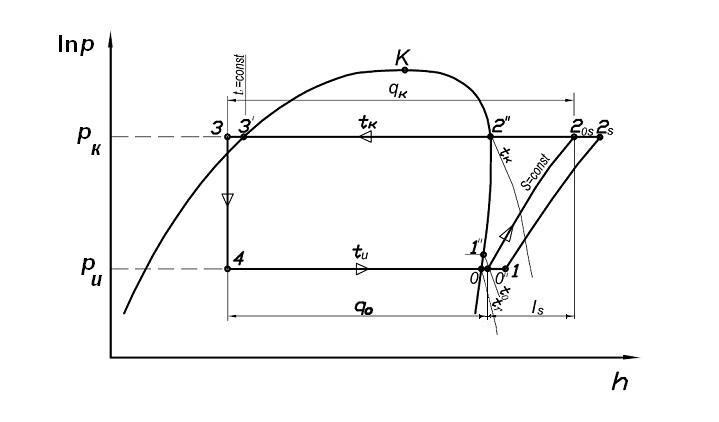
Рис. 5. Цикл одноступенчатой ПКХМ в h-ln p-диаграмме |
Процесс конденсации пара 2"→3' протекает при постоянном давлении pк и постоянной температуре tк. Он сопровождается выделением большого количества тепла в окружающую среду, омывающую конденсатор. Разность энтальпий в этих точках численно равна удельной теплоте конденсации rк= h2" - h3'. Обычно после конденсации жидкий хладагент здесь же, в конденсаторе, немного переохлаждается до более низкой температуры (процесс 3'→3). В расчёте обычно принимается, что все процессы в конденсаторе протекают при постоянном давлении pк. Считается, что процессы 2→2", 2"→3' и 3'→3 протекают в одном и том же аппарате, в конденсаторе, и поэтому удельная тепловая нагрузка на конденсатор равна qк = h2 - h3 [кДж/кг]. Для каждого из этих процессов в конденсаторе предусматривается своя, дополнительная теплообменная поверхность.
|
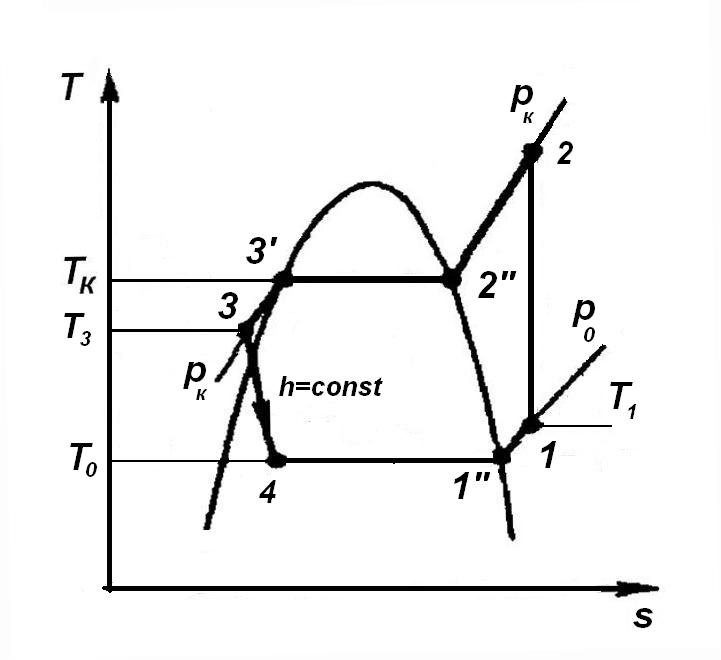
Рис. 6. Цикл одноступенчатой ПКХМ в s-T-диаграмме |
Переохлажденный жидкий хладагент (рис. 4) поступает в регулирующий вентиль, где осуществляется процесс дросселирования 3→4. При этом его давление падает от pк до pи, хладагент частично испаряется и за счёт этого его температура снижается от tк до tи. В процессе дросселирования внешняя работа над потоком хладагента не совершается, теплота не подводится и поэтому его энтальпия не меняется. В этом случае процесс протекает по изоэнтальпе (h=const), что хорошо видно на h-ln p-диаграмме (рис. 5).
Процесс кипения хладагента 4→1" протекает в испарителе при постоянном pи и включает процесс собственно кипения (процесс 4→1") и процесс небольшого перегрева (процесс 1"→1). Кипение протекает при постоянных pи и tи, т.е. является одновременно изобарическим и изотермическим, как и процесс конденсации. В процессах кипения (4→1") и перегрева (1"→1) энтальпия хладагента возрастает от h4 до h1. Величина q0 = h1 - h4 [кДж/кг] называется удельной холодопроизводительностью цикла. Она составляет полезный эффект работы холодильной машины. Работа в цикле подводится только в процессе сжатия (1→2) и она определяется как разность энтальпий в конечных точках l = h2 - h1 [кДж/кг]. Работа в реальных машинах затрачивается не только на сжатие газа, но и на функционирование вспомогательных механизмов. Однако для целей анализа и сравнения циклов холодильный коэффициент можно определять как:
![]() .
.
Сравнивая полученное значение εд с холодильным коэффициентом идеального цикла Карно, можно судить об эффективности конкретного цикла. Удельная теплота, отводимая в конденсаторе, равна сумме удельной холодопроизводительности и работе сжатия qк = q0 + l. Данное уравнение является записью закона сохранения энергии для этой холодильной машины.