
- •25. Теорія хімічної будови органічних сполук. Ізомерія.
- •26. Алкани. Будова , фізичні властивості. Ізомерія. Номенклатурні назви. Хімічні властивості , добування та застосування.
- •Добування алканів з природного газу та нафти.
- •2. Приєднання водню до алкенів та алкінів.
- •3. Взаємодія галогеналканів з металічним натрієм (реакція Вюрца).
- •4. Декарбоксилювання карбонових кислот
- •5. Добування метану.
- •27. Алкени. Будова молекули , фізичні і хімічні властивості. Правило Марковнікова, полімеризація. Ізомерія та номенклатурні назви. Добування та застосування
- •28. Алкіни, Гомологічний ряд , загальна формула. Будова молекули , фізичні і хімічні властивості. Правило Марковнікова, полімеризація. Ізомерія та номенклатурні назви. Добування та застосування .
- •29. Алкадієни . Гомологічний ряд , загальна формула. Будова молекули , фізичні і хімічні властивості. Правило Марковнікова, полімеризація. Ізомерія та номенклатурні назви. Добування та застосування .
- •30. Застосування та добування полімерів,канчуків , гуми.
- •31. Арени, склад, електронна та структурна формула,, фізичні властивості. Номенклатурні назви аренів. Хімічні властивості бензену. Застосування бензену. Хімічні засоби захисту рослин.
- •32. Нафта, склад, добування, застосування, перегонка нафти, крекінг нафтопродуктів.
- •33. Одноатомні спирти., будова молекули, фізичні властивості , класифікація. Ізомерія спиртів , номенклатурна назва. Хімічні властивості спиртів . Застосування та добування спиртів.
- •34. Багатоатомні спирти,фізичні властивості . Ізомерія спиртів , номенклатурна назва, хімічні властивості спиртів. Якісна реакція на багатоатомні спирти. Застосування та добування спиртів.
- •38. Естери, фізичні властивості. Ізомерія та номенклатурні назви естерів Добування та застосування естерів, Хімічні властивості естерів.
- •39. Жири,будова молекули, фізичні властивості, класифікація жирів. Ізомерія та номенклатурні назви жирів. Хімічні властивості жирів. Добування та застосування жирів. Значення жирів у життєдіяльності
- •40. Синтетичні миючі засоби, мило. Охорона довкілля від смз
- •41. Моносахариди. Глюкоза – альдегідо спирт, склад, будова молекули. Фізичні властивості. Хімічні властивості , якісна реакція . Поширення в природі, добування , застосування.
- •42. Дисахариди. Сахароза – дисахарид, склад та будова молекули, фізичні та хімічні властивості. Поширення в природі, застосування , загальна схема виробництва цукру.
- •43. Полісахариди. Крохмаль та целюлоза – полісахариди , склад та будова молекули, фізичні та хімічні властивості. Поширення в природі, застосування.
- •44. Аміни. Класифікація амінів. Склад і будова молекули, фізичні властивості. Ізомерія та номенклатура амінів. Хімічні властивості амінів. Добування та застосування.
- •45. Анілін. Ізомерія та номенклатура. Хімічні властивості, якісна реакція на анілін. Склад і будова молекули, фізичні властивості. Добування та застосування.
- •48. Волокна, класифікація .Способи добування волокон, застосування волокон.
39. Жири,будова молекули, фізичні властивості, класифікація жирів. Ізомерія та номенклатурні назви жирів. Хімічні властивості жирів. Добування та застосування жирів. Значення жирів у життєдіяльності
Жири — велика група органічних сполук, які, з фізичного погляду, мають меншу від одиниці питому вагу і, як правило, розчинні в органічних розчинниках, тому як правило не розчиняються у воді, і під звичайним тиском їх не можна перегнати, не розклавши.
Хімічні властивості жирів
1. Гідроліз жирів.
Як і у випадку естерів, гідроліз жирів проводять у присутності лугу (або соди), який перетворює утворені карбонові кислоти на солі. Причому солі вищих карбонових кислот, які при цьому утворюються, є милом, і внаслідок цього реакцію гідролізу (і не тільки жирів, але й естерів) незрідка називають також омиленням:
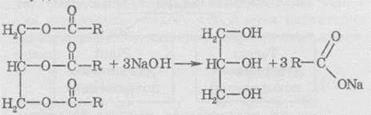
2. Гідрування жирів.
Оскільки до складу рідких жирів входять залишки ненасичених карбонових ,кислот, то вони здатні приєднувати молекули водню. Таким чином рідкі жири перетворюють у тверді. Цей процес дуже часто застосовують для добування комбінованих жирів та маргаринів.
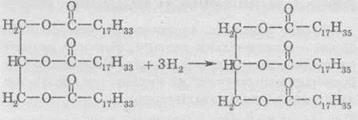
Як і будь-який процес гідрування, жири гідрують у присутності каталізатора — платини або нікелю при високому тиску водню. Одним з найбільш істотних недоліків цієї реакції є використання дорогих каталізаторів, невеликі кількості яких потім можуть входити до складу отриманих жирових сумішей. Пошук дешевих і нетоксичних каталізаторів — це одна з основних проблем виробництва жирових сумішей.
Фізичні властивості
Жири - в'язкі рідини або тверді речовини, легше води. Їх щільність коливається в межах 0,9-0,95 г/см3. У воді не розчиняються, але розчиняються в багатьох органічних розчинниках (бензол, дихлоретан, ефір і ін)
Класифікація
Чим більше в жирах вміст ненасичених кислот, тим нижче температура плавлення жирів.[3]
Агрегатний стан жирів |
Відмінності в хімічному складі |
Походження жирів |
Винятки |
Тверді жири |
Містять залишки насичених ЛКК |
Тваринні жири |
Риб'ячий жир(рідин та си. при н/в) |
Змішані жири |
Містять залишки насичених і ненасичених ЛКК |
||
Рідкі жири(масла) |
Містять залишки ненасичених ЛКК |
Рослинні жири |
Кокосове масло, какао масло(твердий. при н/в) |
Номенклатура
За тривіальною номенклатурою гліцериди називають, додаючи закінчення-ід до скороченій назві кислоти і приставку, яка показує, скільки гідроксильних груп в молекулі гліцерину проэтерифицировано.
Застосування жирів
Харчова промисловість (зокрема, кондитерська).
Фармацевтика
Виробництво мила і косметичних виробів
Виробництво мастильних матеріалів
40. Синтетичні миючі засоби, мило. Охорона довкілля від смз
Синтетичні миючі засоби (СМС) - це рідкі, пастоподібні і порошкоподібні речовини, які містять поверхнево-активні речовини, а також інші органічні і неорганічні речовини, що підвищують ефективність поверхнево-активних речовин. Основне призначення миючих засобів - видалення забруднень з різних поверхонь. Забруднення міцно утримуються на них за рахунок фізико-хімічних сил, не змочуються водою і тому практично нею не змиваються. Щоб перевести забруднення в розчин, слід зробити їх гідрофільними (змочують). Молекули миючих речовин, адсорбируясь на грязьовий частці, «притягають» її до води, відривають від поверхні перешкоджають зворотному прилипанню та злипанню частинок між собою. Таким чином, частки переходять в розчин. Так як розчин поверхнево-активних речовин краще змочує поверхні, він проникає в найдрібніші пори і руйнує великі частки забруднень.
Всі синтетичні миючі засоби є органічними сполуками. Вони мають односторонньо розташовану углеводородную ланцюг і групу, що бере участь в реакціях. Основною складовою частиною СМС є органічні поверхнево-активні речовини, що володіють смачивающей, емульгує, пептізірующей і пенообразующей здатністю. Сукупність цих властивостей обумовлює їх миючу дію. ПАР, використовувані для виробництва СМС, поділяються на іоногені, диссоциирующие у водних розчинах на іони, і неіоногенні. Найбільш поширені аніоноактівние речовини (алкілсульфати, алкілсульфонати і алкіларілсульфонати), які розпадаються у водних розчинах на аніони (більші негативно заряджені частинки) і катіони (дрібні позитивно заряджені іони, як правило, натрію або калію). Великі за розміром аніони забезпечують поверхнево-активні властивості. Всі аніоноактівние ПАР є кристалічні речовини, розчинні у воді. Зміст їх в СМС складає від 10 до 40%.
ОПИС
ТЕХНОЛОГІЧНОГО ПРОЦЕСУ
СМС
випускають у формі порошку, рідини або
пасти. Технологія приготування полягає
в складанні композиції, змішуванні і
розчиненні всіх компонентів рецептури.
Для отримання порошкоподібних засобів
використовують сушку. Далі слід розфасовка
і упаковка готового
продукту.
Приготування композиції
полягає у змішуванні поверхнево-активних
речовин з необхідними за рецептурою
добавками. Щоб знизити витрати на
випаровування води, для порошкоподібних
засобів готують найбільш концентровані
композиції (до 50-60% сухої речовини),
фактично представляють собою суспензії.
Потім композиції фільтрують і пропускають
через колоїдну млинок для додання
однорідності. Сушіння полягає в розпиленні
розчину в сушильній башті під тиском
до 50 атм і температурі 250-350 ![]() З.
При такому способі порошки одержують
у гранульованому вигляді. Основна
кількість порошкоподібних СМС проводиться
методом високотемпературної розпилювальної
сушки, що забезпечує отримання
гранульованого продукту високої якості.
З.
При такому способі порошки одержують
у гранульованому вигляді. Основна
кількість порошкоподібних СМС проводиться
методом високотемпературної розпилювальної
сушки, що забезпечує отримання
гранульованого продукту високої якості.
ОБЛАСТЬ ЗАСТОСУВАННЯ Синтетичні миючі засоби є найбільш широко вживаними засобами побутової хімії. Перший синтетичний порошок «Новина» був випущений в 1953 році на основі продуктів, виділених з китового саломас. Сучасний асортимент синтетичних миючих засобів досить великий. Підбір доцільного складу (композиції) синтетичного миючого засобу дозволяє легко виробляти миючі препарати найрізноманітнішого призначення. Засоби кожного підродини випускають порошкоподібними, рідкими і у вигляді паст. Близько 85% всього виробництва синтетичних миючих засобів припадає на частку порошкових засобів, приблизно 15% випуску складають рідкі та пастоподібні препарати. Дані опитування покупців показують, що ѕ всіх сімей користуються в даний час в основному порошковими синтетичними миючими засобами, близько 14% використовують пасти і тільки 10% споживачів застосовують рідкі миючі засоби. Малий попит на рідкі та пастові миючі засоби пояснюється в основному поганою рекламою. Покупець не завжди належним чином поінформований про переваги цих миючих засобів: легкості дозування, хорошою розчинності. Приблизно 45% всіх СМС для побуту складають універсальні синтетичні миючі засоби, стільки ж - кошти для прання бавовняних і лляних тканин і лише 10% випуску припадає на частку СМС, застосовуваних для прання виробів з вовни, шовку і хімічних волокон. Останнім часом намітилася тенденція збільшення виробництва синтетичних миючих засобів комбінованої дії, що забезпечують, крім прання, дезінфекцію, підфарбовування, пом'якшення, антистатична дія. З кожним роком зростає також випуск синтетичних миючих засобів, що містять ферменти, що полегшують видалення білкових забруднень (кошти з біоеффектом).
Ми́ло — розчинна у воді мийна речовина; як хімічний продукт являє собою відносно складне з'єднанняжирних кислот з лугами, а за своєю будовою відноситься до класу солей. Випускається в твердому стані, рідкому, а також у вигляді порошку і гранул.
Технологія виготовлення
Мило ручної роботи з екстрактом кропиви
Головною складовою твердого мила є суміш розчинних солей вищих жирних кислот. Зазвичай це натрієві, рідше - калієві чи амонієві солі стеаринової, пальмітинової, міристинової, лауринової чи олеїнової кислот. Додатково в складі можуть буть: наповнювачі, барвники, ароматизатори, дезинфікуючі та лікувально-профілактичні додатки (борна кислота, тимол,гліцерин, хна, ланолін, дьоготь березовий, сірка, спермацет, гексаметафосфат та ін.). Важливими якостями мила є: розчинність в воді, мийна здатність, мило має не швидко стиратись та добре пінитись.
Мило виготовляють кип'ятінням у воді жирів з лугами: гідроксид натрію (каустична сода), гідроксид калію. Жири виділяють з продуктів рослинного походження: (бавовникова, пальмова чи соєва олії), а також з тваринних продуктів: свинячого сала, яловичого чи баранячого жиру, риб'ячого жиру. Під час кип'ятіння жирів з лугами утворюється гліцеринта солі жирних кислот (мило). Натрієві мила густіші і, як правило, тверді; калійні мила м'якші, або взагалі рідкі. Подальший етап виготовлення включає очищення мила від залишку солей, лугів та гліцерину. До туалетних мил додають барвники, ароматизатори, інертний наповнювач (каолін) тощо. Господарське мило містить невелику кількість надлишкового лугу.
