
- •3Принципы построения, структура и содержание клинического диагноза.
- •Сердечно-сосудистая система
- •1. Острая ревматическая лихорадка: этиология, патогенез, классификация, клиническая картина, принципы лечения, принципы первичной профилактики.
- •2. Хроническая ревматическая болезнь сердца: понятие, диагностика, вторичная профилактика.
- •3.Недостаточность митрального клапана: этиология, изменение гемодинамики, клиника, диагностика.
- •4. Митральный стеноз: этиология, изменение гемодинамики, клиника, диагностика.
- •5.Недостаточность аортального клапана: этиология, изменение гемодинамики, клиника, принципы диагностики.
- •6.Стеноз устья аорты: этиология, изменение гемодинамики, клиника, диагностика.
- •7.Показания к оперативному лечению приобретенных пороков сердца, возможные варианты оперативных вмешательств.
- •8.Инфекционный эндокардит: этиология, патогенез, клиника, диагностика.
- •9.Принципы лечения инфекционного эндокардита.
- •10. Впс: дефект межжелудочковой перегородки: клиника, диагностика, лечение.
- •11. Впс: дефект межпредсердной перегородки: клиника, диагностика, лечение.
- •Расположение дефекта может быть различным, и на основании этого выделяют
- •3 Основных типа.
- •12. Впс: коарктация аорты: клиника, диагностика, тактика лечения.
- •13. Впс: открытый артериальный проток: клиника, диагностика, лечения.
- •14. Факторы риска сердечно-сосудистых заболеваний (модифицируемые и нет), первичная профилактика сердечно-сосудистых заболеваний.
- •15.Гипертоническая болезнь — заболевание, характеризующееся
- •16. Классификация гипертонической болезни.
- •17. Гипертонические кризы. Гк- внезапное повышение
- •18. Гипертонический криз: клиническая картина, объем лечебных
- •20. Классификации ишемической болезни сердца. Факторы
- •21. Стенокардия. Определение. Классификация.
- •22. Клинические проявления стенокардии. Диагностика.
- •23. Принципы терапии стабильной стенокардиии.
- •24. Острый коронарный синдром. Включающий острый инфаркт
- •25. Нестабильная стенокардия. Понятие. Современные методы
- •26. Современные подходы к медикаментозному лечению ибс. 1.Среди нитратов в настоящее время наиболее широко используют
- •27. Показания к оперативному лечению ибс.
- •28. Инфаркт миокарда. Этиология. Клиника.
- •29. Клинические формы им. Особенности диагностики.
- •30.Периоды течения инфаркта миокарда. Клинические и лабораторные
- •32. Ранние осложнения им: клиника, диагностика, лечение
- •33. Поздние осложнения им: клиника, диагностика, лечение.
- •34. Неотложная терапия больных с острым инфарктом миокарда
- •35. Острая левожелудочковая и левопредсердная недостаточность
- •36. Острая правожелудочковая недостаточность
- •38. Хсн: этиология, классификация, клиника
- •39. Хсн: современные подходы к лечению
- •40. Неревматические миокардиты: этиология, патогенез, клиника, принципы лечения.
- •41. Неревматические миокардиты: классификация, критерии диагностики
- •Диагностика
- •42. Нарушения ритма сердца: причины, патогенез, клиника
- •43. Принципы диагностики нарушений сердечного ритма
- •Симптомы синусовой тахикардии
- •Лечение синусовой тахикардии
- •45. Экстрасистолия
- •46.Нарушения проводимости сердца: классификация, диагностика Классификация
- •47.Нарушения проводимости сердца: этиология, клиника Этиология
- •48. Фибрилляция предсердий. Этоиология
- •Классификация
- •Электрическая кардиоверсия
- •Фармакологическая кардиоверсия
- •52.Кардиомиопатии: определение, классификация, методы диагностики.
- •53.Дилатационная кардиомиопатия: клиника, диагностика, принципы лечения.
- •56.Симптоматические артериальные гипертонии: классификация, особенности обследования пациента с целью исключения почечной этиологии артериальной гипертонии
- •57.Реноваскулярная артериальная гипертония: этиология, особенности клинической картины, диагностика, методы лечения.
- •58.Роль инструментальных методов в диагностике заболеваний сердечно-сосудистой системы
- •59.Принципы лечебного питания при заболеваниях сердечно-сосудистой системы.
- •3.Пневмонии: этиология, классификация, клиника, диагностика.
- •Критерии компенсации углеводного обмена при сахарном диабете
- •7.Поздние осложнения сахроного диабета:классификация,диагностика и лечение
- •8.Принципы лечения сд 1 типа . Лечение Общие принципы
- •Инсулинотерапия
- •9.Принципы лечения сд 2 типа. Основные принципы лечения сахарного диабета 2-го типа
- •10.Особенности диетотерапии при сд 1 и 2 типов. Показания и противопоказания к физическоим нагрукам . Диета при диабете 1 типа
- •Диета при диабете 2 типа
- •Диета «Стол № 9» при диабете
- •I. Препараты, способствующие снижению инсулинорезистентности
- •III. Препараты, снижающие всасывание глюкозы в кишечнике.
- •IV. Инсулины и аналоги инсулинов
- •31.Гиперпаратиреоз: классификация, этиология, клиническая картина, диагностика, лечение.
- •32.Гипопаратиреоз: этиология, клиника, диагностика, лечение.
- •33.Феохромоцитома: этиология, классификация, клиника, диагностика, лечение.
- •34.Первичный альдостеронизм: этиология, клиника, диагностика, лечение.
- •35.Болезнь и синдром Иценко-Кушинга: этиология, клиника, диагностика, принципы лечения
- •36.Хроническая недостаточность надпочечников: классификация, клиника, диагностика, лечение.
- •37.Острая надпочечниковая недостаточность: провоцирующие факторы, клиническая картина, неотложная помощь.
- •38.Ожирение: классификация, методы диагностики, принципы лечения. Понятие о метаболическом синдроме.
- •1. Алиментарно-конституциональное (экзогенно-конституциональное)
- •2. Симптоматическое ожирение
- •Анемии: классификация. Методы диагностики гематологических заболеваний).
- •2.Хронические железодефицитные анемии: этиология, клиника, диагностика, лечение.
- •4.Гипо- и апластические анемии: этиология, клиника, диагностика, лечение.
- •5.Острые лейкозы: классификация, клиника, диагностика, принципы терапии.
- •6.Хронические лейкозы: классификация, клиника, диагностика, лечение.
- •7.Геморрагические диатезы: классификация, типы кровоточивости.
- •8.Гемофилии: классификация, этиология, клиника, диагностика, лечение.
- •9.Тромбоцитопатии: понятие, этиология, клиника, лабораторная диагностика, лечение
- •Хронический гастрит: этиология, классификация, принципы диагностики.
- •Хеликобактерный гастрит: клиника, диагностика, лечение.
- •Атрофический гастрит: этиология, патогенез, клиника, диагностика, лечение.
- •Язвенная болезнь желудка: этиология, патогенез, клиника, диагностика.
- •Язвенная болезнь двенадцатиперстной кишки: этиология, патогенез, клиника, диагностика, лечение
- •6. Современные подходы к терапии язвенной болезни.
- •7.Рак желудка: факторы риска, клиническая картина, диагностика, лечение.
- •8.Хронические гепатиты: классификация, клиническая картина, принципы диагностики.
- •9.Принципы диагностики и лечения хронических гепатитов.
- •2. Диагностические критерии и принципы лечения системной склеродермии.
- •3.Диагностические критерии и принципы лечения дерматомиозита.
- •4.Диагностические критерии ревматоидного артрита. Современные принципы лечения.
- •6.Гюкокортикостероиды и цитостатики, применяемые в ревматологии: показания, нежелательные и побочные явления ,профилактика осложнений.
- •Ниже приведены показания к интенсивной терапии у больных ревматоидным артритом
- •Общая физиотерапия
- •Физиотерапия ( определение, предмет, классификация природных лечебных факторов).
- •Техника безопасности в физиотерапии, принципы применения лечебных факторов.
- •Постоянный ток (гальванизация, электрофорез, постоянный импульсивный ток)…
- •Переменный ток (амплипульстерапия, дарсонвализация, увч), механизм действия, показания к применению.
- •Лазеротерапия: механизм действия, показания к применению.
- •Применение ультразвука с лечебной целью, механизм действия, показания.
- •Светотерапия: механизм действия, показания.
- •Водолечение. Способы, механизм действия, показания к применению.
- •Теплолечения. Способы, механизм действия, показания к применению.
- •Принципы и основные технические приемы массажа, механизм действия, показания к применению.
- •Курорты Краснодарского края и их лечебные факторы.
- •Профпатология
- •Понятия о профпатологии как клинической дисциплины, ее предмет и задачи.
- •Юридические основы диагностики профессиональных заболеваний (необходимые документы)
- •3.Профилактические (предварительные и периодические) медицинские осмотры рабочих промышленных предприятий и сельскохозяйственных производств, их цели и задачи.
- •4.Врачебно-трудовая экспертиза при профессиональных заболеваниях.
- •5.Методы реабилитации профессиональных заболеваний.
- •6.Пневмокониозы от высоко и умеренно фиброгенной пыли (Силикоз): этиопатогенез, клиника, лечение, профилактика.
- •7.Пневмокониозы от низко фиброгенной пыли (силикатозы): патогенез, клиника, лечение, профилактика.
- •8.Пылевой бронхит. Этиопатогенез, клиника, лечение, профилактика.
- •9.Профессиональные заболеваний аллергической природы (бронхиальная астма, экзогенные аллергические альвеолиты):этиопатогенез, клиника, лечение, профилактика.
- •10.Пневмокониозы. Классификация, клиника, лечение, профилактика.
- •11.Экзогенный аллергический альвеолит профессиональной этиологии, причины развития, клиника, диагностика, лечение, профилактика.
- •12.Вибрационная болезнь. Этиопатогенез, классификация, диагностика, клинические проявления, принципы лечения, профилактики.
- •13.Профессиональные болезни опорно-двигательного аппарата, обусловленные физическим перенапряжением и микротравматизацией.
- •14.Интоксикация свинцом и его соединениями, этиопатогенез, клиника, лечение, профилактика.
- •15.Интоксикация фосфорорганическими соединениями: клиника, лечение, профилактика.
- •16.Интоксикация хлорорганическими и ртутьорганическими соединениями: клиника, лечение, профилактика.
- •17.Неотложная помощь при острых профессиональных отравлениях.
- •18.Профессиональные заболевания у медицинских работников.
3.Пневмонии: этиология, классификация, клиника, диагностика.
Пневмония (П) — острое инфекционное поражение нижних отделов дыхательных путей, подтвержденное рентгенологически, доминирующее в картине болезни и не связанное с другими известными причинами.
В определении П подчеркивается острый характер воспаления, поэтому нет необходимости употреблять термин «острая пневмония» (в Международной классификации болезней, принятой Всемирной организацией здравоохранения, рубрика «острая пневмония» отсутствует).
В зависимости от эпидемиологической обстановки заболеваемость пневмонией в России колеблется от 3 — 5 до 10— 14 на 1000 населения.
Классификация. До последнего времени в нашей стране пользовались классификацией острой пневмонии (ОП), предложенной Е.В. Гем-бицким и соавт. (1983), являющейся модификацией классификации, разработанной Н.С. Молчановым (1962) и утвержденной XV Всесоюзным съездом терапевтов. В этой классификации выделяют следующие рубрики.
Этиология: 1) бактериальные (с указанием возбудителя); 2) вирусные (с указанием возбудителя); 3) орнитозные; 4) риккетсиозные; 5) микоплазменные; 6) грибковые (с указанием вида); 7) смешанные; 8) аллергические, инфекционно-аллергические; 9) неустановленной этиологии.
Патогенез: 1) первичные; 2) вторичные. Клинико-морфологическая характеристика: 1) паренхиматозные:
а) крупозные, б) очаговые; 2) интерстициальные.
Локализация и протяженность: 1) односторонние; 2) двусторонние (1 и 2 с указанием протяженности).
Тяжесть: 1) крайне тяжелые; 2) тяжелые; 3) средней тяжести; 4) легкие и абортивные.
Течение: 1) острые; 2) затяжные.
I. Внебольнично приобретенная пневмония.
И. Внутрибольнично приобретенная (госпитальная или нозокомиаль-ная) пневмония.
Пневмония при иммунодефицитных состояниях.
Атипично протекающие пневмонии.
При внебольничных пневмониях в 80 — 90 % случаев возбудителями являются Streptococcus pneumoniae, Haemophilus influenzae, Mycoplasma pneumoniae, Moraxella catarrhalis.
Среди наиболее распространенных возбудителей П по-прежнему главным остается пневмококк. Реже возбудителем П является клебсиелла (палочка Фридлендера), Chlamidia psittaci.
Для внутрибольничных (нозокомиальных) пневмоний характерно большое разнообразие этиологических агентов, включающих грамотрицательную флору (энтеробактерии, синегнойная палочка, ацинетобактер), золотистый стафилококк и анаэробы.
Интоксикационный (общая слабость, разбитость, головные и мы шечные боли, одышка, сердцебиение, бледность, снижение аппетита).
Синдром общих воспалительных изменений (чувство жара, озноб, повышение температуры тела, изменение острофазовых показате лей крови: лейкоцитоз со сдвигом лейкоцитарной формулы влево, увеличение СОЭ, уровня фибриногена, аг-глобулинов, появление С-реактивного белка — СРБ).
Синдром воспалительных изменений легочной ткани (появление кашля и мокроты, укорочение перкуторного звука), усиление голо сового дрожания и бронхофонии, изменение частоты и характера дыхания, появление влажных хрипов, характерные рентгенологи ческие изменения).
Синдром вовлечения других органов и систем (сердечно-сосудистой системы, пищеварительного тракта, почек, нервной системы).
Наиболее важным методом, позволяющим уточнить наличие пневмонии и степень вовлечения в процесс легочной ткани, является рентгенологическое исследование органов грудной клетки. Крупнокадровая флюорография и рентгенография в двух проекциях, производимая в динамике, помогают (с учетом клинической картины) с достоверностью поставить диагноз пневмонии.
Иногда по характеру рентгенологических изменений можно с определенной долей вероятности судить о возбудителе, вызвавшем пневмонию. Четкой сегментарностью поражения легких с вовлечением в процесс нескольких сегментов (в 60 % случаев двустороннее поражение) отличаются стафилококковые пневмонии. Характерным рентгенологическим признаком их является образование на 5 —7-й день от начала болезни множественных полостей в легких типа пневмоцеле, а в дальнейшем — некротических полостей с наличием жидкости. В отличие от истинных абсцессов конфигурация и количество полостей быстро меняются.
Для выявления П, протекающих с выраженными клиническими проявлениями, но без четких рентгенологических данных, следует проводить компьютерную томографию легких, при которой удается выявить инфильтрацию легочной ткани.
Бронхография позволяет выявить полости распада в легочной ткани, а также наличие бронхоэктазов, вокруг которых при обострении возможны инфильтративные изменения (так называемая перифокальная пневмония). Дифференциальную диагностику проводят с туберкулезом и раком легкого по результатам бронхоскопии, а при необходимости и плевро-скопии.
В диагностике инфарктной пневмонии определенную роль играет ра-дионуклидное исследование легочного кровотока, выявляющее его нарушения.
Бактериологическое исследование мокроты (или бронхиальных смывов) до назначения антибиотиков помогает обнаружить возбудитель и определить его чувствительность к антибиотикам.
Особенно важно исследование бронхиального смыва в диагностике П пневмоцистной этиологии.
Не всегда выявленный микроорганизм является возбудителем пневмонии. Уточненный этиологический диагноз может быть поставлен с помощью иммунологических исследований, реакции связывания комплемента (РСК) и реакции торможения гемагглютинации (РТГА) с вирусными и бактериальными антигенами.
В диагностике вирусных и вирусно-бактериальных пневмоний имеют значение вирусологические и серологические исследования (результаты культурального исследования мокроты, включая биологическую пробу на мышах, метод культивирования вирусов в развивающемся курином эмбрионе, метод иммунофлюоресценции, серологический метод с использованием парных сывороток против вирусов и Mycoplasma pneumoniae, причем придают значение лишь 4-кратному нарастанию титра антител).
Все эти сложные иммунологические, вирусологические и серологические методы обязательно применяют при обследовании больных, не поддающихся общепринятой терапии, в случае атипичного течения пневмонии или развития тяжелых осложнений.
Исследование мокроты помогает уточнить природу пневмонии. Большое число эозинофилов свидетельствует об аллергических процессах, наличие атипических клеток — о пневмонии ракового генеза; микобактерии туберкулеза обнаруживают при туберкулезе; эластические волокна являются свидетельством распада легочной ткани (рак, туберкулез, абсцесс). При микозных пневмониях наряду с обнаружением грибов отмечается отсутствие гноеродной флоры вследствие угнетающего действия продуктов жизнедеятельности грибов.
По данным бактериоскопии (микроскопия мазков мокроты, окрашенных по Граму) можно говорить о грамотрицательных или грамположи-тельных микроорганизмах, обитающих в бронхах уже в первые сутки пребывания больного в стационаре (важно учитывать при выборе антибиотиков).
Об остроте воспалительного процесса можно судить по выраженности острофазовых показателей крови и их динамике (лейкоцитоз со сдвигом лейкоцитарной формулы, увеличение СОЭ, повышенное содержание ссг-глобулинов, фибриногена, появление СРБ, повышение уровня сиаловых кислот). Для бактериальных пневмоний более характерен ней-трофильный лейкоцитоз со сдвигом лейкоцитарной формулы влево; СОЭ увеличена, степень этого увеличения определяется распространенностью и тяжестью процесса. Вирусные пневмонии отличает лейкопения. При микоплазменных и орнитозных пневмониях лейкопения сочетается с очень высокой СОЭ. Как правило, отмечается тенденция к лейкопении при парагриппозных и аденовирусных пневмониях, но СОЭ в этих случаях нормальная.
При затяжном течении пневмонии и развитии осложнений необходимо изучение иммунологической реактивности организма. Снижение показателей гуморального (IgM) и клеточного (задержка миграции лейкоцитов, изменение тестов, характеризующих систему Т-лимфоцитов) иммунитета требует проведения иммуномодулирующей терапии.
Лабораторные и инструментальные методы имеют дополнительное значение в уточнении степени вовлечения в процесс других органов и систем и развития осложнений:
ЭКГ позволяет оценить состояние миокарда; иногда возникает не обходимость использовать с этой целью и эхокардиографию;
эхокардиография помогает обнаружить выпот в перикарде или бактериальные колонии на клапанах сердца при осложнении инфекцион ным эндокардитом;
показатели функции внешнего дыхания позволяют оценить состоя ние бронхиальной проходимости.
4.Атипичные пневмонии: особенности диагностики.
Атипичные П (вызваны атипичными возбудителями и имеют атипичную клиническую картину) более характерны для молодежи (школьники, студенты, солдаты) и часто носят характер эпидемической вспышки.
Атипичные пневмонии характеризуются лихорадкой, головной болью и появлением непродуктивного кашля. Поражению нижних отделов дыхательных путей предшествуют симптомы поражения верхних: боль в горле, потеря голоса и кашель, который периодически носит пароксизмальный характер, нарушая сон.
5.Современные принципы лечения внебольничных пневмоний.
I. Лечебный режим и рациональное питание.
II. Лекарственную терапию: 1) этиотропную, 2) патогенетическую, 3) симптоматическую.
Физиотерапевтическое воздействие.
Диспансерное наблюдение.
Лечение внебольнично приобретенных пневмоний легкого или средне-тяжелого течения, протекающих без осложнений, у лиц молодого возраста (при отсутствии сопутствующих заболеваний) можно проводить в домашних условиях. Следует назначать препараты новой генерации макроли-дов — азитромицин (сумамед), рокситромицин (рулид). Сумамед назначают коротким 3-дневным курсом по 500 мг 1 раз в день или 5-дневным курсом: в 1-й день 500 мг, а затем по 250 мг 1 раз в день в течение 4 дней. Рулид назначают по 150 мг 2 раза в день в течение 5 — 7 дней.
• Патогенетическая терапия. При тяжелых и затяжных пневмониях используют препараты иммуномодулирующего дейст вия (интерферон, левамизол, зимозан, диуцифон, Т-активин, тима- лин).
Больным вирусной пневмонией показаны введение противогриппозного у-глобулина, противовирусных препаратов (рибоварин, интерферон), ингаляции фитонцидов [сок чеснока и(или) лука, приготовленные ex tem-рогае, в изотоническом растворе хлорида натрия].
При стафилококковой пневмонии проводят пассивную иммунизацию гипериммунной антистафилококковой плазмой или стафилококковым антитоксином.
Для восстановления неспецифической резистентности организма назначают витамины А, С, Е, группы В, используют биогенные стимуляторы и адаптогенные средства (алоэ, настойки женьшеня и лимонника, жидкий экстракт элеутерококка).
Для восстановления бронхиальной проходимости применяют бронхо-литические средства (эуфиллин, теопэк и пр.) и средства, разжижающие бронхиальный секрет (внутрь мукалтин, ацетилцистеин, бромгексин, горячее щелочное питье). Если наблюдается надсадный кашель как проявление бронхоспазма, сопутствующего П, назначают адреномиметические средства: фенотерол (беротек), сальбутамол.
При затяжном течении пневмонии иногда решающую роль играет восстановление бронхиального дренажа с помощью бронхоскопической санации.
• Симптоматическая терапия. При непродуктивном сухом кашле назначают противокашлевые средства (кодеин, либек- син, тусупрекс, глауцина гидрохлорид и пр.); при затрудненном от- хождении мокроты — отхаркивающие (настой травы термопсиса, корень алтея и пр.). В случае плохой переносимости высокой тем-
пературы тела показаны жаропонижающие средства (анальгин, ацетилсалициловая кислота). Больным с сопутствующей патологией сердечно-сосудистой системы, особенно пожилым, а также при тяжелом течении пневмонии назначают инъекции камфоры, сульфо-камфокаина, кордиамина, при недостаточности кровообращения — сердечные гликозиды.
Наличие одышки и цианоза служит показанием к проведению кислородной терапии. При выраженной интоксикации и деструкции легочного инфильтрата проводят дезинтоксикационную терапию (внутривенное введение реополиглюкина, гемодеза и других растворов).
Больным с тяжелой формой пневмонии, с выраженной интоксикацией, инфекционно-токсическим шоком показано внутривенное введение кортикостероидов. Небольшие дозы кортикостероидов (10—15 мг в день) внутрь назначают при вялом рассасывании инфильтрата или сопутствующем аллергическом бронхоспазме.
III. Физиотерапевтическое воздействие. При лечении больных П используют отвлекающие процедуры: банки, горчичники, горчичные обер тывания, которые при невысокой температуре тела принимают с первых дней болезни. После снижения температуры тела для ликвидации воспа лительных изменений назначают диатермию, индуктотермию, СВЧ, УВЧ и т.д. Рассасыванию очага пневмонии способствуют массаж грудной клет ки и ЛФК.
Аэрозольтерапия с использованием бронхолитических смесей отдельно или в комбинации с различными антибактериальными препаратами применяется в стадии разрешения.
6.Современные принципы лечения внутрибольничных пневмоний.
I. Лечебный режим и рациональное питание.
II. Лекарственную терапию: 1) этиотропную, 2) патогенетическую, 3) симптоматическую.
Физиотерапевтическое воздействие.
Диспансерное наблюдение.
При лечении нозокомиальных (внутрибольничных) пневмоний с учетом наиболее частых ее возбудителей (синегнойная палочка, золотистый стафилококк, энтеробактер) на первое место выходят цефалоспорины второй — третьей генерации, в том числе фортум, фторхинолоны, имипенем (см. табл. 3). Цефтазидим (фортум) — цефалоспорин, устойчивый к действию большинства бета-лактамаз и обладающий высокой активностью в отношении широкого спектра грамположительных, грам-отрицательных бактерий и синегнойной палочки. Препарат вводят парентерально по 500 мг— 1 г каждые 8 или 12 ч в зависимости от выраженности инфекции, возраста, массы больного и функции почек. При присоединении грибковой инфекции применяют амфотерицин В и ни-зорал.
• Патогенетическая терапия. При тяжелых и затяжных пневмониях используют препараты иммуномодулирующего дейст вия (интерферон, левамизол, зимозан, диуцифон, Т-активин, тима- лин).
Больным вирусной пневмонией показаны введение противогриппозного у-глобулина, противовирусных препаратов (рибоварин, интерферон), ингаляции фитонцидов [сок чеснока и(или) лука, приготовленные ex tem-рогае, в изотоническом растворе хлорида натрия].
При стафилококковой пневмонии проводят пассивную иммунизацию гипериммунной антистафилококковой плазмой или стафилококковым антитоксином.
Для восстановления неспецифической резистентности организма назначают витамины А, С, Е, группы В, используют биогенные стимуляторы и адаптогенные средства (алоэ, настойки женьшеня и лимонника, жидкий экстракт элеутерококка).
Для восстановления бронхиальной проходимости применяют бронхо-литические средства (эуфиллин, теопэк и пр.) и средства, разжижающие бронхиальный секрет (внутрь мукалтин, ацетилцистеин, бромгексин, горячее щелочное питье). Если наблюдается надсадный кашель как проявление бронхоспазма, сопутствующего П, назначают адреномиметические средства: фенотерол (беротек), сальбутамол.
При затяжном течении пневмонии иногда решающую роль играет восстановление бронхиального дренажа с помощью бронхоскопической санации.
• Симптоматическая терапия. При непродуктивном сухом кашле назначают противокашлевые средства (кодеин, либек- син, тусупрекс, глауцина гидрохлорид и пр.); при затрудненном от- хождении мокроты — отхаркивающие (настой травы термопсиса, корень алтея и пр.). В случае плохой переносимости высокой тем-
пературы тела показаны жаропонижающие средства (анальгин, ацетилсалициловая кислота). Больным с сопутствующей патологией сердечно-сосудистой системы, особенно пожилым, а также при тяжелом течении пневмонии назначают инъекции камфоры, сульфо-камфокаина, кордиамина, при недостаточности кровообращения — сердечные гликозиды.
Наличие одышки и цианоза служит показанием к проведению кислородной терапии. При выраженной интоксикации и деструкции легочного инфильтрата проводят дезинтоксикационную терапию (внутривенное введение реополиглюкина, гемодеза и других растворов).
Больным с тяжелой формой пневмонии, с выраженной интоксикацией, инфекционно-токсическим шоком показано внутривенное введение кортикостероидов. Небольшие дозы кортикостероидов (10—15 мг в день) внутрь назначают при вялом рассасывании инфильтрата или сопутствующем аллергическом бронхоспазме.
III. Физиотерапевтическое воздействие. При лечении больных П используют отвлекающие процедуры: банки, горчичники, горчичные обер тывания, которые при невысокой температуре тела принимают с первых дней болезни. После снижения температуры тела для ликвидации воспа лительных изменений назначают диатермию, индуктотермию, СВЧ, УВЧ и т.д. Рассасыванию очага пневмонии способствуют массаж грудной клет ки и ЛФК.
Аэрозольтерапия с использованием бронхолитических смесей отдельно или в комбинации с различными антибактериальными препаратами применяется в стадии разрешения.
7.Современные принципы лечения пневмоний у пожилых лиц и при иммунодефицитных состояниях.
I. Лечебный режим и рациональное питание.
II. Лекарственную терапию: 1) этиотропную, 2) патогенетическую, 3) симптоматическую.
Физиотерапевтическое воздействие.
Диспансерное наблюдение.
У больных с иммунодефицитными состояниями выбор антибактериальной терапии еще в большей степени зависит от природы возбудителя. Наиболее распространенной схемой является назначение аминогли-козидов и современных цефалоспоринов. У больных СПИДом при развитии пневмонии, вызванной Pneumocystis carinii, принятой схемой лечения является парентеральное введение пентамидина и бактрима, сеп-трима.
• Патогенетическая терапия. При тяжелых и затяжных пневмониях используют препараты иммуномодулирующего дейст вия (интерферон, левамизол, зимозан, диуцифон, Т-активин, тима- лин).
Больным вирусной пневмонией показаны введение противогриппозного у-глобулина, противовирусных препаратов (рибоварин, интерферон), ингаляции фитонцидов [сок чеснока и(или) лука, приготовленные ex tem-рогае, в изотоническом растворе хлорида натрия].
При стафилококковой пневмонии проводят пассивную иммунизацию гипериммунной антистафилококковой плазмой или стафилококковым антитоксином.
Для восстановления неспецифической резистентности организма назначают витамины А, С, Е, группы В, используют биогенные стимуляторы и адаптогенные средства (алоэ, настойки женьшеня и лимонника, жидкий экстракт элеутерококка).
Для восстановления бронхиальной проходимости применяют бронхо-литические средства (эуфиллин, теопэк и пр.) и средства, разжижающие бронхиальный секрет (внутрь мукалтин, ацетилцистеин, бромгексин, горячее щелочное питье). Если наблюдается надсадный кашель как проявление бронхоспазма, сопутствующего П, назначают адреномиметические средства: фенотерол (беротек), сальбутамол.
При затяжном течении пневмонии иногда решающую роль играет восстановление бронхиального дренажа с помощью бронхоскопической санации.
• Симптоматическая терапия. При непродуктивном сухом кашле назначают противокашлевые средства (кодеин, либек- син, тусупрекс, глауцина гидрохлорид и пр.); при затрудненном от- хождении мокроты — отхаркивающие (настой травы термопсиса, корень алтея и пр.). В случае плохой переносимости высокой тем-
пературы тела показаны жаропонижающие средства (анальгин, ацетилсалициловая кислота). Больным с сопутствующей патологией сердечно-сосудистой системы, особенно пожилым, а также при тяжелом течении пневмонии назначают инъекции камфоры, сульфо-камфокаина, кордиамина, при недостаточности кровообращения — сердечные гликозиды.
Наличие одышки и цианоза служит показанием к проведению кислородной терапии. При выраженной интоксикации и деструкции легочного инфильтрата проводят дезинтоксикационную терапию (внутривенное введение реополиглюкина, гемодеза и других растворов).
Больным с тяжелой формой пневмонии, с выраженной интоксикацией, инфекционно-токсическим шоком показано внутривенное введение кортикостероидов. Небольшие дозы кортикостероидов (10—15 мг в день) внутрь назначают при вялом рассасывании инфильтрата или сопутствующем аллергическом бронхоспазме.
III. Физиотерапевтическое воздействие. При лечении больных П используют отвлекающие процедуры: банки, горчичники, горчичные обер тывания, которые при невысокой температуре тела принимают с первых дней болезни. После снижения температуры тела для ликвидации воспа лительных изменений назначают диатермию, индуктотермию, СВЧ, УВЧ и т.д. Рассасыванию очага пневмонии способствуют массаж грудной клет ки и ЛФК.
Аэрозольтерапия с использованием бронхолитических смесей отдельно или в комбинации с различными антибактериальными препаратами применяется в стадии разрешения.
8.Бронхиальная астма: этиология, патогенез, классификация, диагностика.
Бронхиальная астма (БА) — «хроническое заболевание, основой которого является воспалительный процесс в дыхательных путях с участием разнообразных клеточных элементов, включая тучные клетки, эозинофилы и Т-лимфоциты. У предрасположенных лиц этот процесс приводит к развитию генерализованной бронхиальной обструкции разной степени выраженности, полностью или частично обратимой спонтанно или под влиянием лечения. Воспалительный процесс вызывает также содружественное усиление ответа дыхательных путей в виде бронхиальной обструкции на различные внешние и внутренние стимулы.
ЭТИОЛОГИЯ
В развитии болезни играют роль внутренние и внешние факторы. Внутренние факторы — это биологические дефекты иммунной, эндокринной систем, вегетативной нервной системы, чувствительности и реактивности бронхов, мукоцилиарного клиренса, эндотелия сосудов легких, системы быстрого реагирования (тучные клетки и др.), метаболизма арахидоновой кислоты и т.д.
Внешние факторы, способствующие клинической реализации биологических дефектов, включают: 1) аллергены (пыльцевые, пылевые, пищевые, лекарственные, производственные, аллергены клещей, насекомых, животных и пр.); 2) инфекцию (вирусы, грибы; некоторые виды бактерий); 3) механические и химические раздражители (металлическая, древесная, силикатная, хлопковая пыль; пары кислот, щелочей; дымы и пр.); 4) метеорологические и физико-химические факторы (изменение температуры и влажности воздуха, колебания барометрического давления, магнитного поля земли, физические усилия и пр.); 5) стрессовые нервно-психические воздействия и физическую нагрузку; 6) фармакологические воздействия (р-адреноблокаторы, нестероидные противовоспалительные препараты и т.д.)
Инфекционные агенты, помимо их аллергизирующего действия, могут играть также иную роль: а) снижать порог чувствительности организма к неинфекционным (атопическим) аллергенам, повышать проницаемость для них слизистой оболочки органов дыхания; б) формировать неиммунологическим путем изменение реактивности клеток-мишеней
Классификация бронхиальной астмы по тяжести течения
• Легкое эпизодическое (интермиттирующее). Кратковременные симптомы реже 1 раза в неделю.
Короткие обострения (от нескольких часов до нескольких дней).
Ночные симптомы < 2 раз в месяц.
Отсутствие симптомов и нормальная функция внешнего дыхания
между обострениями.
ПСВ и ОФВ1: 2: 80 % от должных.
Разброс показателей < 20 %.
• Легкое персистирующее. Симптомы от 1 раза в неделю до 1 раза в день.
Обострения могут снижать физическую активность и нарушать
сон.
Ночные симптомы > 2 раз в месяц.
ПСВ и OOBi: £ 80 % от должных.
Разброс показателей 20 — 30 %.
• Среднетяжелое. Ежедневные симптомы.
Обострения могут приводить к ограничению физической активности и сна.
Ночные симптомы > 1 раза в неделю. ПСВ и ОФВ1 : 60-80 % от должных. Суточный разброс показателей > 30 %.
• Тяжелое.
Постоянное наличие симптомов.
Частые ночные симптомы.
Ограничение физической активности из-за симптомов астмы.
ПСВ и ОФВ1 : <; 60 % от должных.
Суточный разброс показателей > 30 %.
Клиническая картина. Наиболее характерный признак БА — наличие приступов удушья. Однако клинический диагноз БА может быть поставлен с учетом оценки результатов всех трех этапов диагностического поиска, так как удушье встречается как симптом и при других заболеваниях. В связи с этим возникает на каждом из трех этапов необходимость ее дифференциации от заболеваний, составной частью которых является бронхоспастический синдром с развитием приступов удушья.
На I этапе диагностического поиска устанавливают: а) наличие приступов удушья, их особенности и связь с определенными факторами; б) аллергический анамнез (наследственную предрасположенность, непереносимость пищевых и лекарственных веществ); в) наличие предшествую-
щих заболеваний легких; г) влияние метеорологических факторов, физических усилий, дизовариальных расстройств и других причин на возникновение приступов удушья; д) эффективность проводимой ранее терапии; е) течение болезни, появление осложнений.
Больные жалуются на приступы удушья (затрудненное дыхание, преимущественно на выдохе), одышку и кашель. Характер кашля может быть разнообразным: чаще кашель сухой, надсадный, приступообразный или с выделением вязкой, трудноотделяемой мокроты. При развитии легочной недостаточности одышка беспокоит и в межприсгупный период. Повышение температуры тела может свидетельствовать об активности бронхоле-гочной инфекции. Затрудненное носовое дыхание, как правило, служит проявлением аллергической риносинусопатии (вазомоторный ринит, полипоз) — частого спутника или предшественника Б А (предастма). При расспросе больного необходимо уточнить частоту возникновения симптомов Б А в неделю, обратив особое внимание на ночные симптомы. Эти данные особенно важны для оценки тяжести течения болезни на момент обследования больного.
Данные анамнеза помогают установить связь развития приступов с воздействием определенных аллергенов и других факторов. Наиболее частой причиной обострения и развития БА является инфекция дыхательных путей; особенно велика ее роль в обострении болезни. Из анамнеза узнают о влиянии физического усилия (быстрая ходьба, смех и пр.), изменений метеорологических факторов (холод, повышенная влажность и др.), дизовариальных расстройств на возникновение приступов удушья. Знакомство с условиями труда помогает обнаружить профессиональную астму.
Изучение аллергологического анамнеза способствует диагностике ато-пического варианта БА. В подобных случаях можно получить сведения о поллинозе: обострения болезни имеют сезонный характер (чаще весной и летом), сопровождаются ринитом, конъюнктивитом. У таких больных бывают крапивница, отек Квинке; выявляется непереносимость пищевых продуктов, ряда лекарственных веществ; отмечается наследственная предрасположенность к аллергическим заболеваниям.
Ориентируясь на данные анамнеза, можно предположительно, а в ряде случаев и с уверенностью высказаться о так называемой аспириновой астме. Эти больные не страдают наследственной формой аллергических заболеваний. Их беспокоит нарушенное носовое дыхание (полипозные разрастания). Наиболее характерный симптом у таких больных — непереносимость нестероидных противовоспалительных препаратов (ацетилсалициловая кислота, индометацин и пр.), вызывающих астматические приступы. На этом этапе уже можно предположить простагландиновый механизм БА.
Указание в анамнезе на прием кортикостероидных препаратов свидетельствует о тяжести болезни, а эффективность приема — об иммунной форме Б А или кортикостероидозависимом ее варианте. Отсутствие эффекта от приема кортикоидных препаратов, особенно у больных с тяжелым течением Б А, делает предположение об аллергическом генезе Б А менее достоверным и практически исключает наличие у больного глюкокортикоид-ной недостаточности. Глюкокортикоиды неэффективны также при астме физического усилия.
Данные о развитии в прошлом астматического статуса свидетельствуют о тяжести течения заболевания и указывают на необходимость проведения терапии кортикостероидами. Наличие предшествующих заболеваний
органов дыхания (ХБ, ХП) предопределяет обычно тяжесть течения БА, отсутствие «светлых» промежутков.
Б А может протекать монотонно, с постоянно нарушенным дыханием и потребностью принимать ежедневно противоастматические средства.
Другой тип течения БА характеризуется периодическими обострениями с заметно усиливающимися признаками бронхиальной обструкции и ремиссиями, когда нарушения бронхиальной проходимости резко уменьшаются или исчезают. Такое течение БА наиболее характерно для атопи-ческого варианта заболевания.
Значение I этапа диагностического поиска особенно велико для диагностики Б А в начальном периоде заболевания, когда все проявления астмы имеют эпизодический характер, а физикальное исследование не дает достаточной информации для постановки диагноза.
На II этапе диагностического поиска в развернутой стадии болезни выявляют: а) внелегочные проявления аллергии; б) признаки бронхо-обструктивного синдрома; в) осложнения БА; г) другие заболевания, сопровождающиеся приступами бронхоспазма.
При обследовании кожных покровов иногда можно выявить изменения, характерные для аллергических проявлений: крапивницу, папулезные и эритематозные высыпания. Эти изменения могут свидетельствовать об иммунологическом варианте БА. При аллергических формах БА могут быть конъюнктивиты (особенно часто у больных поллинозами). Сочетание Б А с экземой, нейродермитом, псориазом предрасполагает к тяжелому течению астмы. Грибковое поражение кожи, ногтевых лож может сопровождаться гиперчувствительностью к грибковым аллергенам.
Часто можно выявить нарушение носового дыхания. Риниты и поли-поз рассматриваются как предастма. Гаймориты и другие синуситы служат очагом инфекции, который может провоцировать удушье.
При физикальном исследовании легких могут быть выявлены признаки эмфиземы. Появлению эмфиземы легких, а затем хронической дыхательной недостаточности и легочного сердца часто способствует хронический бронхит. Он может присоединиться к БА, если она затяжная, а также может служить фоном, на котором развивается инфекционнозависимая Б А.
Аускультация легких помогает обнаружить признаки бронхиальной обструкции, для которой характерны изменение дыхания (удлиненный выдох), сухие, преимущественно свистящие, хрипы. Иногда при обследовании вне приступа удушья сухих хрипов может быть немного или они не прослушиваются. Форсированный выдох позволяет выявить скрытый бронхоспазм (появление или нарастание сухих хрипов).
Обязательно проводят аускультацию легких в положении больного лежа: количество сухих хрипов увеличивается при «вагусном» их механизме.
Постоянно выслушиваемые на определенном участке влажные звонкие («трескучие») мелкопузырчатые хрипы могут свидетельствовать о развившемся пневмосклерозе.
В случае астматического статуса отмечается уменьшение количества сухих хрипов при аускультации вплоть до развития «немого» легкого, несмотря на резкое нарастание удушья и одышки.
Объективное обследование больного помогает выявить симптомы других заболеваний («бабочка» на коже лица, лимфоаденопатия в сочетании с увеличением печени и селезенки, стойкое повышение артериального дав-
ления, упорная лихорадка и пр.), при которых возникают приступы брон-хоспазма, проявляющиеся удушьем (системная красная волчанка, узелковый периартериит, реже другие диффузные заболевания соединительной ткани). В таких случаях предполагаемый диагноз Б А становится маловероятным.
На III этапе диагностического поиска выявляют:
а) нарушение бронхиальной проходимости;
б) измененную реактивность бронхов;
в) характерные изменения при проведении аллергологического обсле дования;
г) наличие очагов инфекции и признаков воспаления;
д) осложнения БА.
Спирография выявляет снижение объема форсированного выдоха за первую секунду (OOBi), уменьшение коэффициента Тиффно (соотношения ОФВ] к ЖЕЛ в процентах) и процентного отношения OOBi к ФЖЕЛ — характерные признаки нарушения бронхиальной проходимости по обструктивному типу. При обострении БА значительно возрастают (на 100 % и более превышают исходный уровень) остаточный объем легких (ООЛ) и функциональная остаточная емкость (ФОЕ). Анализ спирограм-мы позволяет обнаружить признаки трахеобронхиальной дискинезии по наличию зазубрины в верхней части нисходящего колена спирограммы (симптом Колбета— Висса). Эта дискинезия также способствует нарушению бронхиальной проходимости.
Пикфлоуметрия — определение пиковой объемной скорости выдоха — является непременным условием контроля за состоянием больного. Ее проводят утром (до приема лекарств) и вечером с помощью индивидуального карманного прибора — пикфлоуметра. Желательно, чтобы разброс утренних и вечерних значений ПСВ не превышал 20 %.
Пневмотахометрия выявляет преобладание мощности вдоха над мощностью выдоха, что служит ранним признаком бронхиальной обструкции.
Пневмотахография с построением кривой «поток —объем» позволяет диагностировать нарушение бронхиальной проходимости раздельно на уровне крупных, средних и мелких бронхов по данным экспираторного потока при легочном объеме, равном 75, 50, 35 % ФЖЕЛ. Для периферической обструкции характерно значительное снижение кривой «поток — объем» на участке 50 — 75 % ФЖЕЛ, т.е. снижение максимальной объемной скорости на уровне 50-75 % ФЖЕЛ (МОС50, МОС75).
По увеличению мощности выдоха при проведении пневмотахометрии и приросту показателей МОС75, MOCso, МОС25 по данным пневмотахометрии, проводимым после предварительного вдыхания больным бронхоли-тических (симпатомиметических и/или холинолитических) веществ определяют роль бронхоспазма в нарушении бронхиальной проходимости и степень его выраженности.
С помощью этих же методов подбирают наиболее активный для данного больного ингаляционный бронхолитический (симпатомиметический или холинолитический) препарат.
Появление повышенного бронхиального сопротивления, зарегистрированного с помощью спирографии, пневмотахометрии и пневмотахогра-фии в ответ на физическую нагрузку, вдыхание холодного воздуха, раз-
дражающих газов, пылей и ацетилхолина, свидетельствует об измененной реактивности бронхов.
Аллергологическое тестирование осуществляется только вне обострения заболевания и проводится с помощью набора разнообразных неинфекционных и инфекционных аллергенов.
Проводят кожные аллергические пробы (аппликационный, скарифи-кационный и внутрикожный способы нанесения аллергена). Выявленный аллерген можно наносить на конъюнктиву глаза, слизистую оболочку носа для оценки его провоцирующего действия. Наиболее достоверным методом специфической диагностики БА считают выявление специфической гиперреактивности бронхов с помощью ингаляционных провокационных тестов. Ингаляционно аллерген вводят с большой осторожностью, так как такой путь введения может спровоцировать тяжелый приступ БА или развитие астматического статуса. Установление аллергена и уточнение его провоцирующего действия — прямое доказательство аллергической природы БА.
Для специфической диагностики БА применяют также радиоиммуно-сорбентный тест, позволяющий количественно оценить IgE-антитела. Повышение уровня общего IgE подтверждает при соответствующих данных анамнеза атопический механизм развития БА (этот тест применяют при невозможности проведения аллергологического тестирования).
Лабораторные исследования помогают подтвердить предполагаемый диагноз, оценить эволюцию заболевания и эффективность проводимого лечения.
Появление эозинофилов в мокроте является одним из основных диагностических критериев Б А. Кроме того, диагностическое значение имеет обнаружение в мокроте спиралей Куршмана и кристаллов Шарко —Лейдена. Эозинофильный лейкоцитоз представляет собой неспецифический признак и может служить проявлением общей аллергической реакции организма.
Лабораторные исследования помогают решать вопрос о наличии активного воспалительного процесса и степени его выраженности (увеличение острофазовых показателей).
При обострении БА и астматическом статусе особое значение имеет исследование кислотно-основного состояния и газового состава крови (изменяющихся при увеличении дыхательной недостаточности).
Рентгенологическое исследование помогает выявить очаги инфекции (в придаточных пазухах, зубах, желчном пузыре) и установить наличие острого (пневмония) или обострения хронического воспалительного процесса в легких, эмфиземы легких и пневмосклероза.
По данным ЭКГ обнаруживают признаки развития компенсированного легочного сердца — гипертрофию правых отделов сердца (подробнее см. «Легочное сердце»). При подозрении на симптоматический характер бронхоспазма проводят дополнительное обследование по программе, определяемой предполагаемым заболеванием.
9.Бронхиальная астма: клиника, современные подходы к лечению.
Клиническая картина. Наиболее характерный признак БА — наличие приступов удушья. Однако клинический диагноз БА может быть поставлен с учетом оценки результатов всех трех этапов диагностического поиска, так как удушье встречается как симптом и при других заболеваниях. В связи с этим возникает на каждом из трех этапов необходимость ее дифференциации от заболеваний, составной частью которых является бронхоспастический синдром с развитием приступов удушья.
На I этапе диагностического поиска устанавливают: а) наличие приступов удушья, их особенности и связь с определенными факторами; б) аллергический анамнез (наследственную предрасположенность, непереносимость пищевых и лекарственных веществ); в) наличие предшествую-
щих заболеваний легких; г) влияние метеорологических факторов, физических усилий, дизовариальных расстройств и других причин на возникновение приступов удушья; д) эффективность проводимой ранее терапии; е) течение болезни, появление осложнений.
Больные жалуются на приступы удушья (затрудненное дыхание, преимущественно на выдохе), одышку и кашель. Характер кашля может быть разнообразным: чаще кашель сухой, надсадный, приступообразный или с выделением вязкой, трудноотделяемой мокроты. При развитии легочной недостаточности одышка беспокоит и в межприсгупный период. Повышение температуры тела может свидетельствовать об активности бронхоле-гочной инфекции. Затрудненное носовое дыхание, как правило, служит проявлением аллергической риносинусопатии (вазомоторный ринит, полипоз) — частого спутника или предшественника Б А (предастма). При расспросе больного необходимо уточнить частоту возникновения симптомов Б А в неделю, обратив особое внимание на ночные симптомы. Эти данные особенно важны для оценки тяжести течения болезни на момент обследования больного.
Данные анамнеза помогают установить связь развития приступов с воздействием определенных аллергенов и других факторов. Наиболее частой причиной обострения и развития БА является инфекция дыхательных путей; особенно велика ее роль в обострении болезни. Из анамнеза узнают о влиянии физического усилия (быстрая ходьба, смех и пр.), изменений метеорологических факторов (холод, повышенная влажность и др.), дизовариальных расстройств на возникновение приступов удушья. Знакомство с условиями труда помогает обнаружить профессиональную астму.
Изучение аллергологического анамнеза способствует диагностике ато-пического варианта БА. В подобных случаях можно получить сведения о поллинозе: обострения болезни имеют сезонный характер (чаще весной и летом), сопровождаются ринитом, конъюнктивитом. У таких больных бывают крапивница, отек Квинке; выявляется непереносимость пищевых продуктов, ряда лекарственных веществ; отмечается наследственная предрасположенность к аллергическим заболеваниям.
Ориентируясь на данные анамнеза, можно предположительно, а в ряде случаев и с уверенностью высказаться о так называемой аспириновой астме. Эти больные не страдают наследственной формой аллергических заболеваний. Их беспокоит нарушенное носовое дыхание (полипозные разрастания). Наиболее характерный симптом у таких больных — непереносимость нестероидных противовоспалительных препаратов (ацетилсалициловая кислота, индометацин и пр.), вызывающих астматические приступы. На этом этапе уже можно предположить простагландиновый механизм БА.
Указание в анамнезе на прием кортикостероидных препаратов свидетельствует о тяжести болезни, а эффективность приема — об иммунной форме Б А или кортикостероидозависимом ее варианте. Отсутствие эффекта от приема кортикоидных препаратов, особенно у больных с тяжелым течением Б А, делает предположение об аллергическом генезе Б А менее достоверным и практически исключает наличие у больного глюкокортикоид-ной недостаточности. Глюкокортикоиды неэффективны также при астме физического усилия.
Данные о развитии в прошлом астматического статуса свидетельствуют о тяжести течения заболевания и указывают на необходимость проведения терапии кортикостероидами. Наличие предшествующих заболеваний
органов дыхания (ХБ, ХП) предопределяет обычно тяжесть течения БА, отсутствие «светлых» промежутков.
Б А может протекать монотонно, с постоянно нарушенным дыханием и потребностью принимать ежедневно противоастматические средства.
Другой тип течения БА характеризуется периодическими обострениями с заметно усиливающимися признаками бронхиальной обструкции и ремиссиями, когда нарушения бронхиальной проходимости резко уменьшаются или исчезают. Такое течение БА наиболее характерно для атопи-ческого варианта заболевания.
Значение I этапа диагностического поиска особенно велико для диагностики Б А в начальном периоде заболевания, когда все проявления астмы имеют эпизодический характер, а физикальное исследование не дает достаточной информации для постановки диагноза.
На II этапе диагностического поиска в развернутой стадии болезни выявляют: а) внелегочные проявления аллергии; б) признаки бронхо-обструктивного синдрома; в) осложнения БА; г) другие заболевания, сопровождающиеся приступами бронхоспазма.
При обследовании кожных покровов иногда можно выявить изменения, характерные для аллергических проявлений: крапивницу, папулезные и эритематозные высыпания. Эти изменения могут свидетельствовать об иммунологическом варианте БА. При аллергических формах БА могут быть конъюнктивиты (особенно часто у больных поллинозами). Сочетание Б А с экземой, нейродермитом, псориазом предрасполагает к тяжелому течению астмы. Грибковое поражение кожи, ногтевых лож может сопровождаться гиперчувствительностью к грибковым аллергенам.
Часто можно выявить нарушение носового дыхания. Риниты и поли-поз рассматриваются как предастма. Гаймориты и другие синуситы служат очагом инфекции, который может провоцировать удушье.
При физикальном исследовании легких могут быть выявлены признаки эмфиземы. Появлению эмфиземы легких, а затем хронической дыхательной недостаточности и легочного сердца часто способствует хронический бронхит. Он может присоединиться к БА, если она затяжная, а также может служить фоном, на котором развивается инфекционнозависимая Б А.
Аускультация легких помогает обнаружить признаки бронхиальной обструкции, для которой характерны изменение дыхания (удлиненный выдох), сухие, преимущественно свистящие, хрипы. Иногда при обследовании вне приступа удушья сухих хрипов может быть немного или они не прослушиваются. Форсированный выдох позволяет выявить скрытый бронхоспазм (появление или нарастание сухих хрипов).
Обязательно проводят аускультацию легких в положении больного лежа: количество сухих хрипов увеличивается при «вагусном» их механизме.
Постоянно выслушиваемые на определенном участке влажные звонкие («трескучие») мелкопузырчатые хрипы могут свидетельствовать о развившемся пневмосклерозе.
В случае астматического статуса отмечается уменьшение количества сухих хрипов при аускультации вплоть до развития «немого» легкого, несмотря на резкое нарастание удушья и одышки.
Объективное обследование больного помогает выявить симптомы других заболеваний («бабочка» на коже лица, лимфоаденопатия в сочетании с увеличением печени и селезенки, стойкое повышение артериального дав-
ления, упорная лихорадка и пр.), при которых возникают приступы брон-хоспазма, проявляющиеся удушьем (системная красная волчанка, узелковый периартериит, реже другие диффузные заболевания соединительной ткани). В таких случаях предполагаемый диагноз Б А становится маловероятным.
На III этапе диагностического поиска выявляют:
а) нарушение бронхиальной проходимости;
б) измененную реактивность бронхов;
в) характерные изменения при проведении аллергологического обсле дования;
г) наличие очагов инфекции и признаков воспаления;
д) осложнения БА.
Спирография выявляет снижение объема форсированного выдоха за первую секунду (OOBi), уменьшение коэффициента Тиффно (соотношения ОФВ] к ЖЕЛ в процентах) и процентного отношения OOBi к ФЖЕЛ — характерные признаки нарушения бронхиальной проходимости по обструктивному типу. При обострении БА значительно возрастают (на 100 % и более превышают исходный уровень) остаточный объем легких (ООЛ) и функциональная остаточная емкость (ФОЕ). Анализ спирограм-мы позволяет обнаружить признаки трахеобронхиальной дискинезии по наличию зазубрины в верхней части нисходящего колена спирограммы (симптом Колбета— Висса). Эта дискинезия также способствует нарушению бронхиальной проходимости.
Пикфлоуметрия — определение пиковой объемной скорости выдоха — является непременным условием контроля за состоянием больного. Ее проводят утром (до приема лекарств) и вечером с помощью индивидуального карманного прибора — пикфлоуметра. Желательно, чтобы разброс утренних и вечерних значений ПСВ не превышал 20 %.
По увеличению мощности выдоха при проведении пневмотахометрии и приросту
Появление повышенного бронхиального сопротивления, зарегистрированного с помощью спирографии, пневмотахометрии и пневмотахогра-фии в ответ на физическую нагрузку, вдыхание холодного воздуха, раз-
дражающих газов, пылей и ацетилхолина, свидетельствует об измененной реактивности бронхов.
Аллергологическое тестирование осуществляется только вне обострения заболевания и проводится с помощью набора разнообразных неинфекционных и инфекционных аллергенов.
Проводят кожные аллергические пробы (аппликационный, скарифи-кационный и внутрикожный способы нанесения аллергена). Выявленный аллерген можно наносить на конъюнктиву глаза, слизистую оболочку носа для оценки его провоцирующего действия. Наиболее достоверным методом специфической диагностики БА считают выявление специфической гиперреактивности бронхов с помощью ингаляционных провокационных тестов. Ингаляционно аллерген вводят с большой осторожностью, так как такой путь введения может спровоцировать тяжелый приступ БА или развитие астматического статуса. Установление аллергена и уточнение его провоцирующего действия — прямое доказательство аллергической природы БА.
Для специфической диагностики БА применяют также радиоиммуно-сорбентный тест, позволяющий количественно оценить IgE-антитела. Повышение уровня общего IgE подтверждает при соответствующих данных анамнеза атопический механизм развития БА (этот тест применяют при невозможности проведения аллергологического тестирования).
Лабораторные исследования помогают подтвердить предполагаемый диагноз, оценить эволюцию заболевания и эффективность проводимого лечения.
Появление эозинофилов в мокроте является одним из основных диагностических критериев Б А. Кроме того, диагностическое значение имеет обнаружение в мокроте спиралей Куршмана и кристаллов Шарко —Лейдена. Эозинофильный лейкоцитоз представляет собой неспецифический признак и может служить проявлением общей аллергической реакции организма.
Рентгенологическое исследование помогает выявить очаги инфекции (в придаточных пазухах, зубах, желчном пузыре) и установить наличие острого (пневмония) или обострения хронического воспалительного процесса в легких, эмфиземы легких и пневмосклероза.
По данным ЭКГ обнаруживают признаки развития компенсированного легочного сердца — гипертрофию правых отделов сердца (подробнее см. «Легочное сердце»). При подозрении на симптоматический характер бронхоспазма проводят дополнительное обследование по программе, определяемой предполагаемым заболеванием.
ЛЕЧЕНИЕ
Ступенчатый подход к лечению бронхиальной астмы
I ступень (лечение легкой персистирующей БА): ингаляцион ные Рг-агонисты короткого действия применяют «по требованию» не более 3 раз в неделю; игаляционное введение хромогликата на трия (интала), или хромогликата натрия недокромила (тайледа), или рг-агониста короткого действия рекомендуется перед предпола гаемым контактом с аллергеном или перед физической нагрузкой.
II ступень (лечение Б А средней тяжести): ежедневная ингаля ционная противовоспалительная терапия — хромогликат натрия (интал) или кортикостероидные препараты в дозе 200 — 500 мкг. При необходимости увеличивают дозу кортикостероидов до 400 — 700 мкг (или при ночных приступах добавляют пролонгированные бронходилататоры). Ингаляционные р2-агонисты короткого дейст вия (используют не чаще 3 — 4 раз в день).
III ступень (лечение Б А средней тяжести): ингаляционные кортикостероидные препараты по 800 — 1000 мкг ежедневно; приме няют пролонгированные теофиллины или пероральные рг-агонис ты, или ингаляционные р2-агонисты пролонгированного действия (особенно при ночных приступах); можно назначать антихолинер- гические препараты; в случае необходимости применяют ингаляци онные рг-агонисты короткого действия, но не чаще 3 — 4 раз в день.
IV ступень (лечение БА тяжелого течения): ингаляционные кортикостероидные препараты по 800—1000 мкг в день; пролонги рованные теофиллины и/или пероральные или пролонгированные Рг-агонисты; при необходимости назначают р2-агонисты короткого действия (как правило, утром) ингаляционно, но не чаще 3 — 4 раз в день. Можно применять антихолинергические препараты. В тера пию включаются кортикостероидные препараты (перорально еже дневно или по альтернирующей схеме).
А Лекарственная противовоспалительная терапия.
Глюкокортикоидные препараты в настоящее время являются наиболее эффективными противовоспалительными средствами при лечении Б А. Их можно применять местно (ингаляционно) или системно (внутрь или парентерально). Способ введения во многом определяется особенностью течения заболевания.
Ингаляционное введение кортикостероидных препаратов оказывает местный эффект и дает минимум побочных эффектов. К числу короткодействующих препаратов относятся бекотид и бекломет (беклометазон дипропионат); их следует применять 4 раза в день. Такие препараты, как ингакорт (флунисолид), фликсотид (флютиказон пропионат) и пульми-корт турбухалер (будезонид), характеризуются большей продолжительностью действия, что позволяет использовать их для надежного контроля за течением БА 2 раза в сутки.
Бронхолитическая терапия: 1) бронхолитические препараты парентерально, в свечах или перорально. Препаратом выбора остается эуфиллин (10 мл 2,4 % раствора внутривенно струйно или капель-но) или теофиллин (по 0,3 г в свечах предпочтительнее на ночь), эуфиллин по 0,15 г в таблетках после еды 3 — 4 раза в день. Применяют препараты эуфиллина пролонгированного действия (теопек, теодур и др.). Эти препараты являются базисными и назначаются всем больным (при условии хорошей переносимости); 2) симпато-миметические и(или) холинолитические препараты назначаются в дозированном аэрозоле, как правило, при появлении предвестников приступа удушья. Постоянное применение этих препаратов в ингаляторах не рекомендуется во избежание побочных эффектов (тахикардия, повышение АД, нарушения ритма сердца); р2-адреностиму-ляторы эффективны при Б А, вызываемой физической нагрузкой, точно так же как и блокаторы медленных кальциевых каналов
Дополнительная патогенетическая терапия:
1) муколитические препараты в виде ингаляции (ацетилцистеин) или таблеток (мукалтин, лазолван), настои и отвары термопсиса назначают при вязкой, трудноотделяемой мокроте. Хорошее секретолитическое действие оказывают горячее щелочное питье и йодистые препараты (3 % раствор йодида калия по 1 столовой ложке 3 — 4 раза в день; следует помнить о возмож-
ной непереносимости препарата: слезотечение, ринорея, усиление бронхоспазма);
2) антибактериальную терапию проводят при обострении воспа лительного процесса в бронхолегочной системе у больных с инфекционнозависимой БА;
лечебная бронхоскопия под наркозом проводится в случае отсутствия эффекта от лекарственной терапии у больных при сопутствующем катарально-гнойном и гнойном эндобронхите (местно вводят антибактериальные средства, предпочтение оказывается 1 % раствору диоксидина). При необходимости эндобронхиально вводят кортикостероиды (гидрокортизон);
антагонисты кальция (нифедипин, изоптин, финоптин) инги- бируют трансмембранный поток кальция, что ведет к уменьше нию выхода медиаторных веществ из тучных клеток. Препара ты показаны больным при сочетании БА с ишемической болез нью сердца и при астме «физического усилия»;
антимедиаторы имеют небольшое значение в лечении Б А: а) антигистаминные препараты блокируют Нгрецепторы, уменьшая действие гистамина на гладкую мускулатуру брон хов; б) антисеротониновые препараты (циннаризин) применя ют лишь при лечении больных БА с четкими клиническими признаками гиперсеротонинемии (тахикардия, наклонность к поносам, гиперемия лица), в) ингибиторы калликреина — тра- силол, контрикал (по 10 000 ЕД) — вводят внутривенно ка- пельно при затянувшихся приступах Б А. Используют также гепарин, улучшающий микроциркуляцию. В настоящее время применяют две генерации антагонистов Hi-рецепторов. Пре параты первого поколения (димедрол, тавегил, супрастин, пипольфен, диазолин) оказывают ряд нежелательных воздей ствий (снотворное, вызывает сухость во рту, тахикардию, задержку мочи и т.д.), что резко ограничивает их применение. Препараты второго поколения — астемизол, кларитин и др. — лишены этих недостатков. Кроме того, помимо блокады Нгре- цепторов, в высоких дозах они уменьшают выделение медиато ров из тучных клеток и базофилов. Комбинацию сосудосужи вающего средства с лоратадином (псевдоэфедрин сульфат 120 мг и лоратадин 5 мг) — клариназе — с успехом применяют (по 1 таблетке 2 раза в день) для лечения аллергических ринитов;
новое направление в лечении Б А — применение антагонистов лейкотриеновых рецепторов — препарата аколата (зафиру- лакста) по 20 мг внутрь 2 раза в день;
физиотерапевтические методы воздействия (массаж грудной клетки, специальный комплекс дыхательной гимнастики). Иг- лорефлексотерапия оказывает благоприятный эффект в ком плексной терапии БА.
10.Астматический статус: причины, клиническая картина, объем неотложных мероприятий.
Астматический статус. Факторы, предрасполагающие к его развитию, почти всегда являются результатом неадекватной терапии. Чаще всего причинами его служат:
1) бесконтрольный прием симпатомиметических и кортикостероид-ных препаратов;
резкое прерывание длительно проводимой кортикостероидной те рапии;
обострение хронического или возникновение острого воспалитель ного процесса в бронхолегочном аппарате неэффективно леченного;
неудачно проведенная специфическая гипосенсибилизация;
злоупотребление снотворными и седативными средствами.
Критерии астматического (метаболического) статуса:
прогрессирующее нарушение дренажной функции бронхов;
развернутая клиническая картина удушья, которая может ослож няться легочной обструкцией, гипоксемической комой, острым легочным сердцем;
резистентность к симпатомиметическим и бронхолитическим пре паратам;
4)гиперкапния; 5) гипоксия тканей.
Классификация астматического статуса: I стадия — затянувшийся приступ удушья, сформировавшаяся резистентность к симпатомиметикам; II стадия — нарастание дыхательной недостаточности по обструктивному типу, III стадия — гипоксемическая, гиперкапническая кома.
Стадия I клинически характеризуется затянувшимся приступом удушья, вынужденным положением больного, учащенным дыханием, приступообразным кашлем со скудной, трудноотделяемой мокротой, тахикардией, часто повышением АД.
Из физикальных симптомов отмечают несоответствие между интенсивностью дыхательных шумов, выслушиваемых дистанционно, и данными непосредственной аускультации легких (скудность хрипов, участки ослабленного дыхания).
Стадия I характеризуется умеренной артериальной гипоксемией (РОг составляет 60 — 70 мм рт.ст.) и нормо- или гипокапнией (показатели РСо2 нормальные или уменьшены в результате гипервентиляции и составляют менее 35 мм рт.ст).
Для II стадии характерно очень тяжелое состояние больного: бледно-серые влажные кожные покровы, учащенное поверхностное дыхание, при аускультации — «немое легкое» (хрипы почти не слышны), частый пульс малого наполнения, аритмия, снижение АД. Периоды безразличия у больного сменяются возбуждением.
Стадия II характеризуется более выраженной гипоксемией (Ро2 50 — 60 мм рт.ст.) и нарастающей гиперкапнией вследствие снижения эффективной (альвеолярной) вентиляции (Рсо2 50 — 70 мм рт.ст. и даже несколько выше).
В III стадии сознание отсутствует, тахипноэ, часто разлитой «красный» цианоз, нередко коллапс. Летальность на высоте астматического статуса достигает 5 — 20 %. Наиболее частые причины смерти — асфиксия вследствие позднего проведения реанимационных мероприятий, невозможность восстановления эффективной вентиляции легких.
Стадия III характеризуется тяжелой артериальной гипоксемией (РОг 40 — 55 мм рт.ст.) и резко выраженной гиперкапнией (РСог на уровне 80 — 90 мм рт.ст. и выше) с некомпенсированным респираторным ацидозом.
При своевременно начатой интенсивной терапии прогноз астматического статуса может быть благоприятным.
Все вышеизложенное касалось так называемого метаболического (медленно развивающегося) астматического статуса. Кроме этого, существует немедленно развивающийся (анафилактический) астматический статус, обусловленный развитием гиперергической анафилактической реакции немедленного типа с мгновенным высвобождением медиаторов аллергии и воспаления, что приводит к тотальному бронхоспазму и асфиксии в момент контакта с аллергеном.
Лечение астматического статуса заключается в проведении интенсивной терапии, которую необходимо начинать в максимально ранние сроки. Она включает:
а) оксигенотерапию, терапию в виде непрерывной подачи кислородно- воздушной смеси с относительно небольшим содержанием Ог(35 —40 %);
б) инфузионную терапию, при которой внутривенно вводят декстра- ны, глюкозу, инсулин, 20 000 ЕД гепарина, натрия гидрокарбонат (под контролем показателей кислотно-основного состояния) в общем количест ве не менее 3 — 3,5 л в первые сутки с целью восполнения дефицита жид кости, устранения гемоконцентрации, разжижения бронхиального содер жимого;
в) обязательное внутривенное введение кортикостероидов: гидрокор тизона по 1 мг/ч на 1 кг массы тела, преднизолона по 60 — 90 мг каждые 2 — 4 ч при I стадии статуса; во II стадии суточную дозу преднизолона до водят до 1000 — 1500 мг. После выведения из астматического статуса дозу стероидов ежесуточно уменьшают на 25 % до минимальной. Лечение аст матического статуса исключает использование средств симпатомиметичес- кого действия, если он развился в результате их передозировки.
В качестве бронхорасширяющего средства используют эуфиллин; показанием для его отмены является развитие частой экстрасистолии.
Лечение анафилактического варианта астматического статуса требует проведения немедленной парентеральной лекарственной терапии: внутривенного введения 0,3 — 0,5 мл 0,1 % раствора адреналина на 20 мл изотонического раствора хлорида натрия и струйно внутривенно 120 мг преднизолона (200 — 400 мг гидрокортизона) с последующим переходом на внутривенное капельное введение этих же препаратов. Одновременно можно добавить 0,5—1 мл 0,1 % раствора атропина, вводя его струйно на 10 мл изотонического раствора.
При отсутствии эффекта от перечисленных мероприятий проводят фторотановый наркоз и переводят больного на ИВЛ.
После купирования приступа Б А проводят плановую терапию, основные направления которой сформулированы ниже.
Болезни эндокринной системы
Сахарный диабет: определение, классификация
Сахарный диабет (СД) - группа обменных заболеваний, характеризующихся гипергликемией вследствие нарушения секреции и/или эффективности действия инсулина. Хроническая гипергликемия, развивающаяся при СД, сопровождается развитием осложнений со стороны многих органов и систем, в первую очередь, со стороны сердца, кровеносных сосудов, глаз, почек и нервов. СД в общей сложности страдают 5-6 % населения. В экономически развитых странах мира каждые 10-15 лет число больных СД возрастает в 2 раза. Ожидаемая продолжительность жизни при СД снижается на 10-15 %.
Причины развития СД широко варьируют. В подавляющем большинстве случаев СД развивается либо вследствие абсолютного дефицита инсулина(сахарный диабет 1 типа - СД-1), либо вследствие снижения чувствительности периферических тканей к инсулину в сочетании с секреторной дисфункцией β-клеток поджелудочной железы (сахарный диабет 2 типа - СД-2). В ряде случаев отнесение пациента к СД-1 или СД-2 затруднено, тем не менее на практике более значима компенсация СД, а не точное установление его типа. Этиологическая классификация выделяет четыре основных клинических класса СД (табл. 7.1).
Наиболее часто встречающиеся СД-1 (п. 7.5), СД-2 (п. 7.6) и гестационный СД (п. 7.9) обсуждаются в отдельных главах. На другие специфические типы приходится всего около 1 % случаев СД. Этиология и патогенез этих типов СД представляется более изученной по сравнению с СД-1 и особенно СД-2. Ряд вариантов СД обусловлено моногенно наследуемыми генетическими дефектами функции β-клеток. Сюда относятся различные варианты аутосомно-доминантно наследуемого синдрома MODY (англ. maturity onset diabetes of the young - диабет взрослого типа у молодых), которые характеризуются нарушением, но не отсутствием секреции инсулина при нормальной чувствительности к нему периферических тканей.
Табл. 7.1. Классификация сахарного диабета
 Казуистически
редко встречаются генетические
дефекты действия инсулина, связанные
с мутацией рецептора инсулина
(лепречаунизм, синдром Рабсона-Мандехолла).
СД закономерно развивается призаболеваниях
экзокринной части поджелудочной
железы, приводящих
к деструкции β-клеток (панкреатит,
панкреатэктомия, кистозный фиброз,
гемохроматоз), а также при ряде эндокринных
заболеваний, при которых происходит
избыточная продукция контроинсулярных
гормонов (акромегалия, синдром
Кушинга). Лекарственные
препараты и химикаты (вакор,
пентамидин, никотиновая кислота,
диазоксид и др.) редко являются причиной
СД, но могут способствовать манифестации
и декомпенсации заболевания у лиц с
инсулинорезистентностью. Рядинфекционных
заболеваний (краснуха,
цитомегалия, коксаки- и аденовирусная
инфекция) могут сопровождаться деструкцией
β-клеток, при этом у большинства пациентов
определяются иммуногенетические маркеры
СД-1. К редким
формам иммуноопосредованного
диабета относят
СД, развивающийся у пациентов со
«stiff-rnan»-синдромом (аутоиммунное
неврологическое заболевание), а также
СД вследствие воздействия аутоантител
к рецепторам инсулина. Различные варианты
СД с повышенной частотой встречаются
при
Казуистически
редко встречаются генетические
дефекты действия инсулина, связанные
с мутацией рецептора инсулина
(лепречаунизм, синдром Рабсона-Мандехолла).
СД закономерно развивается призаболеваниях
экзокринной части поджелудочной
железы, приводящих
к деструкции β-клеток (панкреатит,
панкреатэктомия, кистозный фиброз,
гемохроматоз), а также при ряде эндокринных
заболеваний, при которых происходит
избыточная продукция контроинсулярных
гормонов (акромегалия, синдром
Кушинга). Лекарственные
препараты и химикаты (вакор,
пентамидин, никотиновая кислота,
диазоксид и др.) редко являются причиной
СД, но могут способствовать манифестации
и декомпенсации заболевания у лиц с
инсулинорезистентностью. Рядинфекционных
заболеваний (краснуха,
цитомегалия, коксаки- и аденовирусная
инфекция) могут сопровождаться деструкцией
β-клеток, при этом у большинства пациентов
определяются иммуногенетические маркеры
СД-1. К редким
формам иммуноопосредованного
диабета относят
СД, развивающийся у пациентов со
«stiff-rnan»-синдромом (аутоиммунное
неврологическое заболевание), а также
СД вследствие воздействия аутоантител
к рецепторам инсулина. Различные варианты
СД с повышенной частотой встречаются
при
многих генетических синдромах, в частности, при синдромах Дауна, Клайнфелтера, Тернера, Вольфрама, Прадера-Вилли и ряде других.
2.Диагностические критерии сахарного диабета. Пероральный глюкозотолерантный тест: показания, методика проведения, интерпретация.
Диагностические критерии СД и других нарушений углеводного обмена (ВОЗ, 1999)
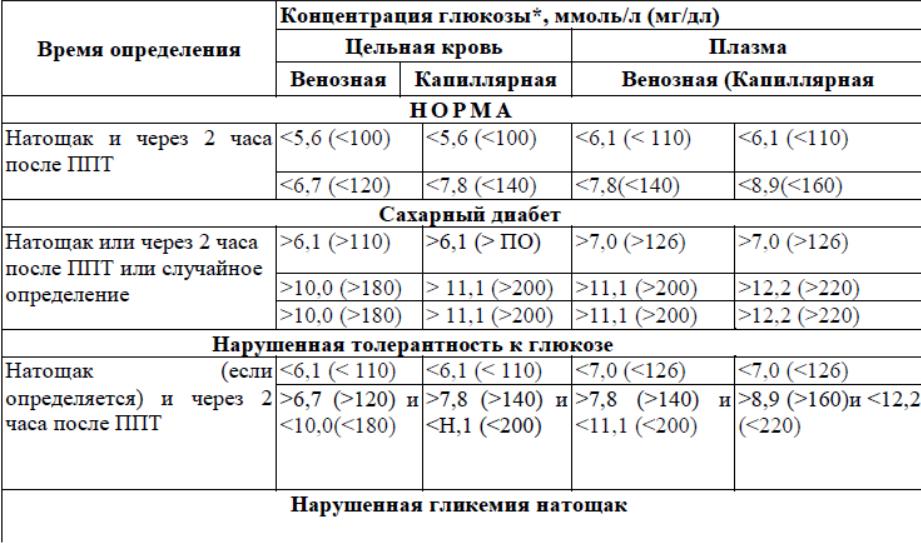
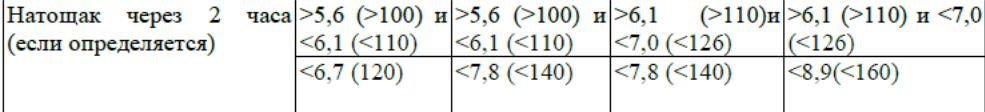
*Диагностика проводится на основании лабораторных определений уровня глюкозы.
**ПГТТ — перcоральный глюкозо-толерантный тест.
Натощак — означает уровень глюкозы утром после предварительного голодания в течение
не менее 8 часов и не более 14 часов.
Случайное — означает уровень глюкозы в любое время суток вне зависимости от времени
приема пищи
ППТ - пероральный глюкозотолерантиый тест. Проводится в случае сомнительных значений
гликемии для уточнения диагноза, при этом гликемия определяется до и через 2 часа после
пероральной нагрузки глюкозой. Нагрузка глюкозой соответствует:
для взрослых: 75 г безводной глюкозы, растворенной в 300 мл воды, выпить в течение
3 — 5 минут.
для детей: 1,75г безводной глюкозы на кг массы тела (но не более 75 г), выпить в
течение 3 — 5 минут
Для предотвращения ошибочных результатов определение концентрации глюкозы следует
проводить сразу после взятия крови, или центрифугировать кровь сразу после взятия, или
хранить ее при температуре 0 — 4°С, или брать кровь в пробирку с консервантом (фторид
натрия).
Диагноз СД следует подтверждать повторным определением гликемии в другие дни, за
исключением случаев несомненной гипергликемии с острой метаболической декомпенсацией
или с очевидными симптомами
ППТ не проводится:
— на фоне острого заболевания
—на фоне кратковременного приема препаратов, повышающих уровень гликемии
(глюкокортикоиды, тиреоидные гормоны, тиазиды, бета-адреноблокаторы и др.)
3.Сахарный диабет 1 типа: определение, этиология, патогенез, диагностика
Сахарный диабет 1 типа — эндокринное заболевание, характеризующееся абсолютной недостаточностью инсулина, вызванной разрушением бета-клеток поджелудочной железы. Диабет 1 типа может развиться в любом возрасте, однако наиболее часто он поражает людей молодого возраста (детей, подростков, взрослых людей моложе 40 лет. В клинической картине преобладают классические симптомы: жажда, полиурия, потеря веса, кетоацидотические состояния.
Этиология и патогенез: В основе патогенетического механизма развития диабета 1 типа лежит недостаточность выработки инсулина эндокринными клетками поджелудочной железы (β-клетки поджелудочной железы), вызванное их разрушением под влиянием тех или иных патогенных факторов (вирусная инфекция, стресс, аутоиммунные заболевания и др.). Диабет 1 типа составляет 10-15 % от всех случаев диабета, и, в большинстве случаев, развивается в детском или подростковом возрасте. Для этого типа диабета характерно появление основных симптомов, которые быстро прогрессируют с течением времени.
Основным методом лечения являются инъекции инсулина, нормализующие обмен веществ организма больного. В отсутствии лечения диабет 1 типа быстро прогрессирует и приводит к возникновению тяжёлых осложнений, таких как кетоацидоз и диабетическая кома, заканчивающиеся смертью больного.
Патогенез и патогистология Дефицит инсулина в организме развивается вследствие недостаточной его секреции β-клетками островков Лангерганса поджелудочной железы. Вследствие инсулиновой недостаточности, инсулинзависимые ткани (печёночная,жировая и мышечная) теряют способность утилизировать глюкозу крови и, как следствие, повышается уровень глюкозы в крови (гипергликемия) — кардинальный диагностический признак сахарного диабета. Вследствие инсулиновой недостаточности в жировой ткани стимулируется распад жиров, что приводит к повышению их уровня в крови, а в мышечной ткани — стимулируется распад белков, что приводит к повышенному поступлению аминокислот в кровь. Субстраты катаболизма жиров и белков трансформируются печенью в кетоновые тела, которые используются инсулиннезависимыми тканями (главным образом мозгом) для поддержания энергетического баланса на фоне инсулиновой недостаточности. Глюкозурия является адаптационным механизмом выведения повышенного содержания глюкозы из крови, когда уровень глюкозы превышает пороговое для почек значение (около 10 ммоль/л). Глюкоза является осмоактивным веществом и повышение ее концентрации в моче стимулирует повышенное выведение и воды (полиурия), что в конечном счете может привести к дегидратации организма, если потеря воды не компенсируется адекватным повышенным потреблением жидкости (полидипсия). Вместе с повышенной потерей воды с мочой теряются и минеральные соли — развивается дефицит катионов натрия, калия, кальция и магния, анионов хлора, фосфата и гидрокарбоната.
Выделяют 6 стадий развития СД1.
1)Генетическая предрасположенность к СД1, ассоциированная с системой HLA. 2)Гипотетический пусковой момент. Повреждение β — клеток различными диабетогенными факторами и триггирование иммунных процессов. У больных уже определяются выше перечисленные антитела в небольшом титре, но секреция инсулина еще не страдает. 3)Активный аутоиммунный инсулинит. Титр антител высок, уменьшается количество β-клеток, снижается секреция инсулина.
4)Снижение стимулированной глюкозой секреции И. В стрессовых ситуациях у больного можно выявить преходящее НТГ (нарушение толерантности к глюкозе) и НГПН (нарушение содержания глюкозы плазмы натощак).
5)Клиническая манифестация СД, в том числе с возможным эпизодом «медового месяца». Секреция инсулина резко снижена, так как погибло более 90 % β-клеток.
6)Полная деструкция β-клеток, полное прекращение секреции инсулина.
Диагностика В клинической практике достаточными критериями диагностики сахарного диабета 1 типа являются наличие типичных симптомов гипергликемии (полиурия и полидипсия) и лабораторно подтвержденная гипергликемия — гликемия в капиллярной крови натощак более 7,0 ммоль/л и/или в любое время суток более 11,1 ммоль/л; При установлении диагноза врач действует по следующему алгоритму. Исключают заболевания, которые проявляются сходными симптомами (жажда, полиурия, потеря веса): несахарный диабет, психогенная полидипсия, гиперпаратиреоз, хроническая почечная недостаточность и др. Этот этап заканчивается лабораторной констатацией синдрома гипергликемии. Уточняется нозологическая форма СД. В первую очередь исключают заболевания, которые входят в группу «Другие специфические типы диабета». И только затем решается вопрос СД1 или СД 2 страдает больной. Проводиться определение уровня С-пептида натощак и после нагрузки. Так же оценивается уровень концентрации в крови GAD-антител.
Сахарный диабет 2 типа - хроническое заболевание, проявляющееся нарушением углеводного обмена с развитием гипергликемии вследсвие инсулинорезистентности и секреторной дисфункции бета-клеток, а также липидного обмена с развитием атеросклероза. Поскольку основной причиной смерти и инвалидизации пациентов являются осложнения системного атеросклероза, сахарный диабет 2 типа иногда называют сердечно-сосудистым заболеванием.
Этиология Сахарный диабет 2 типа является многофакторным заболеванием с наследственной предрасположенностью. Большинство пациентов с сахарным диабетом 2 типа указывают на наличие сахарного диабета 2 типа у ближайших родственников; при наличии сахарного диабета 2 типа у одного из родителей вероятность его развития у потомка на протяжении жизни составляет 40 %. Какого-то одного гена, полиморфизм которого определяет предрасположенность к сахарному диабету 2 типа, не обнаружено. Большое значение в реализации наследственной предрасположенности к сахарному диабету 2 типа играют факторы окружающей среды, в первую очередь, особенности образа жизни. Факторами риска развития сахарного диабета 2 типа являются:
Патогенез Патогенетически сахарный диабет 2 типа представляет собой гетерогенную группу нарушений обмена веществ, именно это и определяет его значительную клиническую неоднородность. В основе его патогенеза лежит инсулинорезистентность (снижение опосредованной инсулином утилизации глюкозы тканями), которая реализуется на фоне секреторной дисфункции бета-клеток. Таким образом, происходит нарушение баланса чувствительности к инсулину и инсулиновой секреции. Секреторная дисфункция бета-клеток заключается в замедлении «раннего» секреторного выброса инсулина в ответ на увеличение уровня глюкозы в крови. При этом 1-я (быстрая) фаза секреции, которая заключается в опорожнении везикул с накопленным инсулином, фактически отсутствует; 2-я (медленная) Фаза секреции осуществляется в ответ на стабилизирующуюся гипергликемию постоянно, в тоническом режиме, и, несмотря на избыточную секрецию инсулина, уровень гликемии на фоне инсулинорезистентности не нормализуется. Следствием гиперинсулинемии является снижение чувствительности и числа инсулиновых рецепторов, а также подавление пострецепторных механизмов, опосредующих эффекты инсулина (инсулинорезистентность). Содержание основного транспортера глюкозы в мышечных и жировых клетках (GLUT-4) снижено на 40 % улиц с висцеральных ожирением и на 80 % - улиц с сахарным диабетом 2 типа. Вследствие инсулинорезистентности гепатоцитов и портальной гиперинсулинемией происходит гиперпродукция глюкозы печенью, и развивается гипергликемия натощак, которая выявляется у большинства пациентов с сахарным диабетом 2 типа, в том числе и на ранних этапах заболевания. Сама по себе гипергликемия неблагоприятно влияет на характер и уровень секреторной активности бета-клеток (глюкозотоксичность). Длительно, на протяжении многих лет и десятилетий существующая гипергликемия в конечном счете приводит к истощению продукции инсулина бета-клетками и у пациента могут появиться некоторые симптомы дефицита инсулина - похудение, кетоз при сопутствующих инфекционных заболеваниях. Тем не менее, остаточная продукция инсулина, которой оказывается достаточно для предотвращения кетоацидоза, при сахарном диабете 2 типа практически всегда сохраняется. Распространенность сахарного диабета 2 типа варьирует в разных странах и этнических группах. С возрастом заболеваемость сахарным диабетом 2 типа увеличивается: среди взрослых распространенность сахарным диабетом 2 типа составляет 10 %, среди лиц старше 65 лет достигает 20 %. ВОЗ предсказывает увеличение числа больных диабетом в мире на 122 % в течение ближайших 20 лет (с 135 до 300 миллионов). Это связано как с прогрессирующим старением населения. В последние годы отмечается значительное «омоложение» сахарного диабета 2 типа и рост его заболеваемости среди детей. Диагностика Диагноз сахарного диабета 2 типа в подавляющем большинстве случаев базируется на выявлении гипергликемии улиц с типичными клиническими признаками сахарного диабета 2 типа (ожирение, возраст старше 40-45 лет, положительный семейный анамнез сахарного диабета 2 типа, другие компоненты метаболического синдрома), при отсутствии клинических и лабораторных признаков абсолютного дефицита инсулина (выраженное похудение, кетоз). Сочетание высокой распространенности сахарного диабета 2 типа, свойственного ему длительного бессимптомного течения и возможности предотвращения его тяжелых осложнений при условии ранней диагностики предопределяют необходимость скрининга, т.е. проведения обследования с целью исключения сахарного диабета 2 типа среди лиц без каких-либо симптомов заболевания. Основным тестом, как указывалось, является определение уровня гликемии натощак. Оно показано в следующих ситуациях:
|
5.Гестационный сахарный диабет: определение, особенности диагностики и лечения.
Гестационный сахарный диабет (ГСД) - это нарушение толерантности к глюкозе, впервые выявленное во время беременности (табл. 7.23). Это определение не исключает того, что патология углеводного обмена могла предшествовать наступлению беременности. ГСД следует отличать от ситуаций, когда у женщины с диагностированным ранее диабетом (в силу возраста, чаще СД-1) наступает беременность.
Этиология и патогенез При ГСД сходны с таковыми при СД-2. Высокий уровень овариальных и плацентарных стероидов, а также увеличение образования кортизола корой надпочечников приводят при беременности к развитию физиологической инсулинорезистентности. Развитие ГСД связывают с тем, что инсулинорезистентность, закономерно развивающаяся при беременности, и, следовательно, повышенная потребность в инсулине у предрасположенных лиц превышает функциональную способность β-клеток ПЖЖ. После родов с возвращением гормональных и метаболических взаимоотношений к исходному уровню он, как правило, проходит. Табл. 7.23. Гестационный сахарный диабет
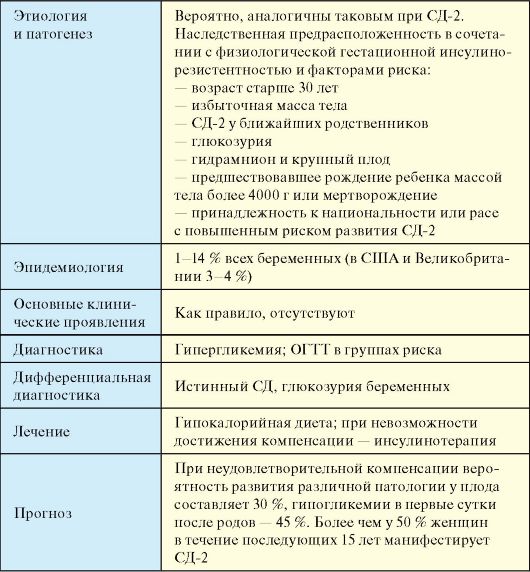 ГСД
обычно развивается в середине 2 триместр,
между 4 и 8 месяцами беременности.
Подавляющее большинство пациенток
имеет избыток массы тела и отягощенный
по СД-2 анамнез. Факторы риска развития
ГСД, а также группы женщин с низким
риском развития ГСД приведены в табл.
7.24.
ГСД
обычно развивается в середине 2 триместр,
между 4 и 8 месяцами беременности.
Подавляющее большинство пациенток
имеет избыток массы тела и отягощенный
по СД-2 анамнез. Факторы риска развития
ГСД, а также группы женщин с низким
риском развития ГСД приведены в табл.
7.24.
|
Табл. 7.24. Факторы риска развития гестационного сахарного диабета
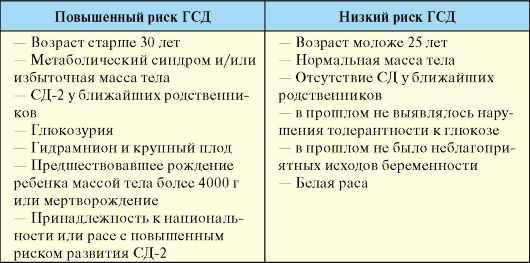 Гипергликемия
матери приводит к гипергликемии в
системе кровообращения ребенка. Глюкоза
легко проникает через плаценту и
непрерывно переходит к плоду из крови
матери. Также происходят активный
транспорт аминокислот и перенос кетоновых
тел плоду. В отличие от этого инсулин,
глюкагон и свободные жирные кислоты
матери в кровь плода не попадают. В
первые 9-12 недель беременности ПЖЖ плода
еще не вырабатывает собственный инсулин.
Это время соответствует той фазе
органогенеза плода, когда при постоянной
гипергликемии у матери могут формироваться
различные пороки развития (сердца,
позвоночника, спинного мозга, ЖКТ). С
12-й недели беременности ПЖЖ плода
начинает синтезировать инсулин, и в
ответ на гипергликемию развиваются
реактивная гипертрофия и гиперплазия
β-клеток фетальной ПЖЖ. Вследствие
гиперинсулинемии развиваются макросомия
плода, а также угнетение синтеза лецитина,
что объясняет высокую частоту развития
респираторного дистресссиндрома у
новорожденных. В результате гиперплазии
β-клеток и гиперинсулинемии появляется
склонность к тяжелым и длительным
гипогликемиям.
Гипергликемия
матери приводит к гипергликемии в
системе кровообращения ребенка. Глюкоза
легко проникает через плаценту и
непрерывно переходит к плоду из крови
матери. Также происходят активный
транспорт аминокислот и перенос кетоновых
тел плоду. В отличие от этого инсулин,
глюкагон и свободные жирные кислоты
матери в кровь плода не попадают. В
первые 9-12 недель беременности ПЖЖ плода
еще не вырабатывает собственный инсулин.
Это время соответствует той фазе
органогенеза плода, когда при постоянной
гипергликемии у матери могут формироваться
различные пороки развития (сердца,
позвоночника, спинного мозга, ЖКТ). С
12-й недели беременности ПЖЖ плода
начинает синтезировать инсулин, и в
ответ на гипергликемию развиваются
реактивная гипертрофия и гиперплазия
β-клеток фетальной ПЖЖ. Вследствие
гиперинсулинемии развиваются макросомия
плода, а также угнетение синтеза лецитина,
что объясняет высокую частоту развития
респираторного дистресссиндрома у
новорожденных. В результате гиперплазии
β-клеток и гиперинсулинемии появляется
склонность к тяжелым и длительным
гипогликемиям.
Эпидемиология СД страдают 0,3 % всех женщин репродуктивного возраста, 0,2-0,3 % беременных уже исходно больны СД, а в 1-14 % беременностей развивается ГСД или манифестирует истинный СД. Распространенность ГСД варьирует в разных популяциях, так, в США он выявляется примерно у 4 % беременных (135 тыс. случаев в год).
Клинические проявления При ГСД отсутствуют. Могут быть неспецифические симптомы декомпенсации СД.
Диагностика Определение уровня глюкозы крови натощак показано всем беременным женщинам в рамках биохимического анализа крови. Женщинам, которые относятся к группе риска (табл. 7.24), показано проведение орального глюкозотолерантного теста (ОГТТ). Описано много вариантов его проведения у беременных. Наиболее простой из них подразумевает следующие правила:
|
• 3 дня до обследования женщина находится на обычном питании и придерживается обычной для себя физической активности;
• тест проводится утром натощак, после ночного голодания не менее 8 часов;
• после взятия пробы крови натощак женщина в течение 5 минут выпивает раствор, состоящий из 75 грамм сухой глюкозы, растворенной в 250-300 мл воды; повторное определение уровня гликемии проводится через 2 часа.
• диагноз ГСД устанавливается по следующим критериям:
- глюкоза цельной крови (венозной, капиллярной) натощак > 6,1 ммоль/л или
- глюкоза плазмы венозной крови ≥ 7 ммоль/л или
- глюкоза цельной капиллярной крови или плазмы венозной крови через 2 часа после нагрузки 75 г глюкозы ≥ 7,8 ммоль/л.
• если у женщины, которая относится к группе риска, результаты исследования соответствуют норме, тест проводится повторно на 24-28 неделе беременности.
Дифференциальная диагностика ГСД и истинный СД; глюкозурия беременных.
Лечение Риск для матери и плода, а также подходы к лечению СД и особенности контроля за ним при ГСД и при истинном СД одинаковы. Поздние осложнения СД во время беременности могут значительно прогрессировать, однако при качественной компенсации СД показаний для прерывания беременности нет. Женщина, страдающая СД (как правило, речь идет о СД-1), должна планировать беременность в молодом возрасте, когда риск развития осложнений наиболее низок. Если планируется беременность, то рекомендуется отменять контрацепцию спустя несколько месяцев после достижения оптимальной компенсации. Противопоказаниями к планированию беременности являются тяжелая нефропатия с прогрессирующей почечной недостаточностью, тяжелая ИБС, тяжелая пролиферативная ретинопатия, не поддающаяся коррекции, кетоацидоз на ранних сроках беременности (кетоновые тела являются тератогенными факторами).
|
Целью лечения ГСД и истинного СД во время беременности является достижение следующих лабораторных показателей:
• гликемия натощак < 5-5,8 ммоль/л;
• гликемия через 1 ч после еды < 7,8 ммоль/л;
• гликемия через 2 ч после еды < 6,7 ммоль/л;
• среднее значение дневного гликемического профиля < 5,5 ммоль/л;
• уровень HbA1c при ежемесячном контроле, как у здоровых (4-6 %).
При СД-1, как и вне беременности, женщина должна получать интенсивную инсулинотерапию, однако уровень гликемии во время беременности рекомендуется оценивать 7-8 раз в сутки. При невозможности достижения нормогликемической компенсации на фоне обычных инъекций, необходимо рассмотреть вопрос о переводе пациентки на инсулинотерапию при помощи дозатора инсулина.
На первым этапе лечения ГСД назначается диетотерапия, заключающаяся в ограничении суточного калоража примерно до 25 кКал/кг фактического веса, в первую очередь за счет легко усваиваемых углеводов и жиров животного происхождения, а также расширение физических нагрузок. Если на фоне диетотерапии не удается достичь поставленных целей лечения, пациентке необходимо назначить интенсивную инсулинотерапию. Любые таблетированные сахароснижающие препараты (ТСП) при беременности противопоказаны. На инсулинотерапию оказывается необходимым переводить около 15 % женщин.
Прогноз При неудовлетворительной компенсации ГСД и СД во время беременности вероятность развития различной патологии у плода составляет 30 % (риск в 12 раз выше, чем в общей популяции). Более чем у 50 % женщин, у которых во время беременности выявлялся ГСД, в течение последующих 15 лет манифестирует СД-2.
Принципы диагностики сахарного диабета. Понятие о компенсации, субкомпенсации и декомпенсации сахарного диабета.
Лабораторная диагностика СД базируется на определении уровня глюкозы крови,при этом критерии диагностики едины для всех типов и вариантов СД.
Диагноз СД может быть установлен на основании двукрастного обнаружения одного из трех критериев:
1.при явных симптомах СД(полиурия,полидипсия )и уровене глюкозы в цельной капилярной крови более11,1 ммоль/л вне зависимости от времени суток и предшествовавшего приема пищи.
2.при уровне глюкозы в цельной капиллярной крови натощак более 6,1 ммоль/л.
3.при уровне глюкозы в цельной капиллярной крови через 2 часа после приема 75 грамм глюкозы(оральный глюкозотолкрантный тест)более11.1ммоль/л.
При возникновении подозрения на диабет назначаются дополнительные методы обследования.
Определение концентрации глюкозы в крови. Это один из наиболее специфических тестов на СД. Нормальная концентрация глюкозы в крови (гликеемия) натощак колеблется в пределах 3,3-5,5 ммоль/л. Повышение концентрации глюкозы выше этого уровня свидетельствует о нарушении метаболизма глюкозы. Для того чтобы установить диагноз диабета нужно установить повышение концентрации глюкозы в крови по меньшей мере в двух последовательных измерениях проводимых в разные дни. Забор крови на анализ проводят в основном в утреннее время. Перед забором крови нужно удостовериться в том, что пациент ничего не ел накануне обследования. Также важно обеспечить пациенту психологический комфорт во время проведения обследования для того, чтобы избежать рефлекторного повышения уровня глюкозы в крови, как ответ на стрессовую ситуацию.
Более чувствительным и специфичным методом диагностики является глюкозотолерантный тест, который позволяет выявить латентные (скрытые) нарушения метаболизма глюкозы (нарушения толерантности тканей к глюкозе). Тест проводится в утренние часы после 10-14 часов ночного голодания. Накануне обследования больному рекомендуется отказаться от повышенных физических нагрузок, употребления алкоголя и курения, а также препаратов способствующих повышению концентрации глюкозы в крови (адреналин, кофеин, глюкокортикоиды, контрацептивны и пр.). Пациенту дают выпить раствор содержащий 75 граммов чистой глюкозы. Определение концентрации глюкозы в крови проводят через 1 час и спустя 2 после употребления глюкозы. Нормальным результатом считают концентрацию глюкозы менее 7,8 ммоль/л спустя два часа после употребления глюкозы. Если концентрация глюкозы колеблется от 7,8 до 11 ммоль/л, то состояние исследуемого расценивается как нарушение толерантности к глюкозе (предиабет). Диагноз диабет устанавливается если концентрация глюкозы превышает 11 ммоль/л через два часа с начала проведения теста. Как простое определение концентрации глюкозы, так и проведение глюкозотолерантного теста дают возможность оценить состояние гликемии только на момент исследования. Для оценки уровня гликемии на более длительном промежутке времени (примерно три месяца) проводят анализ по определению уровня гликозилированного гемоглобина (HbA1c). Образование этого соединения находится в прямой зависимости от концентрации глюкозы в крови. Нормальная содержание этого соединения не превышает 5,9% (от общего содержания гемоглобина). Повышение процентного содержания HbA1c выше нормальных значений свидетельствует о длительном повышении концентрации глюкозы в крови на протяжении трех последних месяцев. Данный тест проводят в основном для контроля качества лечения больных диабетом.
Определение глюкозы в моче. В норме глюкоза в моче отсутствует. При сахарном диабете повышение гликемии достигает значений позволяющих глюкозе проникать через почечный барьер. Определение глюкозы в крови является дополнительным методом диагностики диабета.
Определение ацетона в моче (ацетонурия) – нередко диабет осложняется нарушением обмена веществ с развитие кетоацидоза (накопление в крови органических кислот промежуточных продуктов метаболизма жиров). Определение в моче кетоновых тел служит признаком тяжести состояния пациента с кетоацидозом.
В некоторых случаях для уточнения причины диабета проводят определение фракции инсулина и продуктов его метаболизма в крови. Для диабета 1-го типа характерно снижение или полное отсутствие фракции свободного инсулина или пептида С в крови.
Для диагностики осложнений диабета и составления прогноза заболевания проводят дополнительные обследования: исследование глазного дна (ретинопатия), электрокардиограмма (ишемическая болезнь сердца), экскреторная урография (нефропатия, почечная недостаточность).
Компенсированный сахарный диабет — это состояние патологического процесса, при котором при помощи различных лечебных действий показатели сахара крови максимально приближены к нормальным, следовательно, вероятность осложнений минимальна.
Декомпенсированный сахарный диабет — это состояние патологического процесса, при котором вероятность развития различных осложнений наиболее выражена.
Субкомпенсированный сахарный диабет — это промежуточное состояние между компенсированным и декомпенсированным состоянием.
