
19. Сформулируйте принцип Паули.
В атоме не может быть больше 1 электрона с заданным набором квантовых чисел(принцип исключительности).Принцип П. работает для всех микрочастиц,волновая ф-ия которых антисимметрична, а в свою очередь волновая ф-ия будет антисимметрична с полуцелым спином.s=1/2(электрон,протон,нейтрон,мюон)фермионы.
Статические св-ва этих частиц описываются распределением Ферми-Дирака (N(E)=N0 (1/(exp((E-μ)/kT)+1))). Частицы с целым спином:фотоны, базоны, альфа-частицы и др базоны(s=1,2…). Описываются симметричной волновой ф-ей, а их статические св-ва подчиняются распределению Бозе- Эйнштейна (N(E)=N0 (1/(exp(E-μ)/kT))). Для этих частиц не выполняются принцип П.
20.
Электронная оболочка атома — область пространства вероятного местонахождения электронов, характеризующихся одинаковым значением главного квантового числа n и, как следствие, располагающихся на близких энергетических уровнях. Число электронов в каждой электронной оболочке не превышает определенного максимального значения.
Порядок заполнения электронных оболочек (орбиталей с одинаковым значением главного квантового числа n) определяется правилом Клечковского, порядок заполнения электронами орбиталей в пределах одного подуровня (орбиталей с одинаковыми значениями главного квантового числа n и орбитального квантового числа l) определяется Правилом Хунда.
В чём заключаются правила Хунда?
Распределение электронов внутри подоболочки происходит в соот-ии с правилами Хунда. Это правило не теор. Выведено.Часть 1:Наименьшей энергией будут обладать те электроны у которых квантовое число спинового момента импульса максимально(общий спин максим.)
2 часть:Наименьшей энергией при заданных значениях проекций спинового момента обладает те состояния в которых квантовое число полного орбитального момента будет максим.3 часть:квантовое число полного механич. Момента в состоянии с наименьшей энергией находится как разница орбитального и спинового квантовых чисел, если пооболочка заполнена меньше,чем на половину.
21 Тормозное излучение: при торможении электрона на аноде. (M*V^2)/2=hv+(m*v(штрих)^2)/2.
Частота диапазон: от 0 до максимума=(m*v^2)/2h. Имеет граничную максимальную частоту. Спектр этого излучения сплошной.
Характеристическое: характер излучения определяется материалом анода. Чем больше энергетических уровней, тем больше частота фотона. Расстояние между ионами = период кристаллической решетки.
Особенности; Лучи, открытые Рентгеном, действовали на фотопластинку, вызывали ионизацию воздуха, но заметным образом не отражались от каких-либо веществ и не испытывали преломления. Электромагнитное поле не оказывало никакого влияния на направление их распространения.
Сразу же возникло предположение, что рентгеновские лучи — это электромагнитные волны, которые излучаются при резком торможении электронов. В отличие от световых лучей видимого участка спектра и ультрафиолетовых лучей рентгеновские лучи имеют гораздо меньшую длину волны. Их длина волны тем меньше, чем больше энергия электронов, сталкивающихся с препятствием. Большая проникающая способность рентгеновских лучей и прочие их особенности связывались именно с малой длиной волны
22 Ядро простейшего атома - атома водорода - состоит из одной элементарной частицы, называемой протоном. Ядра всех остальных атомов состоят из двух видов элементарных частиц - протонов и нейтронов. Эти частицы носят название нуклонов. Характеристики атомного ядра. Одной из важнейших характеристик атомного ядра является зарядовое число Z. Оно равно количеству протонов, входящих в состав ядра, и определяет его заряд, который равен +Ze. Число Z определяет порядковый номер химического элемента в периодической таблице Менделеева. Поэтому его также называют атомным номером ядра.
Число нуклонов (т. е. суммарное число протонов и нейтронов) в ядре обозначается буквой А и называется массовым числом ядра. Число нейтронов в ядре равно N = A – Z.
Для обозначения ядер применяется символ
![]()
Масса ядра измеряется в атомных единицах массы (а.е.м). За одну атомную единицу массы принимается 1/12 часть массы нейтрального атома углерода 12 С:
1а.е.м = 1.6606 10-27 кг.
А.е.м. выражается через энергетические единицы:
1а.е.м = 1.510-3 эрг = 1.510-10Дж = 931.49 МэВ
Масса ядра всегда меньше суммы масс составляющих его нуклонов. Энергия связи ядра Eсв(A,Z) это минимальная энергия, необходимая, чтобы развалить ядро на отдельные, составляющие его нуклоны.
Есв(A, Z) = [Z mp + (A - Z)mn - M(A, Z)]c2,
где Z - число протонов, ( A - Z) - число нейтронов, mp - масса протона, mn - масса нейтрона, М(A,Z) - масса ядра с массовым числом А и зарядом Z. Энергия связи ядра, выраженная через массу атома Mат, имеет вид:
Есв(A, Z) = [ZmH + (A - Z)mn - Mат(A, Z)]c2 ,
где mH - масса атома водорода.
23 главная особенность-огромное притяжение между нуклонами, резко уменьшающееся с увеличением расстояния. Ядерные сила, она очень большая по модулю, несмотря на это действует лишь на очень малом расстоянии, и никак не зависит от заряда частицы
Согласно классической физике взаимодействие между частицами осуществляется посредством силовых полей. Так, покоящийся электрический заряд создает вокруг себя электрическое поле, которое воздействует на другой заряд с некоторой силой.
Квантовая физика не изменила такое представление, но учла квантовые свойства самого поля: всякому полю должна соответствовать определенная частица – квант поля, которая и является переносчиком взаимодействия.
При взаимодействии нуклонов квантами поля являются π-мезоны, существование которых было предсказано Юкавой (1935 г.). По его оценке эти частицы занимали промежуточное положение по массе между электроном и нуклоном. И такие частицы были экспериментально обнаружены.
Взаимодействие между нуклонами, возникающее в результате обмена квантами массы m, приводит к появлению потенциала U(r):
|
|
(2.19) |
gЯ – константа взаимодействия частиц с полем квантов, переносящих ядерное взаимодействие. |
Квантовая природа подобных процессов взаимодействия заключается в том, что они могут происходить только благодаря соотношению неопределенностей. По классическим законам такие процессы идти не могут в связи с нарушением закона сохранения энергии. Ясно, что, например, покоившийся свободный нейтрон не может самопроизвольно превратиться в нейтрон +π-мезон, суммарная масса которых больше массы нейтрона.
рассмотрением двух моделей ядра: капельной и оболочечной. Более подробно об этих моделях можно посмотреть здесь.
Капельная модель
Эта простейшая модель была предложена М. Борном (1936 г.). В ней атомное ядро рассматривается как капля заряженной несжимаемой жидкости с очень высокой плотностью (~ 1014 г/см3). Капельная модель позволила вывести полуэмпирическую формулу для энергии связи ядра и помогла объяснить ряд других явлений, в частности процесс деления тяжелых ядер.
Оболочечная модель
Эта модель, предложенная Гепперт-Майер и Йенсоном в 1950 г., является более реалистичной. В данной модели считается, что каждый нуклон движется в усредненном поле остальных нуклонов ядра. В соответствии с этим имеются дискретные энергетические уровни, заполненные нуклонами с учетом принципа Паули. Эти уровни группируются в оболочки, в каждой из которых может находиться определенное число нуклонов. Полностью заполненные оболочки образуют особо устойчивые структуры
24 Радиоактивность - неустойчивость ядер некоторых атомов, проявляющаяся в их способности к самопроизвольным превращениям (распаду), сопровождающимся испусканием ионизирующего излучения - радиацией. Различают естественную и искусственную радиоактивность. Естественной называют радиоактивность естественных изотопов, т. е. химических элементов, которые встречаются в природе. Искусственной называют радиоактивность изотопов, получаемых искусственным путем. Естественная радиоактивность наблюдается у таких изотопов химических элементов, как, например, радий, ypart, торий и другие.
Закон радиоактивного распада — физический закон, описывающий зависимость интенсивности радиоактивного распада от времени и количества радиоактивных атомов в образце. Открыт Фредериком Содди и Эрнестом Резерфордом. Закон радиоактивного распада -описывает зависимость радиоактивного распада от времени и количестве радиоактивных атомов в данном образце
![]() Для
практического использования закон
радиоактивного распада можно
записать так:
Для
практического использования закон
радиоактивного распада можно
записать так:![]()
Время, за которое распадается половина первоначального числа радиоактивных ядер, называетсяпериодом полураспада (Т). Чем меньше период полураспада, тем меньше живут атомы и следовательно тем быстрее происходит радиоактивный распад.
75. Период полураспада. Важнейшей характеристикой радиоактивного атома является его время жизни. Согласно закону радиоактивного распада, вероятность того, что за данный промежуток времени произойдет распад одного атома, есть величина постоянная. Следовательно, число ежесекундно происходящих распадов пропорционально количеству имеющихся атомов, а закон, описывающий процесс распада, имеет экспоненциальный характер. Если за время Т распадается половина исходного количества радиоактивных атомов, то половина оставшихся атомов распадется в течение следующего промежутка времени той же длительности. Время Т называется периодом полураспада радиоактивного элемента. Для различных элементов период полураспада составляет от десятков миллиардов лет до миллионных долей секунды и менее.

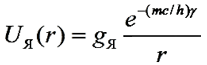 ,
,